Clear Sky Science · de
Dynamisches optisches Kohärenzmikroskop integriert mit Zellkultivierungs-Kammer für longitudinale und frühzeitige Bewertung der Wechselwirkung zwischen Tumorsphäroiden und Medikamenten
Krebszellen in Echtzeit beobachten
Krebsmedikamente werden üblicherweise danach beurteilt, wie stark sie einen Tumor verkleinern, doch bis ein Tumorvolumen sichtbar schrumpft, sind oft wertvolle Stunden oder Tage vergangen. Diese Studie stellt eine Methode vor, um winzige 3D-Cluster von Brustkrebszellen – sogenannte Tumorsphäroide – nahezu sofort nach Verabreichung eines Wirkstoffs in ihrer Reaktion zu beobachten. Durch die Kombination eines fortschrittlichen lichtbasierten Mikroskops mit einer miniaturisierten Zellkulturkammer verfolgen die Forschenden, wie lebende Krebszellen tief im Inneren der Sphäroide arbeiten, ganz ohne Farbstoffe, Marker oder Zerstörung der Probe.
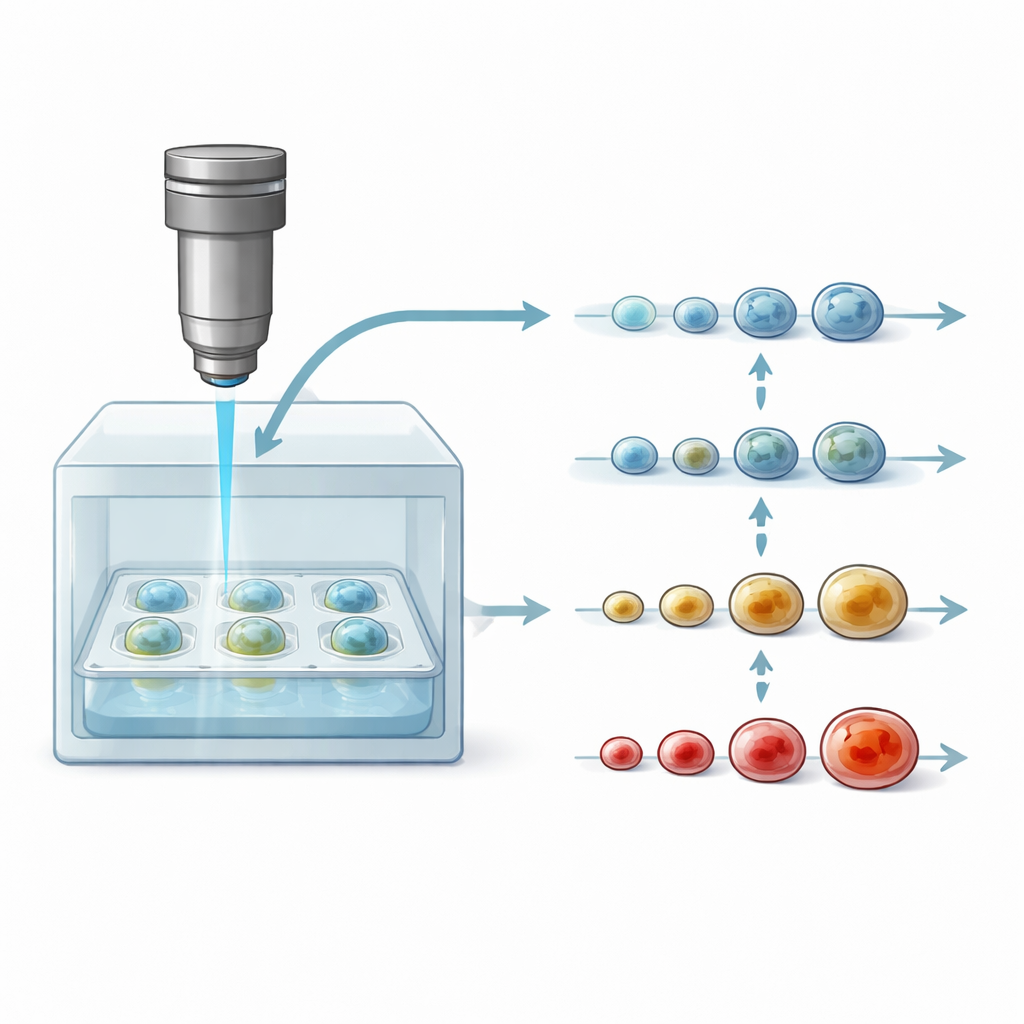
Ein neues Fenster in lebende Krebsmodelle
Forschende züchten zunehmend Tumorsphäroide, weil sie viele Eigenschaften realer Tumoren besser nachbilden als flache Zellschichten oder manche Tiermodelle. Standardwerkzeuge zur Untersuchung, wie Färbungen und Fluoreszenzbildgebung, erfordern jedoch oft das Schneiden oder chemische Verändern des Gewebes. Das bedeutet, jedes Sphäroid kann nur einmal getestet werden, und eine feinmaschige Verfolgung über die Zeit ist unmöglich. Herkömmliche optische Kohärenztomographie (OCT) – eine nichtinvasive 3D-Bildgebungsmethode, die in Augenkliniken verwendet wird – kann zwar in Sphäroide hineinsehen, zeigt aber überwiegend Form und Größe. Diese strukturellen Veränderungen treten meist spät auf, lange nachdem ein Medikament begonnen hat, die Zellgesundheit zu beeinflussen.
Bewegung als Vitalzeichen nutzen
Das Team baute auf OCT auf, indem es eine dynamische Variante, DOCT genannt, einsetzte, die nicht nur Strukturen abbildet, sondern subtile Schwankungen des Lichtsignals misst, die durch winzige Bewegungen innerhalb der Zellen entstehen. Zwei Analysemethoden – eine bewertet, wie stark das Signal über die Zeit variiert, die andere, wie schnell es entkorrigiert – wirken zusammen wie ein bewegungssensitives Stethoskop. Sind Zellen gesund und aktiv, bewegen und reorganisieren sich ihre inneren Komponenten und erzeugen ein lebhaftes DOCT-Signal. Verlangsamen sie sich, geraten sie unter Stress oder sterben sie, nimmt dieses innere Treiben ab. Indem das System „hochdynamische“ und „niederdynamische“ Bereiche innerhalb jedes Sphäroids quantifiziert, schätzt es in 3D ab, wo sich lebende und nicht-viable Zellen befinden und wie sich diese Muster entwickeln.
Zellen während der Beobachtung wohlbehalten halten
Um dasselbe Sphäroid über Tage hinweg zu verfolgen, integrierten die Forschenden ihr DOCT-Mikroskop mit einer kompakten Kultivierungskammer, die körperähnliche Bedingungen aufrechterhält: 37 °C und kontrolliertes Kohlendioxid. Eine Standard-96-Well-Platte mit vielen Sphäroiden liegt unter dem Bildgebungskopf und ist durch einen Deckel vor Kontamination geschützt. Der Lichtstrahl passiert dünne Glasschichten, um die Probe zu erreichen, und das Scannen ist schnell und schonend genug, dass jeder Punkt im Gewebe nur kurz belichtet wird. Dieses Setup erlaubte zwei Versuchsformen: eine, bei der Dutzende Sphäroide, die mit unterschiedlichen Dosen von drei gängigen Brustkrebsmedikamenten behandelt wurden, etwa alle vier Stunden für rund vier Tage abgebildet wurden, und eine andere, bei der einzelne Sphäroide automatisch alle 30 Minuten über denselben Zeitraum verfolgt wurden.
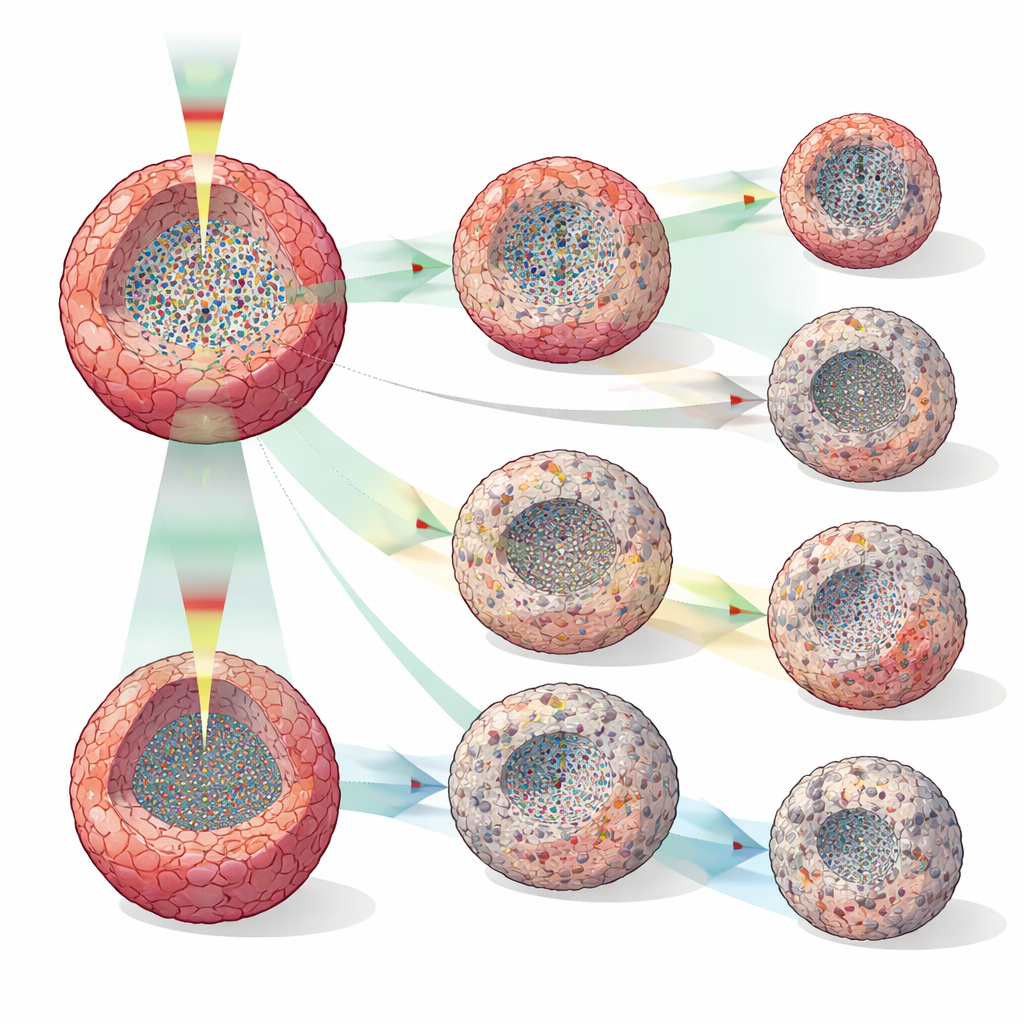
Wirkungen von Medikamenten sehen, lange bevor sich die Größe ändert
Die Gruppe behandelte menschliche Brustkrebssphäroide (MCF-7) mit Doxorubicin, Tamoxifen oder Paclitaxel in mehreren Konzentrationen und verglich DOCT‑Ausgaben mit einfachen Volumenmessungen. Während die Sphäroidgröße über viele Stunden bei verschiedenen Dosen oft ähnlich erschien, gingen die DOCT‑Metriken viel früher auseinander – manchmal schon zwei Stunden nach der Behandlung und durchweg bis zwölf Stunden. Verschiedene Wirkstoffe erzeugten unterschiedliche interne Muster: hohe Doxorubicin‑Dosen führten zu schrumpfenden Sphäroiden und zentralen Zonen reduzierter Aktivität, was auf Zelltod hindeutet; Tamoxifen verlangsamte hauptsächlich das Wachstum und bildete manchmal eine ruhige äußere Schicht, die Wachstumsstopp oder Apoptose am Rand widerspiegeln könnte; und Paclitaxel erzeugte verstreute Bereiche mit niedriger Aktivität, konsistent mit seiner bekannten Störung der Zellteilung und des intrazellulären Transports. Zeitauflösende Messungen im 30‑Minuten‑Intervall zeigten Übergangspunkte – etwa das Verschwinden und Wiederauftreten ruhiger Kerne oder die Bildung von Niedrig‑Aktivitäts‑Schichten –, die in rareren, zerstörerischen Tests unsichtbar blieben.
Was das für zukünftige Tests von Krebsmedikamenten bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft, dass dieses integrierte DOCT–Kammer‑System quasi „zuhören“ kann, wie tumorähnliche Zellcluster von innen auf Medikamente reagieren – Stunden bevor sie sichtbar wachsen oder schrumpfen. Anstatt Tage zu warten, um zu sehen, ob eine Behandlung wirkt, können Forschende frühzeitige, dosisabhängige Veränderungen der Zellaktivität ohne Zusatz von Farbstoffen oder Vernichtung der Proben erkennen. Das erleichtert den Vergleich von Wirkstoffen, die Feinabstimmung von Dosen und das Studium, warum bestimmte Tumoren resistent sind. Obwohl es derzeit noch ein Laborinstrument ist, deutet dieser Ansatz auf schnellere, aussagekräftigere präklinische Testplattformen hin, die letztlich helfen könnten, vielversprechende Krebstherapien effizienter zu identifizieren und den Einsatz von Tierversuchen zu reduzieren.
Zitation: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Schlüsselwörter: dynamische optische Kohärenztomographie, Tumorsphäroide, Krebsmedikamentenreaktion, markierungsfreie Bildgebung, longitudinale Zellkultur