Clear Sky Science · fr
Microscope de cohérence optique dynamique intégré à une chambre de culture cellulaire permettant une évaluation longitudinale et précoce de l’interaction sphéroïde tumoral‑médicament
Observer en temps réel la réponse des cellules cancéreuses
Les médicaments anticancéreux sont généralement évalués d’après la réduction du volume tumoral, mais lorsque la masse change visiblement de taille, des heures ou des jours précieux se sont déjà écoulés. Cette étude présente une méthode permettant d’observer de très petits agrégats 3D de cellules mammaires cancéreuses — appelés sphéroïdes tumoraux — répondre au traitement presque dès l’ajout du médicament. En combinant un microscope optique de pointe avec une chambre de culture miniaturisée, les chercheurs suivent le comportement des cellules vivantes à l’intérieur de ces sphéroïdes en profondeur, sans colorants, sans marqueurs et sans détruire l’échantillon.
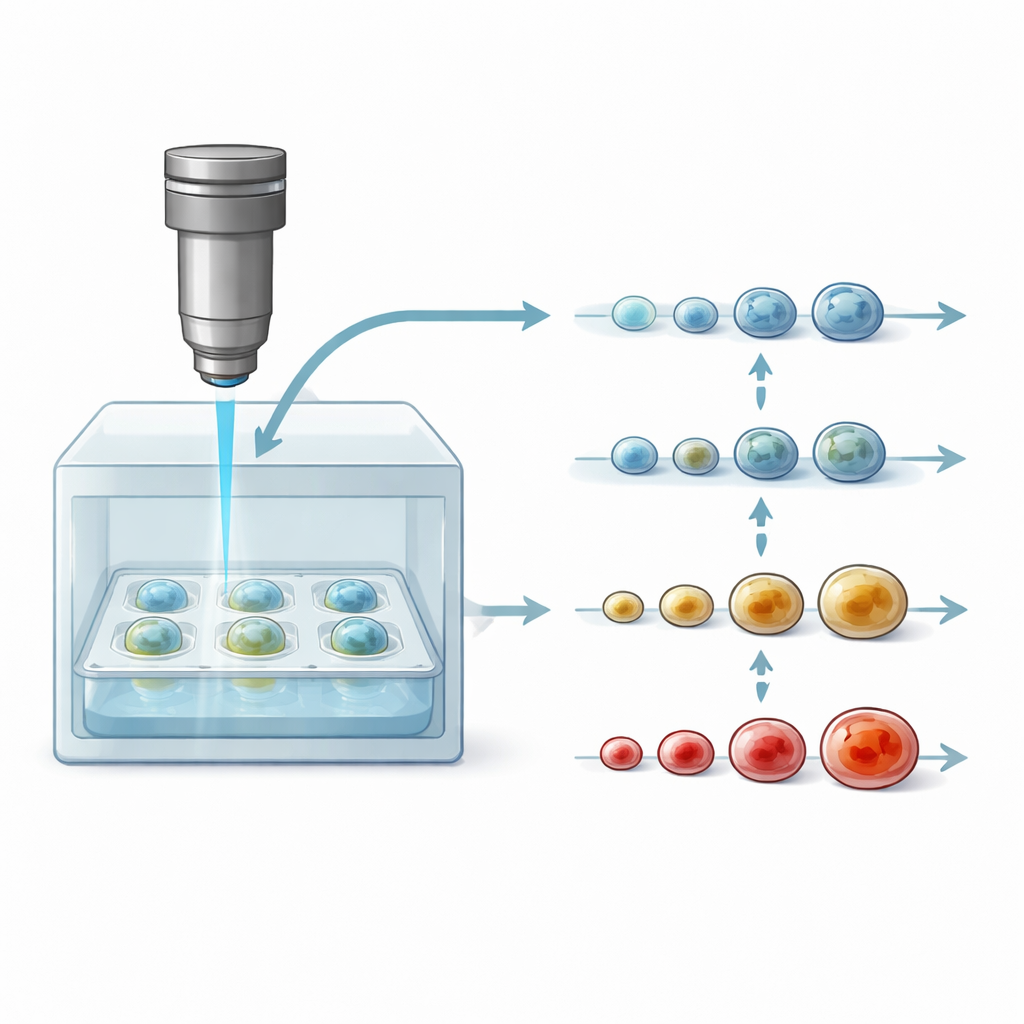
Une nouvelle fenêtre sur des modèles tumoraux vivants
Les chercheurs cultivent de plus en plus de sphéroïdes tumoraux car ils reproduisent mieux que des couches cellulaires plates ou certains modèles animaux de nombreux aspects des tumeurs réelles. Cependant, les outils standards pour les examiner, tels que les colorations et l’imagerie par fluorescence, exigent souvent de sectionner ou d’altérer chimiquement le tissu. Cela signifie que chaque sphéroïde ne peut être testé qu’une seule fois et qu’un suivi fin dans le temps est impossible. La tomographie de cohérence optique (OCT) traditionnelle — une méthode d’imagerie 3D non invasive utilisée en ophtalmologie — peut pénétrer dans les sphéroïdes, mais montre principalement la forme et la taille. Ces changements structurels apparaissent en général tardivement, bien après que le médicament ait commencé à affecter la santé cellulaire.
Transformer le mouvement en signe vital
L’équipe a étendu l’OCT en utilisant une version dynamique, appelée DOCT, qui ne se contente pas de cartographier les structures : elle mesure les fluctuations subtiles du signal lumineux provoquées par de minuscules mouvements à l’intérieur des cellules. Deux méthodes d’analyse, l’une évaluant l’amplitude des variations temporelles du signal et l’autre la vitesse de décorrélation, fonctionnent ensemble comme un stéthoscope sensible au mouvement. Quand les cellules sont saines et actives, leurs composants internes bougent et se réorganisent, produisant un signal DOCT animé. Quand les cellules ralentissent, sont stressées ou meurent, cette agitation interne diminue. En quantifiant les régions à « haute dynamique » et à « basse dynamique » à l’intérieur de chaque sphéroïde, le système estime en 3D où se trouvent les cellules viables et non viables et comment ces motifs évoluent.
Maintenir le confort des cellules pendant l’observation
Pour suivre un même sphéroïde pendant plusieurs jours, les chercheurs ont intégré leur microscope DOCT à une chambre de culture compacte qui maintient des conditions proches du corps : 37 °C et une concentration de dioxyde de carbone contrôlée. Une plaque standard à 96 puits contenant de nombreux sphéroïdes est placée sous la tête d’imagerie, protégée par un couvercle contre les contaminations. Le faisceau lumineux traverse de fines couches de verre pour atteindre l’échantillon, et le balayage est suffisamment rapide et doux pour que chaque point du tissu ne soit exposé que brièvement. Cette configuration a permis deux types d’expériences : l’une où des dizaines de sphéroïdes, traités par différentes doses de trois médicaments courants contre le cancer du sein, étaient imagés toutes les quatre heures pendant environ quatre jours, et l’autre où des sphéroïdes individuels étaient suivis automatiquement toutes les 30 minutes sur la même période.
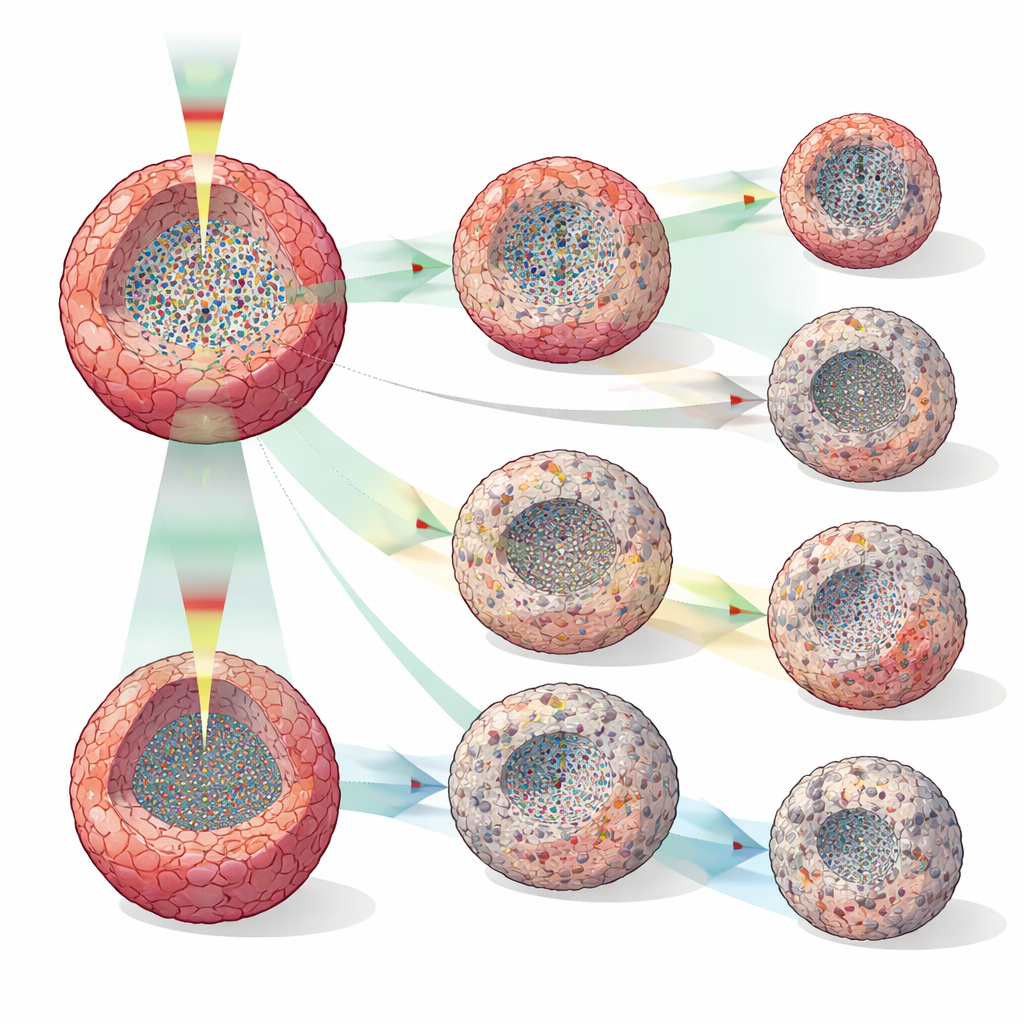
Voir les effets des médicaments bien avant les changements de taille
Le groupe a traité des sphéroïdes de cancer du sein humain (MCF‑7) par la doxorubicine, le tamoxifène ou le paclitaxel à plusieurs concentrations et a comparé les lectures DOCT avec de simples mesures de volume. Alors que la taille des sphéroïdes restait souvent similaire entre les doses pendant de nombreuses heures, les métriques DOCT divergeaient beaucoup plus tôt — parfois dès deux heures après le traitement, et de façon systématique dès 12 heures. Différents médicaments produisaient des motifs internes distincts : des doses élevées de doxorubicine entraînaient un rétrécissement des sphéroïdes et des zones centrales d’activité réduite suggérant la mort cellulaire ; le tamoxifène ralentissait principalement la croissance, formant parfois une coquille externe silencieuse pouvant refléter l’arrêt de croissance ou l’apoptose en périphérie ; et le paclitaxel produisait des taches éparses de faible activité, cohérentes avec sa perturbation connue de la division cellulaire et du transport intracellulaire. Des acquisitions à haute résolution temporelle, toutes les 30 minutes, ont révélé des points de transition — quand des noyaux silencieux disparaissaient puis réapparaissaient, ou quand des couches de faible activité se formaient — qui resteraient invisibles dans des tests destructifs et peu fréquents.
Ce que cela implique pour l’avenir des tests de médicaments anticancéreux
Pour un non‑spécialiste, le message principal est que ce système intégré DOCT–chambre peut « écouter » la façon dont des agrégats cellulaires proches de tumeurs réagissent aux médicaments de l’intérieur vers l’extérieur, des heures avant que leur croissance ou leur rétraction ne soit visible. Plutôt que d’attendre des jours pour savoir si un traitement fonctionne, les chercheurs peuvent détecter des changements précoces dépendant de la dose dans l’activité cellulaire sans ajouter de colorants ni sacrifier les échantillons. Cela facilite la comparaison des médicaments, l’ajustement des doses et l’étude des raisons pour lesquelles certaines tumeurs résistent aux thérapies. Bien qu’encore cantonnée au laboratoire, cette approche ouvre la voie à des plateformes de tests précliniques plus rapides et plus informatives qui pourraient ultimement aider à identifier plus efficacement des traitements anticancéreux prometteurs et réduire la dépendance aux expériences animales.
Citation: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Mots-clés: tomographie de cohérence optique dynamique, sphéroïdes tumoraux, réponse aux médicaments anticancéreux, imagerie sans marquage, culture cellulaire longitudinale