Clear Sky Science · sv
Dynamiskt optiskt koherensmikroskop integrerat med cellodlingskammare möjliggjorde longitudinell och tidig bedömning av tumörspheroid–läkemedelsinteraktion
Att iaktta cancerceller reagera i realtid
Cancerläkemedel bedöms vanligtvis efter hur mycket de krymper en tumör, men först när en massa synligt ändrar storlek har dyrbara timmar eller dagar ofta förflutit. Denna studie presenterar ett sätt att se små 3D-kluster av bröstcancerceller — kallade tumörspheroider — reagera på behandling nästan så fort ett läkemedel tillsätts. Genom att kombinera ett avancerat ljusbundet mikroskop med en miniaturiserad cellodlingskammare följer forskarna hur levande cancerceller beter sig djupt inne i dessa spheroider utan färgämnen, markörer eller att förstöra provet.
Ett nytt fönster in i levande cancermodeller
Forskare odlar i allt större utsträckning tumörspheroider eftersom de efterliknar många egenskaper hos verkliga tumörer bättre än plana cellskikt eller vissa djurmodeller. Standardverktyg för att undersöka dem, såsom färgning och fluorescensavbildning, kräver dock ofta att vävnaden skivas eller kemiskt förändras. Det innebär att varje spheroid bara kan testas en gång och att detaljerad uppföljning över tid blir omöjlig. Traditionell optisk koherenstomografi (OCT) — en icke-invasiv 3D-avbildningsmetod som används i ögonkliniker — kan se in i spheroider, men visar mest form och storlek. Dessa strukturella förändringar tenderar att synas sent, långt efter att ett läkemedel börjat påverka cellhälsan.
Att omvandla rörelse till ett vitalt tecken
Teamet byggde vidare på OCT genom att använda en dynamisk version, kallad DOCT, som inte bara kartlägger strukturer; den mäter subtila fluktuationer i ljussignalen orsakade av små rörelser inne i cellerna. Två analysmetoder — en som följer hur mycket signalen varierar över tiden och en annan som följer hur snabbt den avkorelateras — fungerar tillsammans som ett rörelsekänsligt stetoskop. När celler är friska och aktiva rör sig och omarrangeras deras inre komponenter, vilket skapar en livfull DOCT-signal. När cellerna saktar ner, stressas eller dör, minskar det inre myllret. Genom att kvantifiera områden med ”hög dynamik” och ”låg dynamik” inne i varje spheroid uppskattar systemet var levande respektive icke-viabla celler ligger i 3D och hur dessa mönster utvecklas.
Att hålla cellerna bekväma medan vi tittar
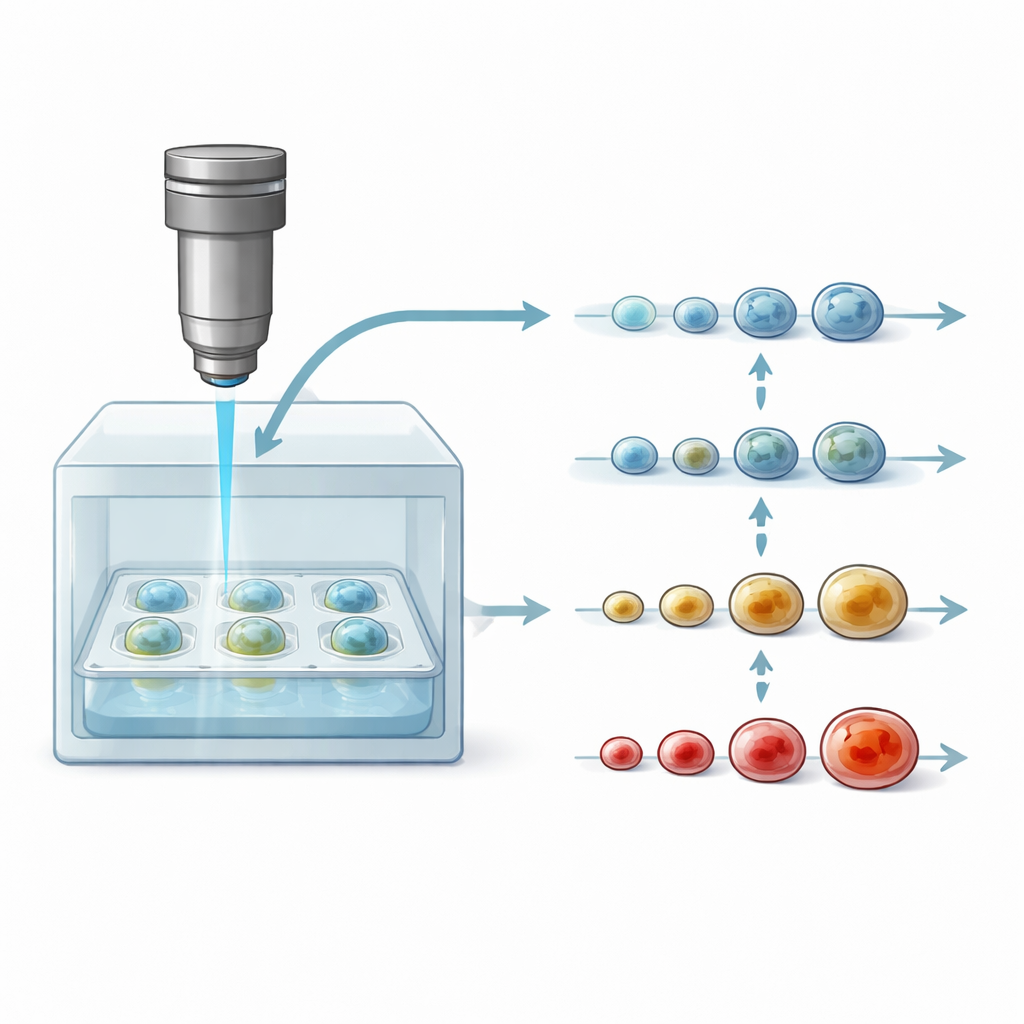
För att följa samma spheroid i flera dagar integrerade forskarna sitt DOCT-mikroskop med en kompakt odlingskammare som upprätthåller kroppslika förhållanden: 37 °C och kontrollerad koldioxidnivå. En standard 96-brunnsplatta med många spheroider står under avbildningshuvudet, skyddad av ett lock för att undvika kontaminering. Ljussignalen passerar genom tunna glaslager för att nå provet, och skanningen är tillräckligt snabb och skonsam för att varje punkt i vävnaden bara exponeras en kort stund. Denna uppställning möjliggjorde två experimentstilar: en där flera dussin spheroider, behandlade med olika doser av tre vanliga bröstcancerläkemedel, avbildades var fjärde timme i ungefär fyra dagar, och en annan där enskilda spheroider följdes automatiskt var 30:e minut under samma period.
Att se läkemedelseffekter långt före storleksförändringar
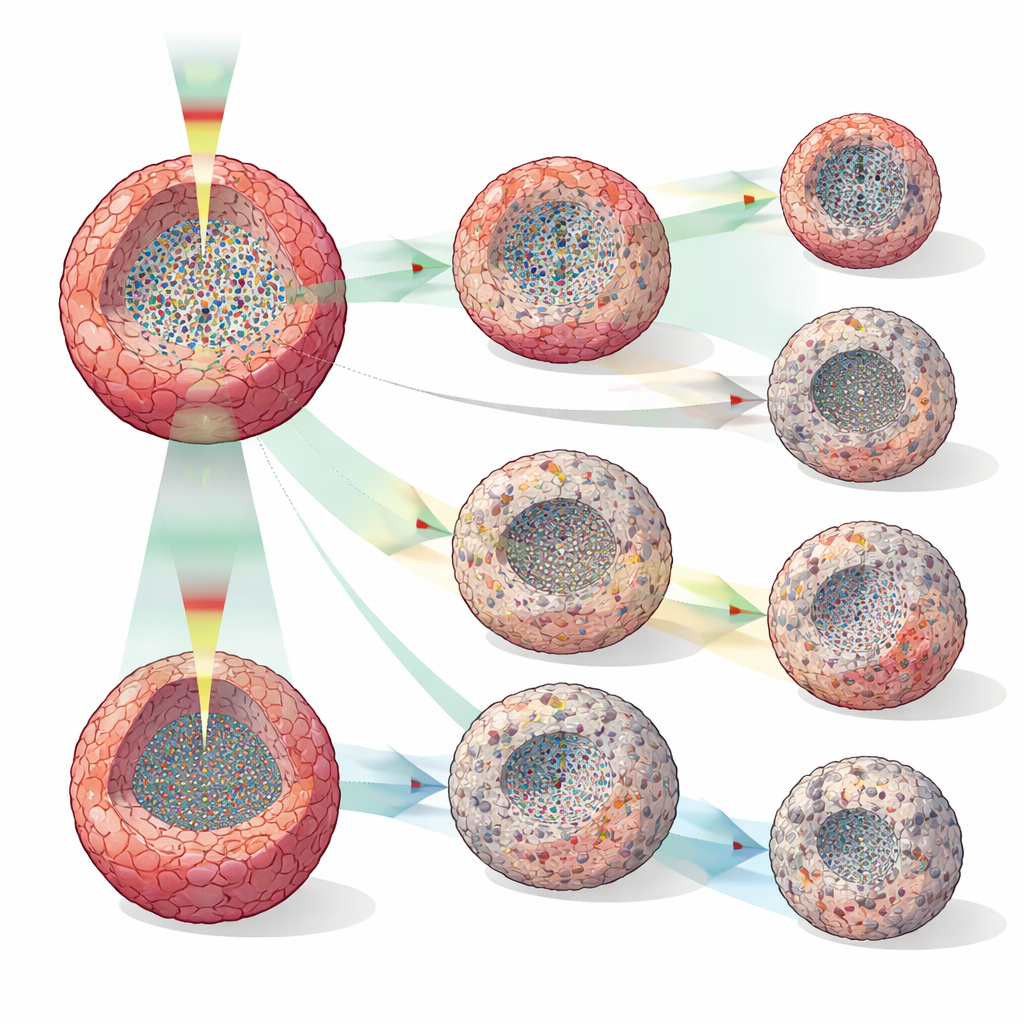
Gruppen behandlade mänskliga bröstcancerspheroider (MCF-7) med doxorubicin, tamoxifen eller paclitaxel i flera koncentrationer och jämförde DOCT-avläsningar med enkla volymmätningar. Medan spheroidernas storlek ofta såg likartad ut över doser under många timmar, skilde sig DOCT-måtten mycket tidigare — ibland redan två timmar efter behandling och konsekvent vid 12 timmar. Olika läkemedel gav distinkta interna mönster: högdos doxorubicin ledde till krympande spheroider och centrala zoner med minskad aktivitet som tyder på celldöd; tamoxifen bromsade främst tillväxten och bildade ibland ett tyst yttre skal som kan reflektera tillväxthämning eller apoptos i periferin; och paclitaxel gav spridda lågaktivitetsfläckar, i linje med dess kända störning av celldelning och intracellulär transport. Körningar med hög tidsupplösning var 30:e minut avslöjade övergångspunkter — när tysta kärnor försvann för att sedan återkomma, eller när lågaktivitetslager bildades — som vore osynliga i glesa, destruktiva tester.
Vad detta betyder för framtida cancerläkemedelstestning
För en icke-specialist är huvudbudskapet att detta integrerade DOCT–kammarsystem kan ”lyssna” på hur tumörlika cellkluster reagerar på läkemedel inifrån och ut, timmar innan de märkbart växer eller krymper. Istället för att vänta dagar för att se om en behandling fungerar, kan forskare upptäcka tidiga, dosberoende förändringar i cellaktivitet utan att tillföra färgämnen eller offra prover. Det gör det lättare att jämföra läkemedel, finjustera doser och studera varför vissa tumörer är resistenta mot behandling. Även om det fortfarande är ett laboratorieverktyg, pekar detta tillvägagångssätt mot snabbare, mer informativa prekliniska testplattformar som i förlängningen kan hjälpa till att identifiera lovande cancerbehandlingar effektivare och minska beroendet av djurexperiment.
Citering: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Nyckelord: dynamisk optisk koherenstomografi, tumörspheroider, cancerläkemedelsrespons, märkningsfri avbildning, longitudinell cellkultur