Clear Sky Science · pt
Microscópio de coerência óptica dinâmico integrado com câmara de cultivo celular possibilitou avaliação longitudinal e em estágio inicial da interação entre fármaco e esferoide tumoral
Observando células cancerígenas responderem em tempo real
Medicamentos contra o câncer costumam ser avaliados pela redução do tamanho do tumor, mas quando uma massa muda visivelmente de tamanho, horas ou dias preciosos já se passaram. Este estudo apresenta uma forma de acompanhar pequenos agregados 3D de células de câncer de mama — chamados esferoides tumorais — respondendo ao tratamento quase imediatamente após a administração do fármaco. Ao combinar um microscópio avançado baseado em luz com uma câmara de cultivo celular miniaturizada, os pesquisadores acompanham o comportamento de células cancerígenas vivas no interior desses esferoides sem corantes, marcadores ou destruição da amostra.
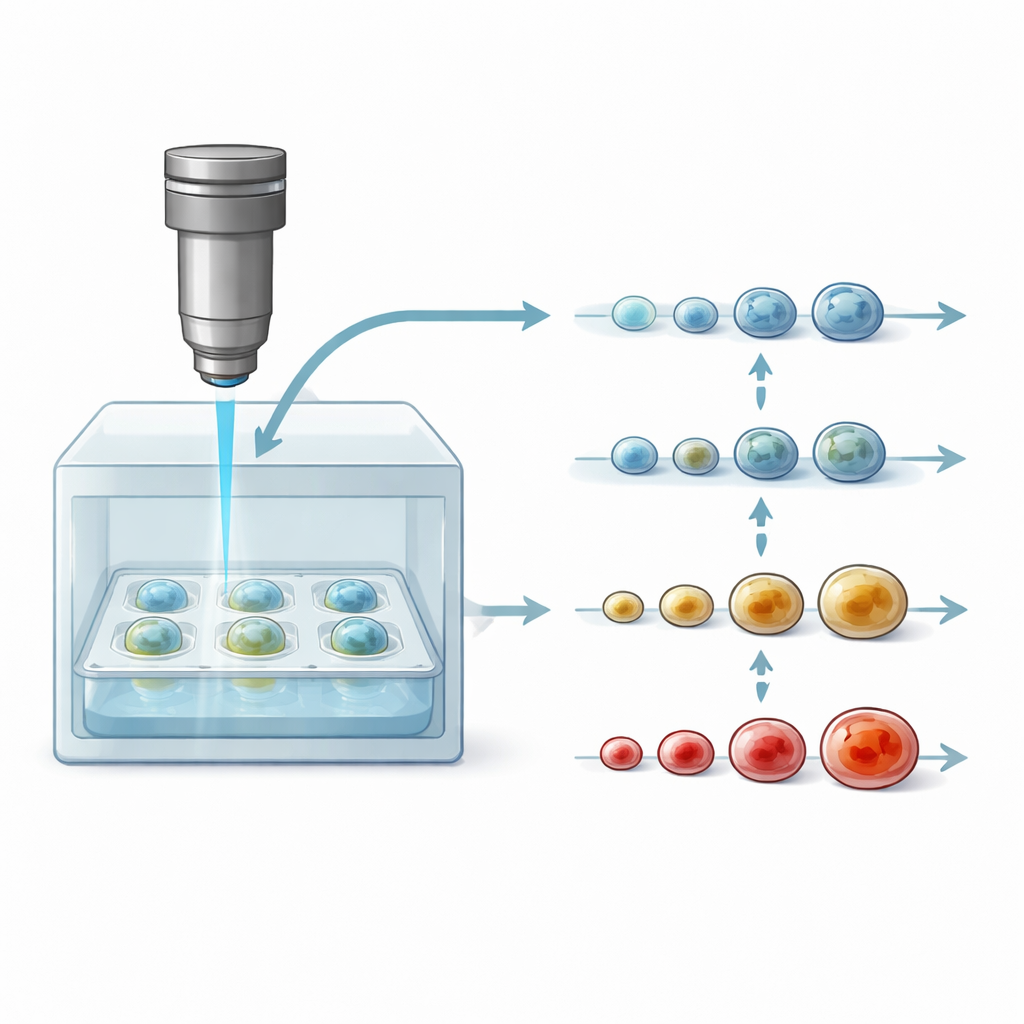
Uma nova janela para modelos de câncer vivos
Pesquisadores cultivam cada vez mais esferoides tumorais porque eles imitam muitas características de tumores reais melhor do que camadas celulares planas ou alguns modelos animais. Entretanto, ferramentas padrão para examiná‑los, como coloração e imagem por fluorescência, frequentemente exigem cortar ou alterar quimicamente o tecido. Isso significa que cada esferoide pode ser testado apenas uma vez, e o acompanhamento detalhado ao longo do tempo é impossível. A tomografia de coerência óptica (OCT) tradicional — um método de imagem 3D não invasivo usado em clínicas oftalmológicas — consegue visualizar o interior dos esferoides, mas mostra principalmente forma e tamanho. Essas mudanças estruturais tendem a surgir tardiamente, muito depois de o fármaco já ter começado a afetar a saúde celular.
Transformando movimento em um sinal vital
A equipe partiu da OCT usando uma versão dinâmica, chamada DOCT, que não apenas mapeia estruturas; ela mede flutuações sutis no sinal de luz causadas por pequenos movimentos dentro das células. Dois métodos de análise — um que acompanha quão variável é o sinal ao longo do tempo e outro que mede a rapidez com que ele perde correlação — atuam em conjunto como um estetoscópio sensível ao movimento. Quando as células estão saudáveis e ativas, seus componentes internos se movem e se reorganizam, gerando um sinal DOCT vívido. Quando as células desaceleram, ficam estressadas ou morrem, esse agito interno diminui. Ao quantificar regiões de “alta dinâmica” e “baixa dinâmica” dentro de cada esferoide, o sistema estima onde se situam células viáveis e não viáveis em 3D e como esses padrões evoluem.
Mantendo as células confortáveis enquanto observamos
Para seguir o mesmo esferoide por dias, os pesquisadores integraram seu microscópio DOCT a uma câmara de cultivo compacta que mantém condições semelhantes às do corpo: 37°C e dióxido de carbono controlado. Uma placa padrão de 96 poços contendo muitos esferoides fica sob a cabeça de imagem, protegida por uma tampa para evitar contaminação. O feixe de luz passa por camadas finas de vidro para alcançar a amostra, e a varredura é rápida e suave o suficiente para que cada ponto do tecido seja exposto apenas brevemente. Essa configuração permitiu dois estilos de experimento: um em que dezenas de esferoides, tratados com diferentes doses de três fármacos comuns para câncer de mama, foram imageados a cada quatro horas por cerca de quatro dias; e outro em que esferoides individuais foram acompanhados automaticamente a cada 30 minutos pelo mesmo período.
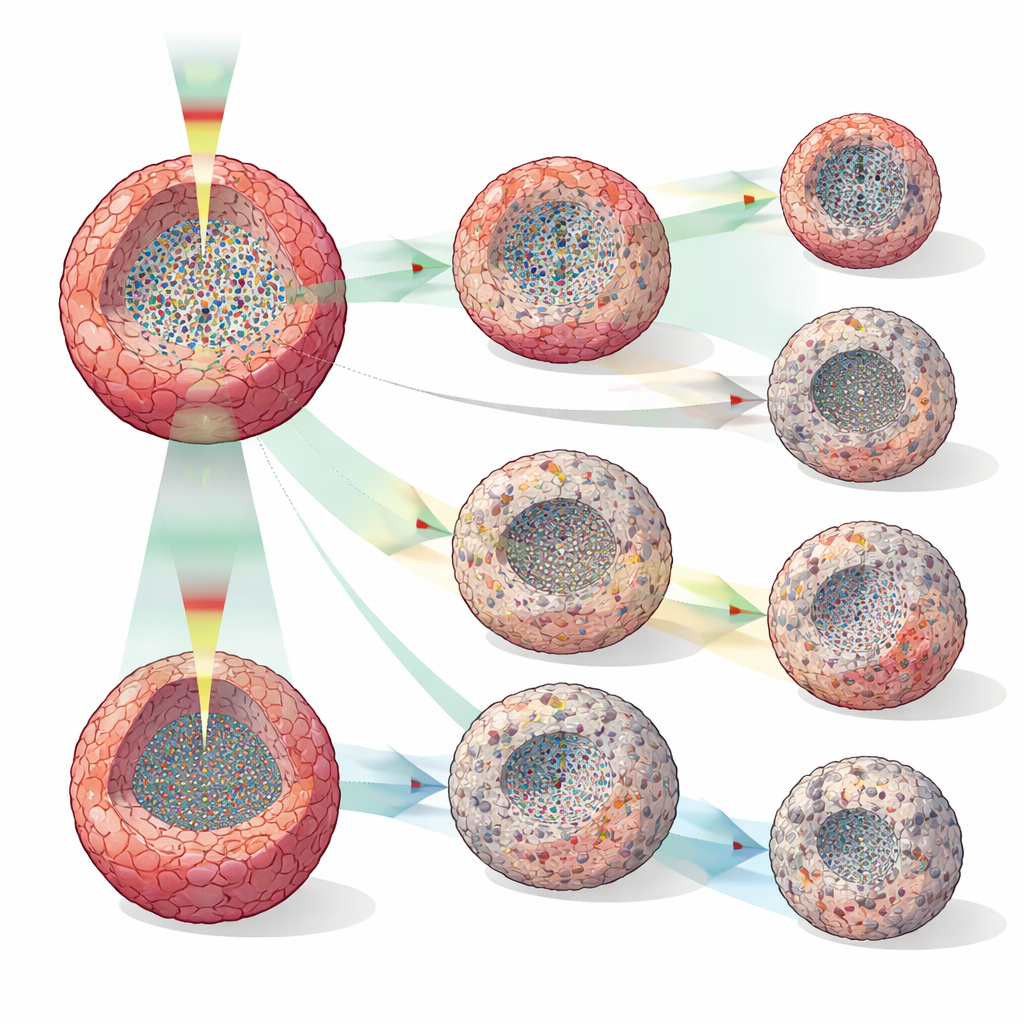
Detectando efeitos de fármacos muito antes de mudanças no tamanho
O grupo tratou esferoides de câncer de mama humano (MCF-7) com doxorrubicina, tamoxifeno ou paclitaxel em várias concentrações e comparou as leituras DOCT com medições simples de volume. Enquanto o tamanho dos esferoides frequentemente parecia semelhante entre doses por muitas horas, as métricas DOCT divergiam muito antes — às vezes apenas duas horas após o tratamento, e de forma consistente em 12 horas. Diferentes fármacos produziram padrões internos distintos: doxorrubicina em altas doses levou a esferoides encolhidos e zonas centrais de atividade reduzida sugestivas de morte celular; tamoxifeno reduziu principalmente o crescimento, por vezes formando uma camada externa silenciosa que pode refletir parada do crescimento ou apoptose na periferia; e paclitaxel gerou manchas dispersas de baixa atividade, compatíveis com sua conhecida interrupção da divisão celular e do transporte intracelular. Ensaios de alta resolução temporal, a cada 30 minutos, revelaram pontos de transição — quando núcleos silenciosos desapareciam e depois reapareciam, ou quando camadas de baixa atividade se formavam — que seriam invisíveis em testes esparsos e destrutivos.
O que isso significa para futuros testes de fármacos contra o câncer
Para um público não especialista, a mensagem principal é que esse sistema integrado DOCT–câmara pode “ouvir” como agregados celulares semelhantes a tumores reagem aos fármacos de dentro para fora, horas antes de mostrarem crescimento ou redução perceptíveis. Em vez de esperar dias para saber se um tratamento funciona, os pesquisadores podem detectar mudanças precoces dependentes da dose na atividade celular sem adicionar corantes ou sacrificar amostras. Isso facilita comparar fármacos, ajustar doses e estudar por que certos tumores resistem à terapia. Embora ainda seja uma ferramenta de laboratório, essa abordagem aponta para plataformas pré-clínicas de testes de fármacos mais rápidas e informativas, que em última instância poderiam ajudar a identificar tratamentos promissores contra o câncer com mais eficiência e reduzir a dependência de experimentos em animais.
Citação: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Palavras-chave: tomografia de coerência óptica dinâmica, esferoides tumorais, resposta a fármacos contra o câncer, imagem sem marcação, cultura celular longitudinal