Clear Sky Science · it
Microscopio dinamico a coerenza ottica integrato con camera di coltura cellulare per valutazioni longitudinali e precoci dell’interazione tra sferoidi tumorali e farmaci
Osservare in tempo reale la risposta delle cellule tumorali
I farmaci antitumorali vengono solitamente valutati in base a quanto riducono un tumore, ma quando una massa cambia visibilmente dimensione possono essere trascorse ore o giorni preziosi. Questo studio presenta un metodo per osservare piccoli ammassi 3D di cellule del cancro al seno—detti sferoidi tumorali—che rispondono al trattamento quasi non appena viene aggiunto un farmaco. Combinando un microscopio ottico avanzato con una camera di coltura compatta, i ricercatori monitorano il comportamento delle cellule vive all’interno di questi sferoidi senza coloranti, marcatori o la distruzione del campione.
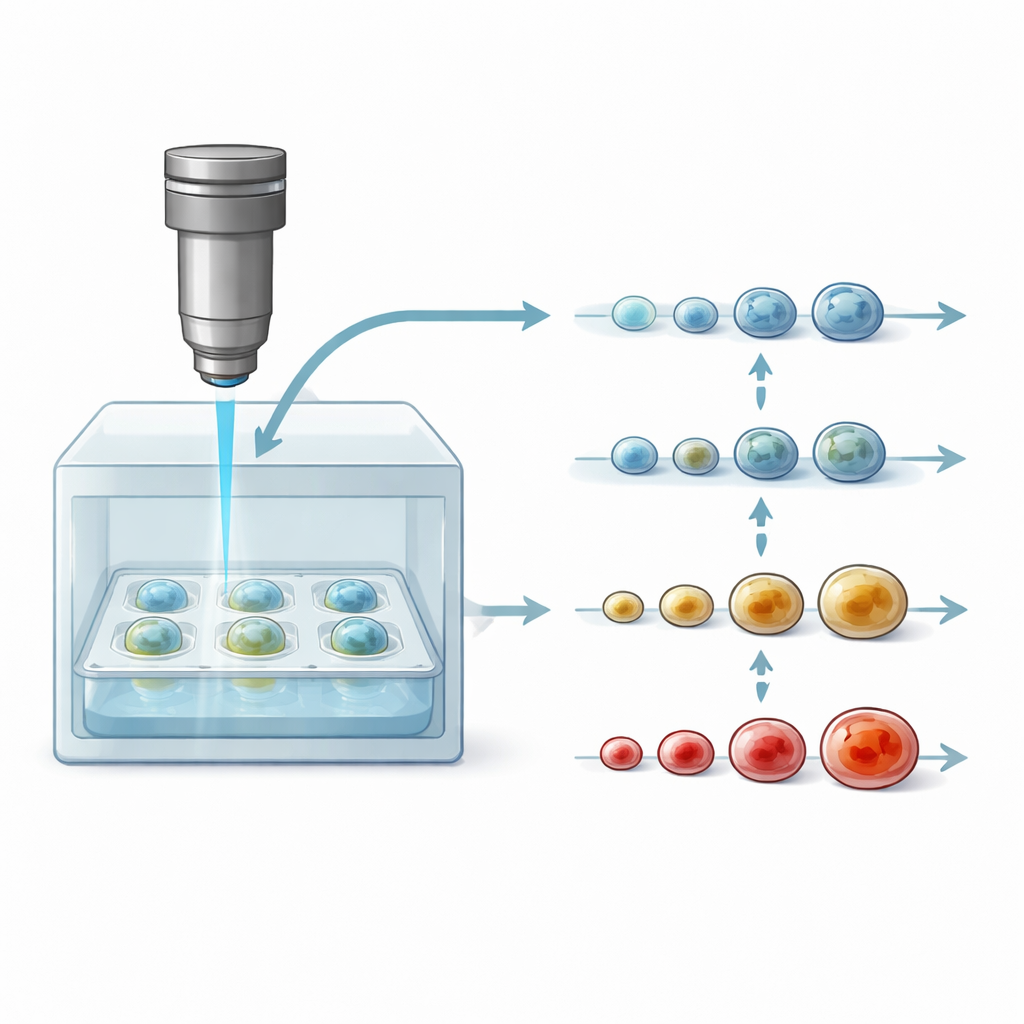
Una nuova finestra sui modelli tumorali vivi
I ricercatori coltivano sempre più spesso sferoidi tumorali perché riproducono molte caratteristiche dei tumori reali meglio di strati cellulari piatti o di alcuni modelli animali. Tuttavia, gli strumenti standard per esaminarli, come la colorazione e l’imaging a fluorescenza, spesso richiedono il sezionamento o l’alterazione chimica del tessuto. Questo significa che ogni sferoide può essere analizzato una sola volta e il tracciamento dettagliato nel tempo risulta impossibile. La tomografia a coerenza ottica tradizionale (OCT)—una tecnica di imaging 3D non invasiva utilizzata nelle cliniche oftalmiche—può vedere all’interno degli sferoidi, ma mostra principalmente forma e dimensione. Questi cambiamenti strutturali tendono a manifestarsi in fase avanzata, molto tempo dopo che un farmaco ha iniziato a influenzare la salute cellulare.
Trasformare il movimento in un segno vitale
Il gruppo ha sviluppato l’OCT usando una versione dinamica, chiamata DOCT, che non si limita a mappare le strutture; misura le sottili fluttuazioni del segnale luminoso causate da microscopici movimenti all’interno delle cellule. Due metodi di analisi, uno che monitora l’ampiezza delle variazioni temporali del segnale e un altro che ne misura la velocità di decorrelazione, lavorano insieme come uno stetoscopio sensibile al movimento. Quando le cellule sono sane e attive, i loro componenti interni si muovono e si riorganizzano, producendo un segnale DOCT vivace. Quando le cellule rallentano, sono stressate o muoiono, quel fermento interno diminuisce. Quantificando regioni a “alta dinamicità” e a “bassa dinamicità” all’interno di ciascuno sferoide, il sistema stima dove si trovano in 3D le cellule vive e non vitali e come questi schemi evolvono nel tempo.
Mantenere il comfort cellulare mentre osserviamo
Per seguire lo stesso sferoide per giorni, i ricercatori hanno integrato il loro microscopio DOCT con una camera di coltura compatta che mantiene condizioni simili a quelle corporee: 37 °C e CO2 controllato. Una piastra standard a 96 pozzetti contenente molti sferoidi è posizionata sotto la testa di imaging, protetta da un coperchio per evitare contaminazioni. Il raggio luminoso attraversa sottili strati di vetro per raggiungere il campione, e la scansione è abbastanza rapida e delicata da esporre ciascun punto del tessuto solo per breve tempo. Questa configurazione ha permesso due tipi di esperimento: uno in cui dozzine di sferoidi, trattati con dosi diverse di tre comuni farmaci per il cancro al seno, sono stati immaginati ogni quattro ore per circa quattro giorni, e un altro in cui singoli sferoidi sono stati seguiti automaticamente ogni 30 minuti per lo stesso periodo.
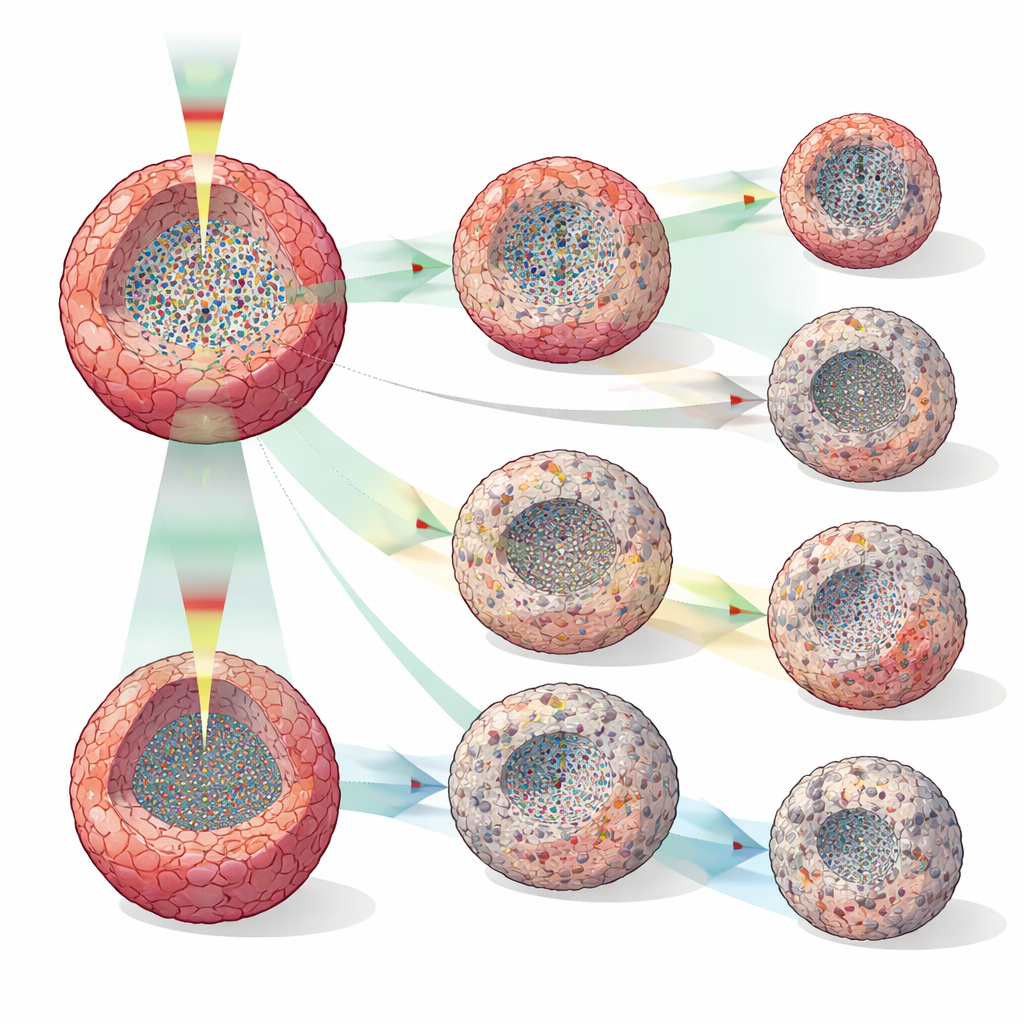
Osservare gli effetti dei farmaci molto prima dei cambiamenti di dimensione
Il gruppo ha trattato sferoidi di carcinoma mammario umano (MCF-7) con doxorubicina, tamoxifene o paclitaxel a diverse concentrazioni e ha confrontato le letture DOCT con semplici misure di volume. Mentre la dimensione degli sferoidi spesso appariva simile tra le diverse dosi per molte ore, le metriche DOCT divergono molto prima—talvolta già dopo due ore dal trattamento e in modo consistente entro 12 ore. Diversi farmaci produssero pattern interni distinti: alte dosi di doxorubicina portarono a sferoidi più piccoli e a zone centrali di attività ridotta suggerendo morte cellulare; il tamoxifene rallentò principalmente la crescita, talvolta formando un guscio esterno quieto che potrebbe riflettere arresto della crescita o apoptosi periferica; e il paclitaxel generò chiazze disperse a bassa attività, coerenti con la sua nota interferenza nella divisione cellulare e nel trasporto intracellulare. Le acquisizioni ad alta risoluzione temporale ogni 30 minuti rivelarono punti di transizione—quando i nuclei quieti scomparivano e poi ricomparivano, o quando si formavano strati a bassa attività—che sarebbero stati invisibili in test distruttivi e scarsi nel tempo.
Cosa significa per il futuro dei test sui farmaci antitumorali
Per un pubblico non specialistico, il messaggio chiave è che questo sistema integrato DOCT–camera può “ascoltare” come ammassi cellulari simili a tumori reagiscono ai farmaci dall’interno verso l’esterno, ore prima che siano visibilmente cresciuti o ridotti. Invece di aspettare giorni per vedere se un trattamento funziona, i ricercatori possono rilevare precoci cambiamenti dipendenti dalla dose nell’attività cellulare senza aggiungere coloranti o sacrificare i campioni. Questo facilita il confronto fra farmaci, la messa a punto delle dosi e lo studio dei meccanismi di resistenza tumorale. Pur rimanendo uno strumento di laboratorio, l’approccio indica piattaforme precliniche più rapide e informative che potrebbero, in futuro, aiutare a identificare trattamenti antitumorali promettenti in modo più efficiente e ridurre la dipendenza dagli esperimenti su animali.
Citazione: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Parole chiave: tomografia dinamica a coerenza ottica, sferoidi tumorali, risposta ai farmaci antitumorali, immagine senza marcatori, coltura cellulare longitudinale