Clear Sky Science · tr
Termoresponsif allosterik proteinların modüler mühendisliği
Sıcaklığı Nazik Bir Açık–Kapalı Anahtarına Çevirmek
Hücre içindeki neredeyse herhangi bir proteinin etkinliğini yalnızca birkaç derece ısıtarak kontrol edebilseydiniz—ilaç yok, güçlü ışık yok, sadece küçük bir sıcaklık değişimi—ne olurdu? Bu çalışma, araştırmacıların böyle ısıya duyarlı protein “anahtarlarını” modüler bir biçimde nasıl inşa edebileceklerini, birçok farklı proteine takılabilecek parçalardan yararlanarak gösteriyor. Ortaya çıkan yeni araç seti, bir gün gen terapilerine rehberlik etmeye, mikrobiyal tedavileri hassaslaştırmaya veya hücrelerin nasıl çalıştığını keşfetmeye yardımcı olabilir; tümü normal vücut ısısı çevresindeki dar sıcaklık aralığından yararlanarak.
Neden Sıcaklık Güçlü ve Görünmez Bir Uzaktan Kumandadır
Bilim insanları hücre içindeki proteinleri açıp kapatmak için zaten ışık ve kimyasallar kullanıyor, ancak her ikisinin de pratik sakıncaları var. Işık genellikle dokulara derinlemesine nüfuz etmez ve kimyasallar yavaş yayılabilir ve vücudun birçok bölümünü aynı anda etkileyebilir. Buna karşın sıcaklık, dokuları iyi geçirir ve uzay ile zaman içinde çok hassas şekilde odaklanabilir. Sorun şu ki, mevcut termal araçların çoğu ya aşırı sıcaklıklarda çalışıyor ya da esasen gen ifadesini dolaylı olarak kontrol ediyor. Yazarların hedefi, sıradan bir proteini alıp 37–41 °C aralığındaki küçük sıcaklık değişimlerine keskin bir yanıt verecek hâle getirebilecek genel bir strateji yaratmaktı—yaklaşık olarak normal vücut ısısı ile hafif bir ateş arasındaki fark kadar.
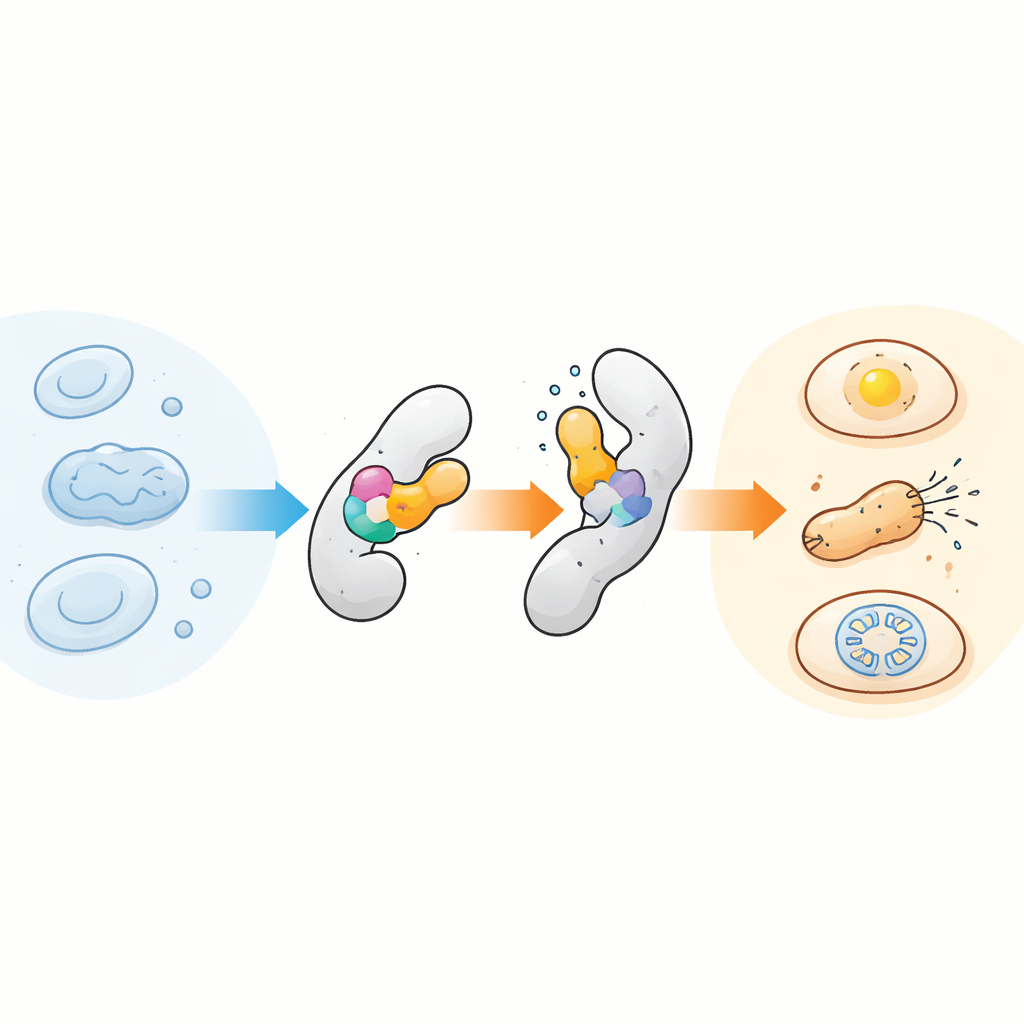
Küçük Bir Sensörü Birçok Proteine Takmak
Temel fikir şaşırtıcı derecede basit: kompakt, sıcaklığa duyarlı bir sensör alanını başka bir proteine yerleştirin; böylece sensördeki küçük yapısal değişiklik konağa iletilir ve içsel bir menteşe gibi davranır. Ekip, doğal olarak farklı şekiller arasında değişebilen ve bu nedenle iyi incelenmiş bir modül olan AsLOV2’ye odaklandı; AsLOV2, başlangıçta yulaflardan gelen bir ışık sensörüdür. Araştırmacılar bu domainin, belirli mutasyonlarla biraz kararsızlaştırıldığında, sıcaklığa da şaşırtıcı derecede duyarlı olduğunu keşfettiler. AsLOV2’nin uyarlanmış sürümlerini hedef proteinlerin farklı konumlarına yerleştirerek, aktivitesi yalnızca birkaç derece içinde keskin şekilde açılıp kapanan kimerik proteinler yarattılar. Bakterilerde bunu önce bir transkripsiyon faktörü olan AraC ile gösterdiler ve ardından sıcaklık yanıtını daha dik, ayarlanabilir ve zamanla tersinir hâle getiren AsLOV2 varyantlarını evrimleştirdiler.
Bakteriyel Öldürme Anahtarlarından Moleküler Termostatlara
Yöntem bir proteinde işe yarayınca, yazarlar bunu görevleri çok farklı olan diğer proteinlere uyguladılar. Sensörün bir antibiyotik direnç enziminin içine yerleştirilmesi, onu ısı tetikli bir öldürme anahtarına dönüştürdü: bakteriler 37 °C’de büyürken, ilaca maruz kaldıklarında 41 °C’de öldüler. Benzer bir strateji sensörü, bakterilerde gen ekspresyonunu nazik ısıtmayla yukarı ya da aşağı ayarlamaya izin veren CRISPR tabanlı bir gen aktivatörünün bir bileşenine bağladı. Ekip ayrıca sensörün kuyruğunun ısı kaynaklı hareketleriyle kısa sinyal peptitlerinin gizlenip açılması fikrini de keşfetti; bu mekanizma, bakterilerde sıcaklığa bağlı protein yıkımını ve insan hücrelerinde çekirdek ile sitoplazma arasındaki protein trafiğinin ılımlı kontrolünü mümkün kıldı.
İnsan Hücrelerinde Isıya Ayarlı Genom Düzenleme Kontrolü
En çarpıcı gösterimler yöntemin memeli hücrelerindeki CRISPR araçlarına uyarlanmasından geldi. Bir tasarımda sensör, normalde bir genom düzenleyiciyi engelleyen bir anti‑CRISPR proteinine yerleştirildi; hücrelerin ısıtılması bu inhibitörü zayıflattı ve düzenlemenin 37 °C ile 40 °C arasında birkaç kat artmasına izin verdi. Başka bir tasarımda sensör doğrudan Cas9’un içine inşa edildi; böylece ısı uygulandığında düzenleme artmak yerine azaldı. Her iki mod da birçok hedef gen üzerinde çalıştı, hücre sağlığı üzerinde çok az etki bıraktı ve CRISPR‑tabanlı transkripsiyonel aktivatörlere de aktarılabildi. Araştırmacılar daha sonra tamamen farklı bir reseptör modülünün—bir hormon reseptöründen kortizol algılayan bir domainin—özellikle hormon mevcut olduğunda alternatif bir sıcaklığa duyarlı insert olarak hizmet edebileceğini gösterdiler. Bu, yalnızca ışık reseptörlerinin değil, birçok doğal sensör domaininin de olağan çalışma sıcaklıklarının biraz üzerine çıkarıldığında kararsızlaşıp anahtar benzeri davranışlar gösterebileceğini düşündürüyor.
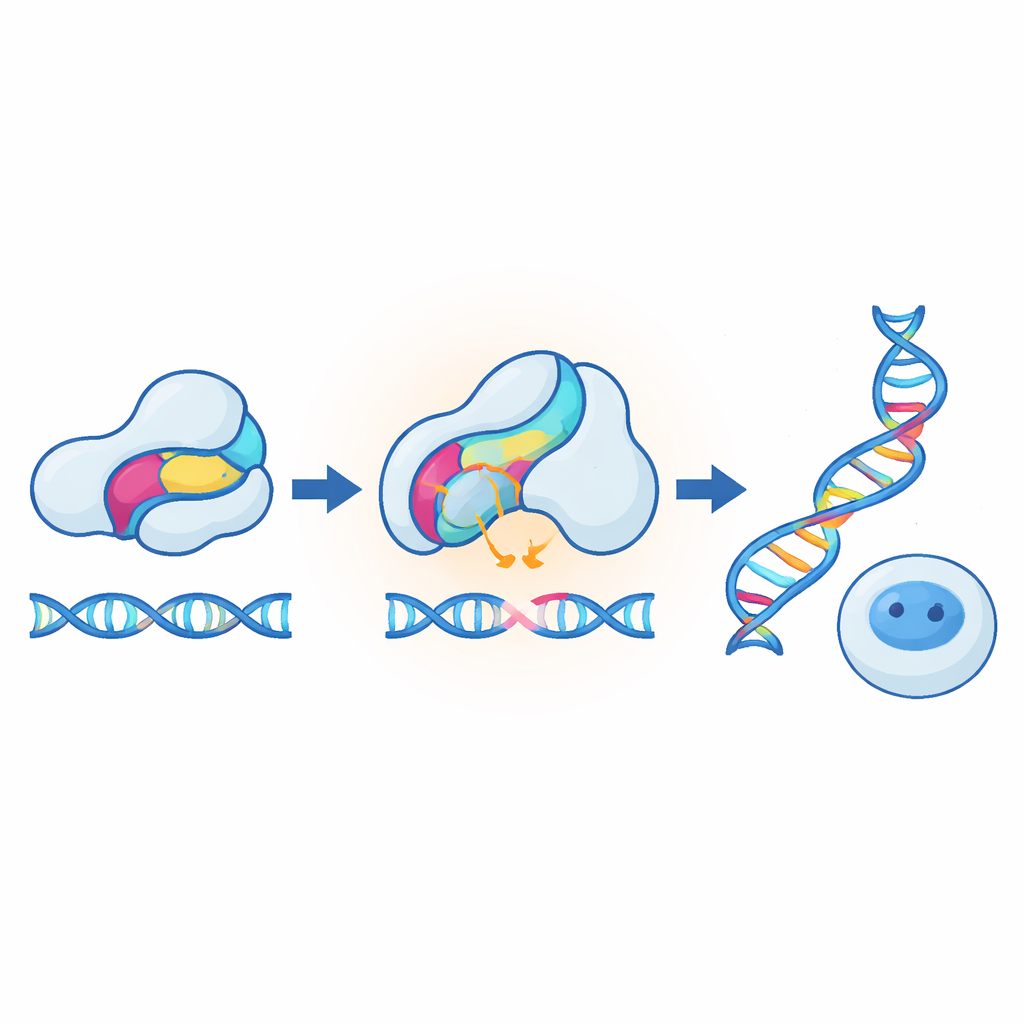
Gelecek Terapiler ve Araçlar İçin İfade Ettikleri
Bir okuyucu için çıkarım şudur: Yazarlar, sıradan proteinleri hassas biyolojik termostatlara dönüştürmek için genel bir reçete geliştirdiler. Küçük sensör domainleri ekleyip bunların stabilitesini hassas şekilde ayarlayarak, protein etkinliğinin normal insan aralığında seçilmiş sıcaklıklarda aniden yükselmesini veya düşmesini sağlayabiliyorlar. Strateji modüler olduğundan, birçok mevcut optogenetik ve kemogenetik tasarımla uyumlu olmalı ve yalnızca gen ifadesinde değil doğrudan protein fonksiyonu düzeyinde çalışabilir. Uzun vadede, bu tür sıcaklığa duyarlı anahtarlar gen düzenlemeyi daha güvenli ve daha kontrol edilebilir kılmaya, istenmeyen koşullar dışında kendi kendini imha eden ısı‑yönlendirmeli bakteriler oluşturmasına ve biyologlara hücrelerin en hafif ısınma değişimlerine nasıl tepki verdiğini araştırmak için yeni ve ince yöntemler sağlamaya yardımcı olabilir.
Atıf: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Anahtar kelimeler: termogenetik, protein anahtarları, CRISPR kontrolü, allosterik regülasyon, sıcaklık algılama