Clear Sky Science · de
Modulare Entwicklung thermoresponsiver allosterischer Proteine
Wärme als sanfter An‑/Aus‑Schalter
Stellen Sie sich vor, Sie könnten die Aktivität nahezu jedes Proteins in einer lebenden Zelle allein durch Erwärmen um ein paar Grad steuern—keine Medikamente, kein starkes Licht, nur eine kleine Temperaturänderung. Diese Studie zeigt, wie Forschende solche wärmeempfindlichen Protein‑„Schalter“ modular bauen können, mit Bausteinen, die in viele verschiedene Proteine eingesetzt werden können. Das Ergebnis ist ein neues Werkzeugset, das eines Tages helfen könnte, Gentherapien zu steuern, mikrobiologische Behandlungen zu verfeinern oder die Zellbiologie zu erforschen—alles durch Ausnutzung des engen Temperaturbereichs um die normale Körpertemperatur.
Warum Temperatur eine starke, unsichtbare Fernbedienung ist
Wissenschaftler nutzen bereits Licht und Chemikalien, um Proteine in Zellen an‑ oder auszuschalten, doch beide Ansätze haben praktische Nachteile. Licht dringt oft nicht tief in Gewebe ein, und Chemikalien können sich langsam verteilen und viele Körperbereiche gleichzeitig beeinflussen. Temperatur hingegen durchdringt Gewebe gut und lässt sich sehr gezielt in Raum und Zeit anwenden. Die Herausforderung war, dass die meisten vorhandenen thermischen Werkzeuge entweder nur bei extremen Temperaturen funktionieren oder hauptsächlich indirekt die Genexpression steuern. Die Autoren verfolgten das Ziel, eine allgemeine Strategie zu entwickeln, mit der sich ein beliebiges Protein so verändern lässt, dass es scharf auf kleine Temperaturschwankungen im Bereich von 37–41 °C reagiert—ungefähr der Unterschied zwischen normaler Körpertemperatur und leichtem Fieber.
Ein winziger Sensor, einsetzbar in vielen Proteinen
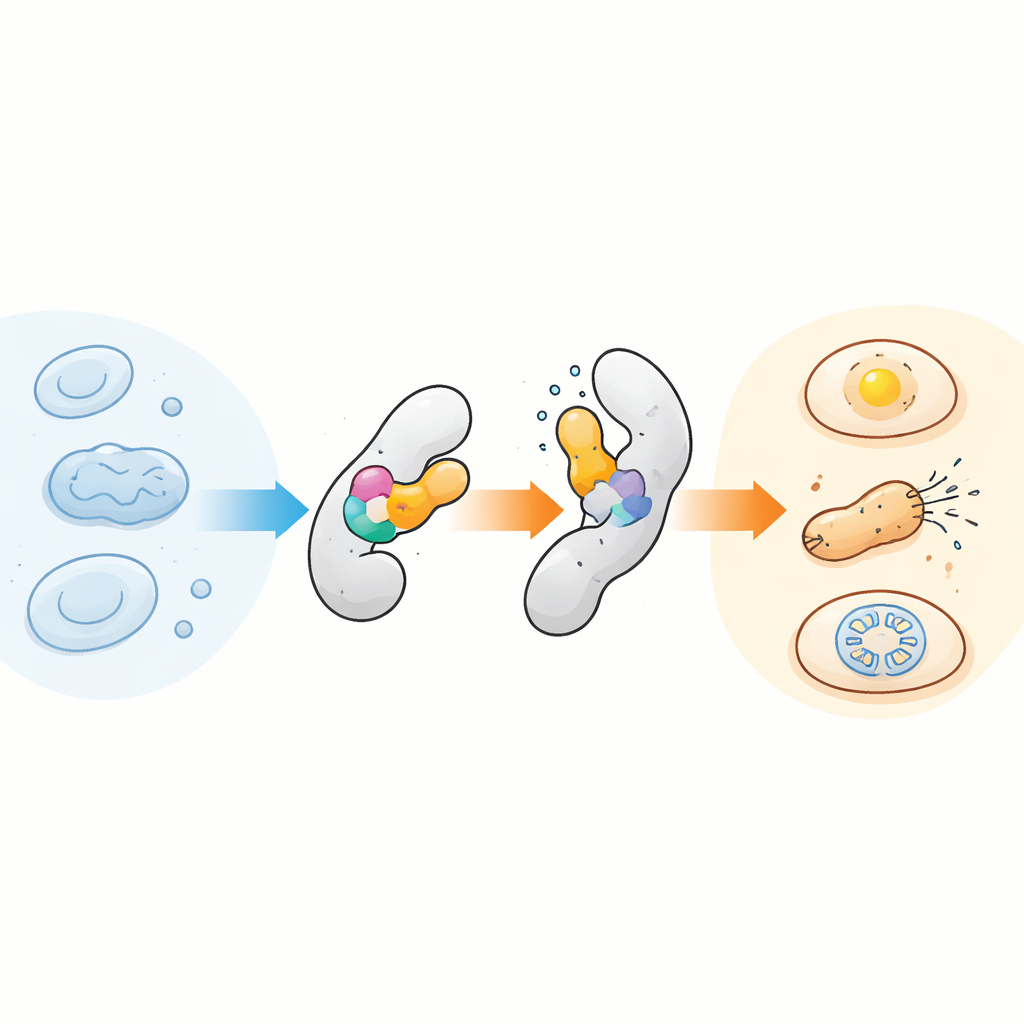
Die Kernidee ist verblüffend einfach: Ein kompakter, temperaturempfindlicher Sensordomäne in ein anderes Protein einfügen, sodass eine kleine strukturelle Änderung im Sensor auf das Wirtsprotein übertragen wird und wie ein inneres Scharnier wirkt. Das Team konzentrierte sich auf ein gut untersuchtes Modul namens AsLOV2, ursprünglich ein Lichtsensor aus Hafer, weil es natürlich zwischen unterschiedlichen Konformationen umschaltet. Sie entdeckten, dass diese Domäne zudem überraschend temperaturanfällig ist, besonders wenn sie durch gezielte Mutationen leicht destabilisiert wird. Durch das Einsetzen maßgeschneiderter AsLOV2‑Varianten an verschiedenen Positionen in Zielproteine erzeugten sie chimäre Proteine, deren Aktivität bereits über wenige Grad scharf ein‑ oder ausgeschaltet wird. In Bakterien zeigten sie dies zunächst mit AraC, einem Transkriptionsfaktor, und entwickelten dann AsLOV2‑Varianten weiter, die die Temperaturantwort steiler, einstellbar und sogar zeitlich reversibel machten.
Von bakteriellen Kill‑Switches zu molekularen Thermostaten
Sobald der Ansatz für ein Protein funktionierte, übertrugen die Autoren ihn auf andere mit sehr unterschiedlichen Aufgaben. Das Einfügen des Sensors in ein Enzym für Antibiotikaresistenz verwandelte dieses in einen wärmeausgelösten Kill‑Switch: Bakterien wuchsen bei 37 °C, starben aber bei 41 °C in Gegenwart des Medikaments. Eine ähnliche Strategie koppelte den Sensor an eine Komponente eines CRISPR‑basierten Genaktivators in Bakterien, sodass die Genexpression durch sanftes Erwärmen hoch‑ oder heruntergeregelt werden konnte. Das Team untersuchte außerdem einen verwandten Trick, bei dem kurze Signalsequenzen durch wärmeinduzierte Bewegungen des Sensorendes verborgen oder freigelegt werden, was temperaturabhängige Proteindegradation in Bakterien und eine mäßige Kontrolle des Proteintransports zwischen Zellkern und Zytoplasma in menschlichen Zellen ermöglicht.
Wärmegesteuerte Steuerung der Genombearbeitung in menschlichen Zellen
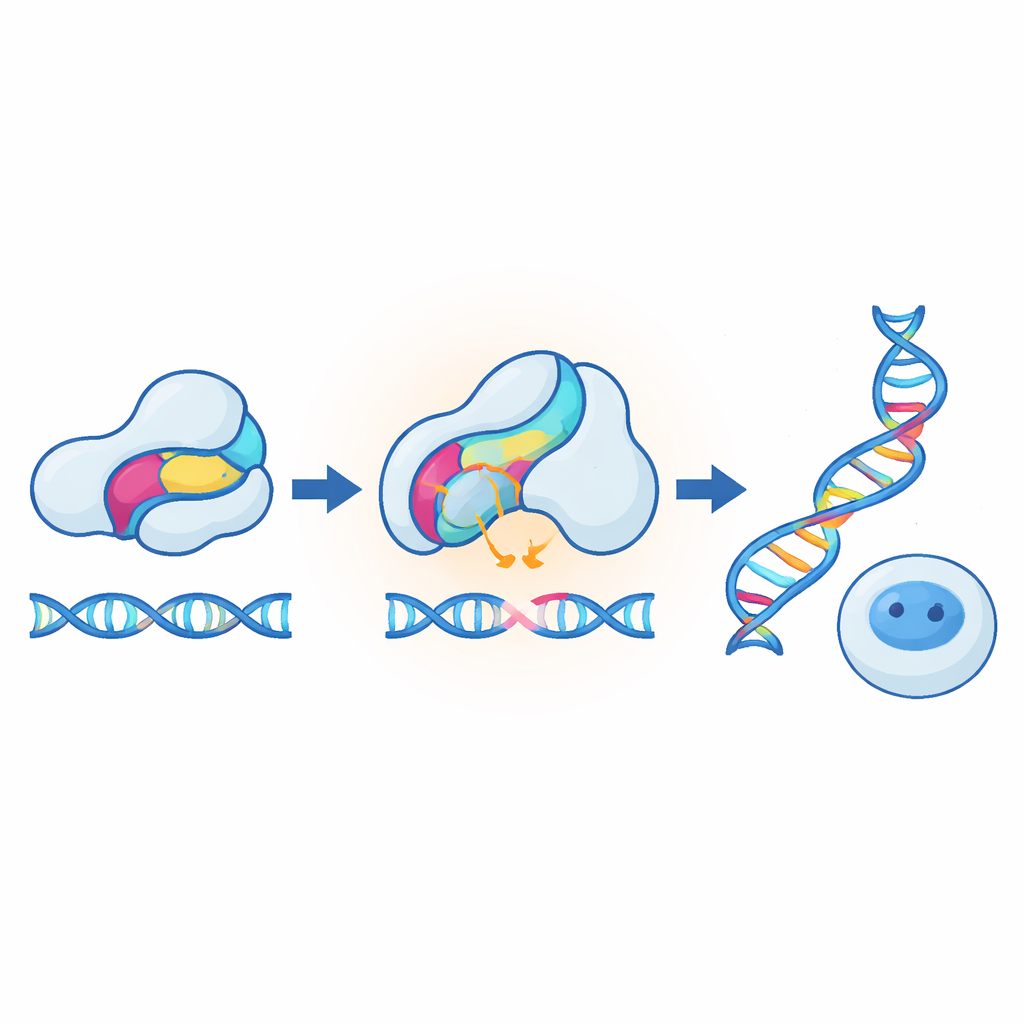
Die eindrucksvollsten Demonstrationen gelangen bei der Anpassung der Methode an CRISPR‑Werkzeuge in Säugerzellen. In einem Design wurde der Sensor in ein Anti‑CRISPR‑Protein eingesetzt, das normalerweise einen Genomeditor blockiert; durch Erwärmen wurde der Inhibitor abgeschwächt, wodurch die Editierung zwischen 37 °C und 40 °C mehrerefach anstieg. In einem anderen Design wurde der Sensor direkt in Cas9 eingebaut, sodass Erwärmung die Editierung statt zu steigern absenkte. Beide Modi funktionierten für mehrere Zielgene, hatten nur geringe Auswirkungen auf die Zellgesundheit und ließen sich auch auf CRISPR‑basierte transkriptionelle Aktivatoren übertragen. Die Forschenden zeigten ferner, dass ein ganz anderes Rezeptormodul—eine Cortisol‑erkennende Domäne aus einem Hormonrezeptor—als alternative temperaturempfindliche Einfügung dienen kann, insbesondere wenn das Hormon vorhanden ist. Das deutet darauf hin, dass viele natürliche Sensordomänen, nicht nur Lichtrezeptoren, instabil werden und schalterartig umschalten können, wenn sie leicht über ihre sonst üblichen Betriebstemperaturen hinaus belastet werden.
Was das für zukünftige Therapien und Werkzeuge bedeutet
Für Laien lautet die Schlussfolgerung, dass die Autoren ein allgemeines Rezept entwickelt haben, um gewöhnliche Proteine in präzise biologische Thermostate zu verwandeln. Durch das Einfügen kleiner Sensordomänen und das Feintuning ihrer Stabilität können sie die Proteinaktivität abrupt bei ausgewählten Temperaturen innerhalb des normalen menschlichen Bereichs ansteigen oder abfallen lassen. Da die Strategie modular ist, sollte sie mit vielen bestehenden optogenetischen und chemogenetischen Ansätzen kompatibel sein und direkt auf der Ebene der Proteinfunktion wirken, nicht nur der Genexpression. Langfristig könnten temperaturresponsive Schalter die Geneditierung sicherer und besser kontrollierbar machen, hitzeführte Bakterien ermöglichen, die außerhalb gewünschter Bedingungen selbstzerstörerisch werden, und Biologen subtile neue Werkzeuge an die Hand geben, um zu untersuchen, wie Zellen auf geringste Wärmeänderungen reagieren.
Zitation: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Schlüsselwörter: Thermogenetik, Protein‑Schalter, CRISPR‑Kontrolle, allosterische Regulation, Temperaturwahrnehmung