Clear Sky Science · ja
熱応答性アロステリックタンパク質のモジュール化設計
熱を穏やかなオン・オフスイッチに変える
たった数度の温度上昇だけで、生細胞内のほぼ任意のタンパク質の活性を制御できると想像してみてください—薬剤も強い光も不要で、ほんのわずかな温度変化だけで済みます。本研究は、そのような熱感受性タンパク質の「スイッチ」をモジュール式に構築する方法を示しています。多くのタンパク質に差し替え可能な部品を用いることで、新しいツールキットが生まれ、将来的には遺伝子治療の誘導、微生物治療の微調整、あるいは細胞の機能探査などが、ほぼ体温付近の狭い温度範囲を利用して行えるようになる可能性があります。
温度が強力な不可視のリモコンである理由
研究者はすでに光や化学物質を使って細胞内のタンパク質をオン・オフしていますが、両者には実用上の制約があります。光は組織深部に浸透しにくく、化学物質は全身に拡散してしまい副作用を及ぼすことがあります。一方で温度は組織に良く浸透し、空間や時間的に非常に精密に焦点を合わせられます。これまでの課題は、既存の熱ツールの多くが極端な温度でしか機能しないか、主に遺伝子発現を介して間接的に制御するにとどまっていたことです。著者らは一般的な戦略を作り、通常のタンパク質に対して37–41 °Cの範囲、すなわち正常体温と軽度の発熱の差に相当する小さな温度変化に鋭く応答するようにすることを目指しました。
小さなセンサーを多くのタンパク質に差し込む
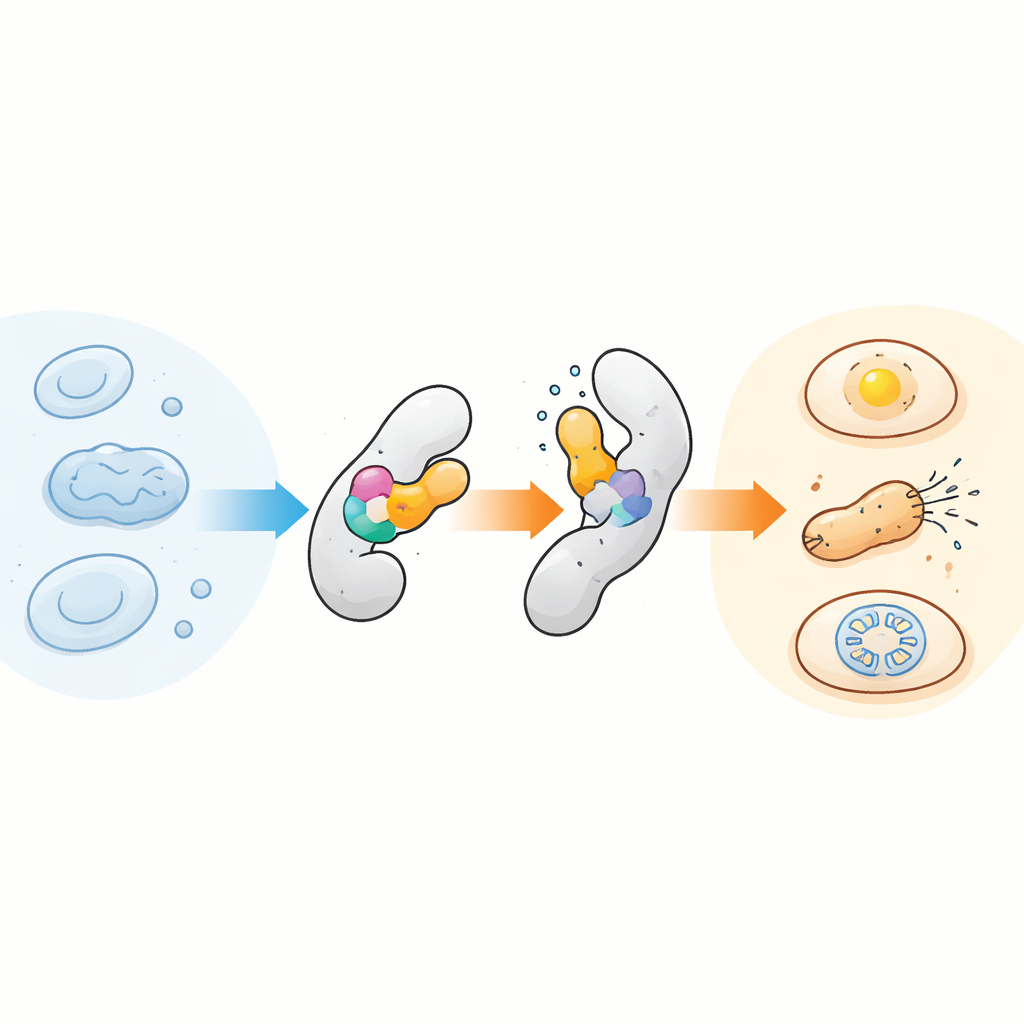
核心は一見すると単純です:小型の温度感受性センサー領域を別のタンパク質に挿入し、センサーがわずかに構造を変えることで宿主タンパク質に伝達され、内部の蝶番のように働かせるのです。研究チームは、もともとオート麦由来の光センサーであるAsLOV2という良く研究されたモジュールに注目しました。AsLOV2は本来形状を切り替える性質があり、特定の変異でわずかに不安定化させると温度に対して驚くほど敏感になることが分かりました。AsLOV2の調整版を標的タンパク質のさまざまな位置に挿入することで、活性がわずか数度で鋭くオンまたはオフに切り替わるキメラタンパク質を作り出しました。細菌での最初の実証では転写因子AraCに適用し、さらにAsLOV2のバリアントを進化的に改良して温度応答の鋭さを増し、調整可能で時間的に可逆的な応答も得られるようにしました。
細菌のキルスイッチから分子サーモスタットへ
この手法が一つのタンパク質で機能することが示されると、著者らは非常に異なる機能を持つ他のタンパク質にも応用しました。抗生物質耐性酵素にセンサーを挿入すると、それは熱トリガー型のキルスイッチになりました:細菌は37 °Cでは増殖しますが、薬剤と組み合わせて41 °Cにすると死にます。同様の戦略で、CRISPRベースの遺伝子活性化因子の構成要素にセンサーを結合させ、穏やかな加熱で遺伝子発現を上下に調整できるようにしました。さらに短いシグナルペプチドをセンサーのテールの熱誘導運動で隠したり露出させたりするトリックも検討し、これにより細菌では温度依存的なタンパク質分解を可能にし、ヒト細胞では核と細胞質間のタンパク質輸送を控えめに制御することができました。
ヒト細胞におけるゲノム編集の熱調整制御
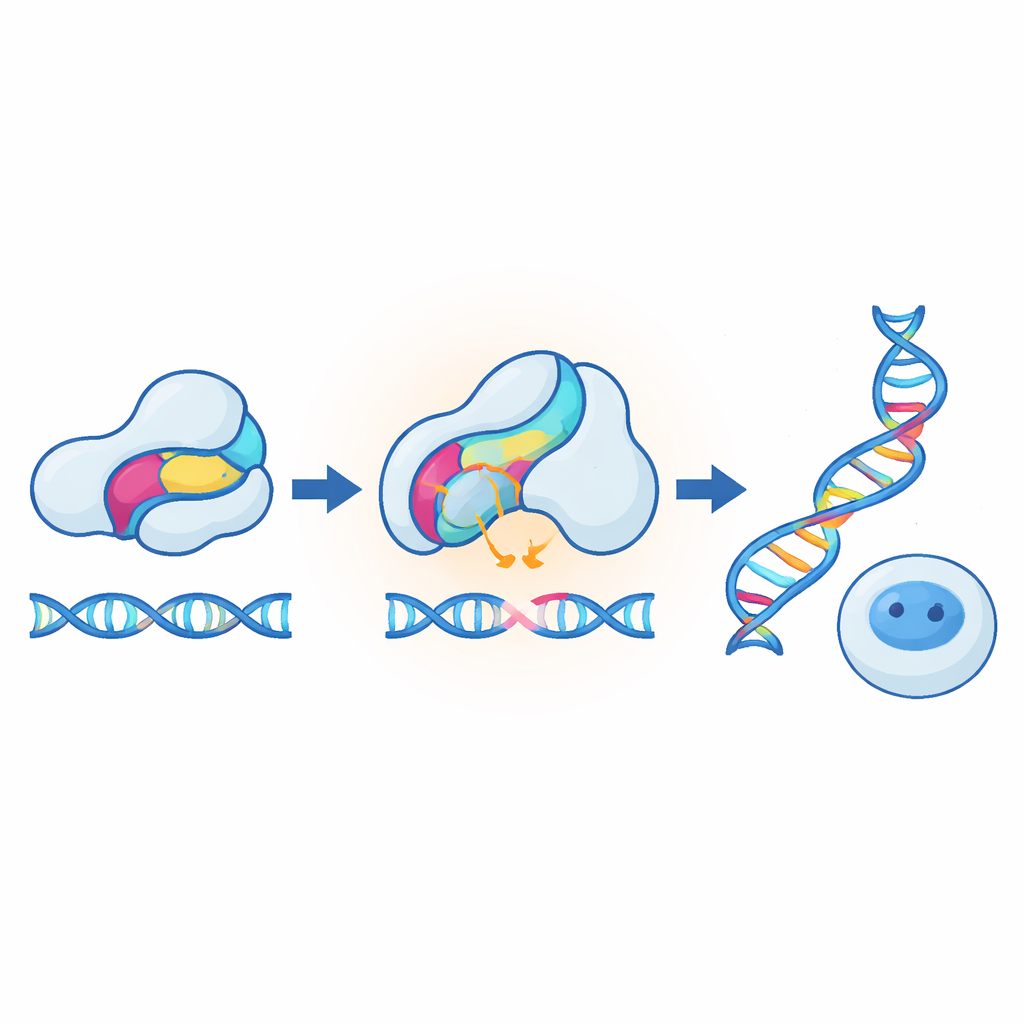
最も印象的な実証は、哺乳類細胞でのCRISPRツールへの適用から得られました。一つの設計では、センサーを通常はゲノムエディターを阻害するアンチCRISPRタンパク質に挿入しました。細胞を温めると阻害因子が弱まり、37 °Cから40 °Cの間で編集効率が数倍に上がりました。別の設計ではセンサーを直接Cas9に組み込み、加熱で編集が低下するようにしました。どちらのモードも複数の標的遺伝子で機能し、細胞の健康にほとんど影響を与えず、CRISPRベースの転写活性化因子にも移植できました。さらに、ホルモン受容体由来のコルチゾール感知ドメインという全く異なる受容モジュールが、ホルモン存在下で特に有効な代替の温度感受性インサートとして働く可能性が示されました。これは、光受容体だけでなく多くの自然のセンサー領域が、その通常の稼働温度をわずかに超えると不安定になりスイッチ状に振る舞うことがあり得ることを示唆します。
将来の療法やツールにとっての意義
一般向けに言えば、著者らは通常のタンパク質を正確な生物学的サーモスタットに変えるための一般的なレシピを構築した、ということです。小さなセンサー領域を挿入しその安定性を微調整することで、タンパク質の活性を人体の通常範囲内の選んだ温度で急激に上げたり下げたりできるようになりました。戦略がモジュール式であるため、多くの既存のオプトジェネティクスやケモジェネティクス設計と互換性があり、遺伝子発現だけでなくタンパク質機能のレベルで直接動作させることができます。長期的には、この種の温度応答性スイッチはゲノム編集をより安全に制御する助けとなり、所望の条件外で自動的に自己破壊する熱誘導菌を可能にし、生物学者がごくわずかな温度変化に対する細胞の応答を微妙に探るための新しい手段を提供する可能性があります。
引用: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
キーワード: サーモジェネティクス, タンパク質スイッチ, CRISPR制御, アロステリック調節, 温度センシング