Clear Sky Science · pl
Modularna inżynieria termoreaktywnych białek allosterycznych
Przekształcanie ciepła w delikatny włącznik
Wyobraź sobie możliwość kontrolowania aktywności niemal dowolnego białka w żywej komórce przez podgrzanie go o kilka stopni — bez leków, bez intensywnego światła, jedynie przez niewielką zmianę temperatury. Badanie prezentuje, jak naukowcy mogą zbudować takie termoczułe „przełączniki” białkowe w sposób modułowy, wykorzystując elementy, które można wstawiać do wielu różnych białek. Efekt to nowy zestaw narzędzi, który w przyszłości może pomagać w precyzowaniu terapii genowych, regulowaniu terapii mikrobiologicznych lub badaniu funkcjonowania komórek, wykorzystując wąski zakres temperatur wokół normalnej temperatury ciała.
Dlaczego temperatura to potężny, niewidzialny pilot
Naukowcy już używają światła i chemikaliów do włączania i wyłączania białek w komórkach, ale oba podejścia mają praktyczne ograniczenia. Światło często słabo przenika tkanki, a substancje chemiczne rozprzestrzeniają się powoli i wpływają na wiele obszarów organizmu jednocześnie. Temperatura natomiast przenika tkanki dobrze i może być precyzyjnie ukierunkowana w czasie i przestrzeni. Problem polegał na tym, że większość istniejących narzędzi termicznych działa tylko w ekstremalnych zakresach temperatur albo kontroluje ekspresję genów pośrednio. Autorzy postawili sobie za cel stworzenie ogólnej strategii, która pozwoliłaby nadać zwykłemu białku wyraźną odpowiedź na niewielkie wahania temperatury w zakresie 37–41 °C — mniej więcej różnicę między normalną temperaturą ciała a łagodną gorączką.
Wtykanie małego czujnika do wielu białek
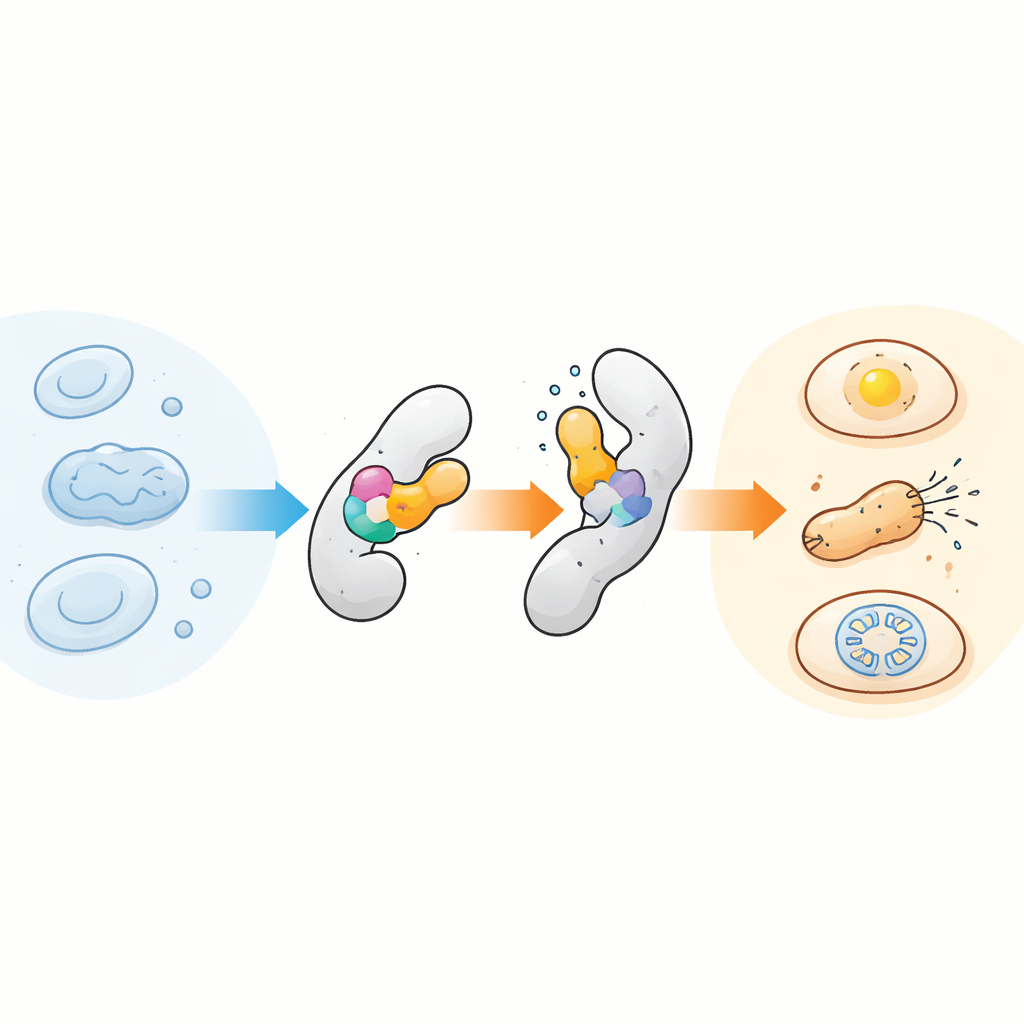
Główna koncepcja jest zwodniczo prosta: wstawić kompaktową, termoczułą domenę sensoryczną do innego białka tak, by niewielka zmiana strukturalna sensora była przekazywana na białko gospodarza, działając jak wewnętrzny zawias. Zespół skupił się na dobrze zbadanym module zwanym AsLOV2, pochodzącym pierwotnie z owsa jako sensor światła, ponieważ naturalnie przechodzi między różnymi kształtami. Odkryli, że domena ta jest również zaskakująco wrażliwa na temperaturę, zwłaszcza gdy zostanie nieco destabilizowana przez konkretne mutacje. Wstawiając dopasowane wersje AsLOV2 w różne pozycje docelowych białek, stworzyli chimeryczne białka, których aktywność gwałtownie przełączała się w ciągu zaledwie kilku stopni. W bakteriach najpierw pokazali to na AraC, czynniku transkrypcyjnym, a następnie ewoluowali warianty AsLOV2, które uczyniły odpowiedź temperaturową bardziej stromą, regulowaną i nawet odwracalną w czasie.
Od bakteryjnych przełączników śmierci do molekularnych termostatów
Gdy podejście zadziałało dla jednego białka, autorzy zastosowali je do innych, pełniących bardzo różne funkcje. Wstawienie sensora do enzymu nadającego oporność na antybiotyk przekształciło go w wyzwalany ciepłem przełącznik śmierci: bakterie rosły w 37 °C, ale ginęły w 41 °C w obecności leku. Podobna strategia dołączyła sensor do składnika aktywatora genów opartego na CRISPR w bakteriach, pozwalając na regulację ekspresji genów przez łagodne podgrzewanie. Zespół badał też pokrewny trik, w którym krótkie peptydy sygnałowe są ukrywane lub odsłaniane przez ruchy ogonka sensora wywołane ciepłem, umożliwiając termozależną degradację białek w bakteriach oraz umiarkowaną kontrolę przemieszczania białek między jądrem a cytoplazmą w komórkach ludzkich.
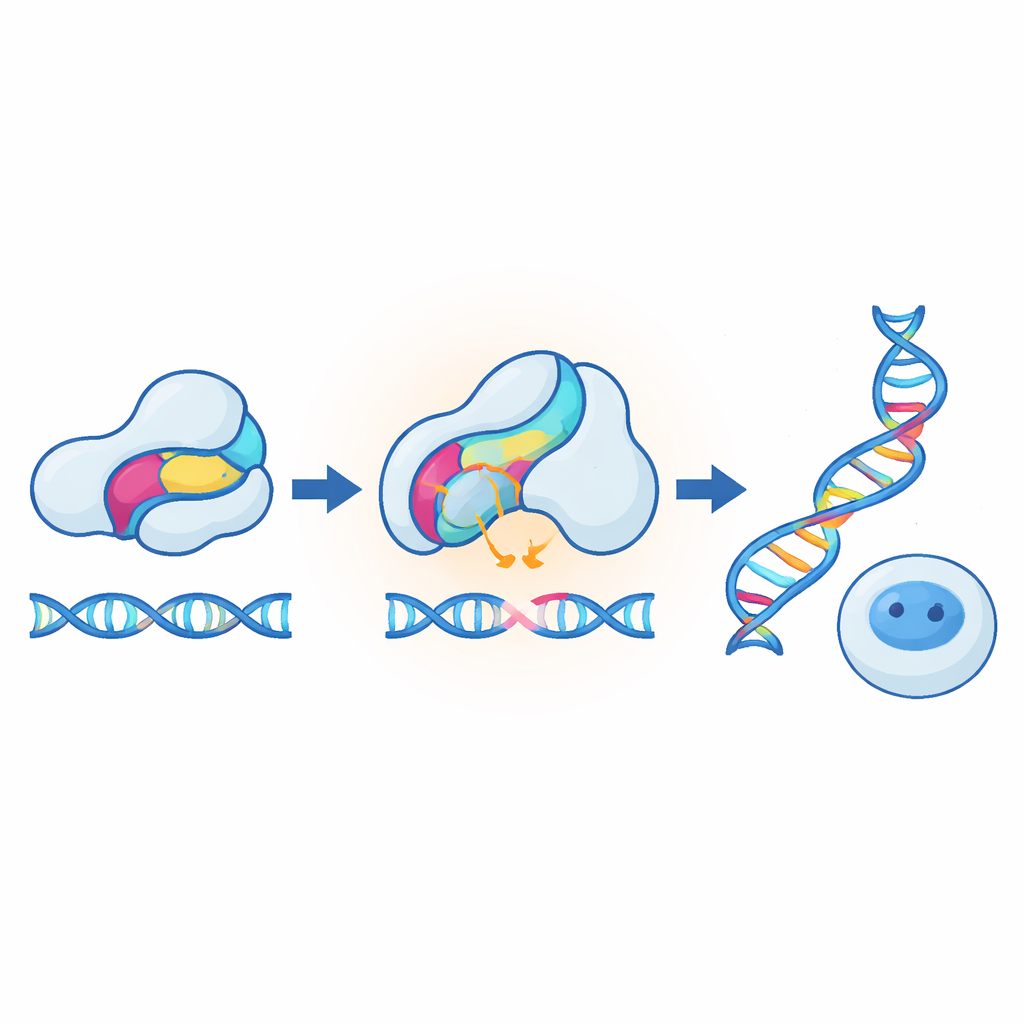
Kontrola edycji genomu w komórkach ludzkich sterowana ciepłem
Najbardziej uderzające demonstracje pochodziły z adaptacji metody do narzędzi CRISPR w komórkach ssaczych. W jednym projekcie sensor został wstawiony do białka anty‑CRISPR, które normalnie blokuje edytor genomu; ogrzewanie komórek osłabiało inhibitor, co pozwalało na wielokrotny wzrost efektywności edycji między 37 °C a 40 °C. W innym rozwiązaniu sensor wbudowano bezpośrednio w Cas9, tak że podgrzewanie redukowało aktywność edycji zamiast ją zwiększać. Oba tryby działały na wielu genach docelowych, przy niewielkim wpływie na zdrowie komórek, i mogły być też przeniesione na oparte na CRISPR aktywatory transkrypcyjne. Badacze wykazali również, że zupełnie inny moduł receptorowy — domena rozpoznająca kortyzol z receptora hormonalnego — może służyć jako alternatywny, termoczuły wkład, szczególnie w obecności hormonu. To sugeruje, że wiele naturalnych domen sensorycznych, nie tylko receptory światła, może stać się niestabilnych i działać jak przełączniki, gdy zostaną nieco podniesione powyżej zwykłych temperatur pracy.
Co to oznacza dla przyszłych terapii i narzędzi
Dla laika wniosek jest taki, że autorzy opracowali ogólny przepis na przekształcenie zwykłych białek w precyzyjne biologiczne termostaty. Poprzez wstawianie małych domen sensorycznych i dopracowywanie ich stabilności mogą sprawić, że aktywność białka gwałtownie wzrośnie lub spadnie w wybranych temperaturach mieszczących się w normalnym zakresie ludzkim. Ponieważ strategia jest modułowa, powinna być zgodna z wieloma istniejącymi projektami optogenetycznymi i chemogenetycznymi oraz działać bezpośrednio na poziomie funkcji białka, a nie tylko ekspresji genów. W dłuższej perspektywie takie termoreaktywne przełączniki mogłyby zwiększyć bezpieczeństwo i kontrolę edycji genów, umożliwić bakteriom sterowanym ciepłem samozniszczenie poza pożądanymi warunkami i dać biologom subtelne nowe narzędzia do badania, jak komórki reagują na najmniejsze zmiany ciepła.
Cytowanie: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Słowa kluczowe: termogenetyka, przełączniki białkowe, kontrola CRISPR, regulacja allosteryczna, czucie temperatury