Clear Sky Science · sv
Modulär ingenjörskonst av termoresponsiva allosteriska proteiner
Att förvandla värme till en mild av‑/på‑knapp
Föreställ dig att kunna styra aktiviteten hos nästan vilket protein som helst i en levande cell genom att helt enkelt värma upp det några grader—inga läkemedel, inget starkt ljus, bara en liten temperaturförändring. Denna studie visar hur forskare kan bygga sådana värmekänsliga protein"switchar" på ett modulärt sätt, med delar som kan kopplas in i många olika proteiner. Resultatet är ett nytt verktygspaket som en dag kan hjälpa till att styra genterapier, finjustera mikrobiella behandlingar eller utforska hur celler fungerar, allt genom att utnyttja det snäva temperaturområdet kring normal kroppsvärme.
Varför temperatur är en kraftfull osynlig fjärrkontroll
Forskare använder redan ljus och kemikalier för att slå på och av proteiner i celler, men båda metoderna har praktiska nackdelar. Ljus tränger ofta inte djupt in i vävnad, och kemikalier kan spridas långsamt och påverka många delar av kroppen samtidigt. Temperatur, däremot, tränger väl igenom vävnader och kan riktas mycket exakt i både rumsligt och tidsmässigt avseende. Utmaningen har varit att de flesta befintliga termiska verktyg antingen fungerar endast vid extrema temperaturer eller främst kontrollerar genuttryck indirekt. Författarna satte upp målet att skapa en generell strategi som skulle låta dem ta ett vanligt protein och ge det ett skarpt svar på små temperaturskift i intervallet 37–41 °C—ungefär skillnaden mellan normal kroppstemperatur och en lindrig feber.
Att koppla in en liten sensor i många proteiner
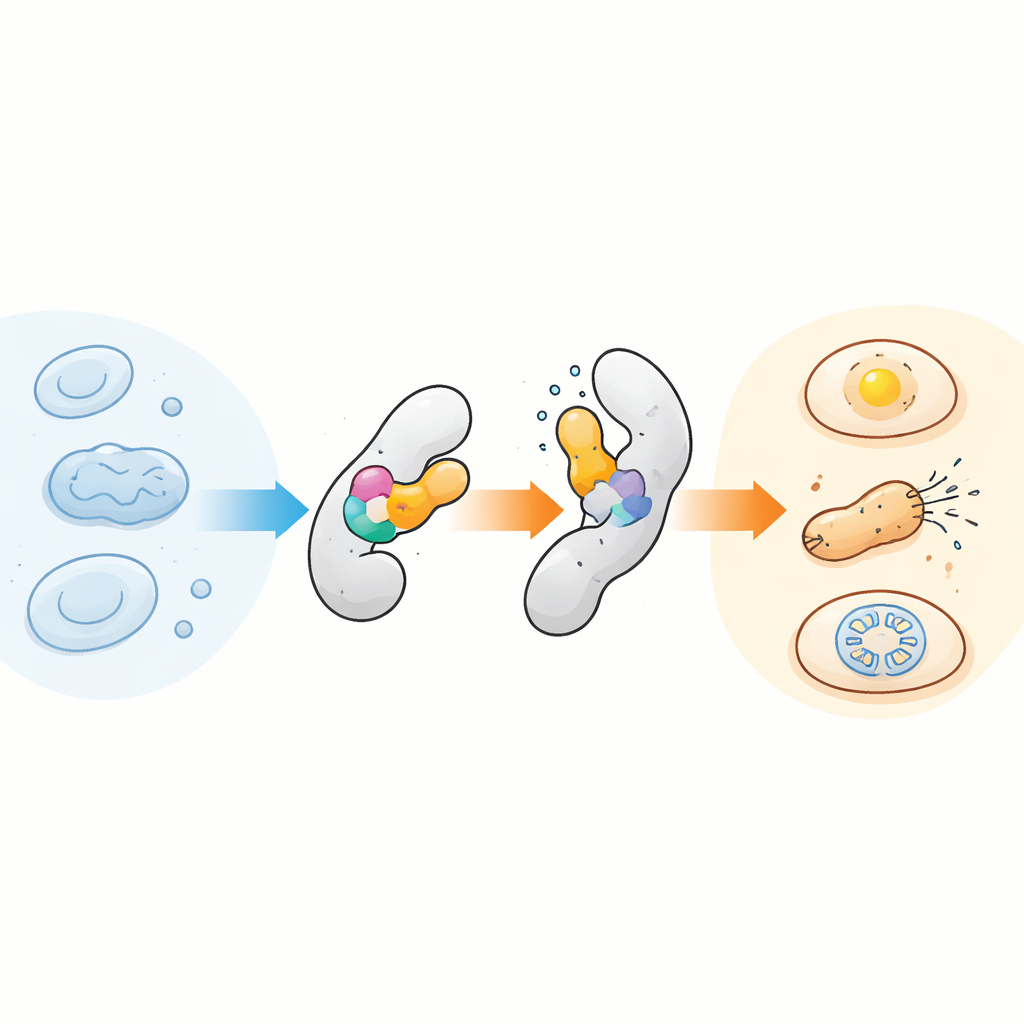
Huvudidén är bedrägligt enkel: sätt in en kompakt temperatursensitiv sensordomän i ett annat protein så att en liten strukturell förändring i sensorn överförs till värdproteinet och fungerar som ett internt gångjärn. Teamet fokuserade på en välstuderad modul kallad AsLOV2, ursprungligen en ljussensor från havre, eftersom den naturligt växlar mellan olika former. De upptäckte att denna domän också är överraskande temperaturkänslig, särskilt när den lätt destabiliseras av specifika mutationer. Genom att infoga skräddarsydda versioner av AsLOV2 i olika positioner i målenzymer skapade de kimeriska proteiner vars aktivitet skiftade skarpt av och på över bara några grader. I bakterier visade de detta först med AraC, en transkriptionsfaktor, och utvecklade sedan AsLOV2‑varianter som gjorde temperaturresponsen brantare, justerbar och till och med reversibel över tid.
Från bakterie‑dödsknappar till molekylära termostater
När metoden fungerade för ett protein applicerade författarna den på andra proteiner med mycket olika funktioner. Att infoga sensorn i ett enzym som ger antibiotikaresistens förvandlade det till en värmetriggerad dödsknapp: bakterier växte vid 37 °C men dog vid 41 °C när de utsattes för drogen. En liknande strategi fäste sensorn vid en komponent i en CRISPR‑baserad genaktivator i bakterier, vilket gjorde att genuttryck kunde steglas upp eller ner med mild uppvärmning. Gruppen utforskade också ett närbesläktat knep där korta signalpeptider döljs eller blottas genom värmeinducerade rörelser i sensorns svans, vilket möjliggör temperaturberoende proteinnedbrytning i bakterier och måttlig kontroll över proteintrafik mellan kärna och cytoplasma i humana celler.
Värmestyrd kontroll av genredigering i humana celler
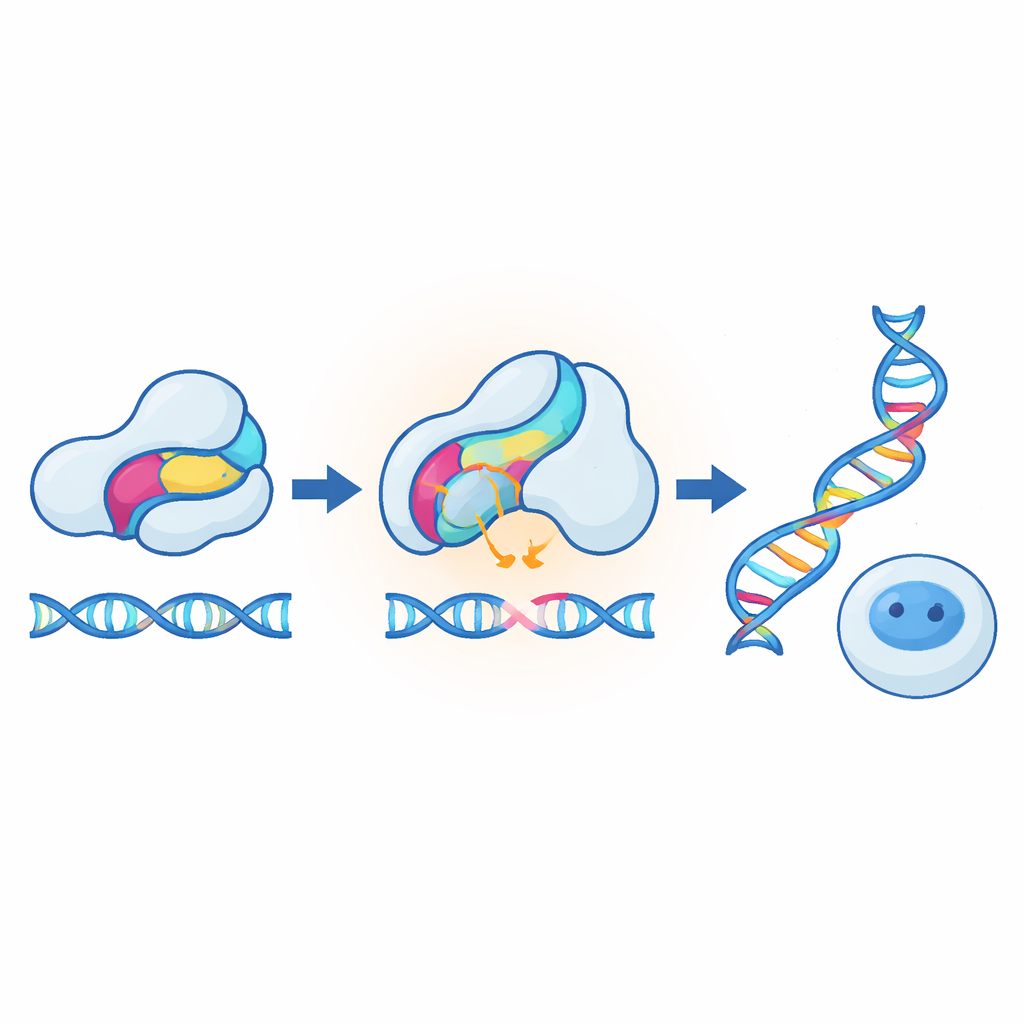
De mest påfallande demonstrationerna kom från att anpassa metoden till CRISPR‑verktyg i däggdjursceller. I en konstruktion infogades sensorn i ett anti‑CRISPR‑protein som normalt blockerar en genredigerare; uppvärmning försvagade inhibitorn och lät redigeringen öka flera gånger mellan 37 °C och 40 °C. I en annan konstruktion byggdes sensorn direkt in i Cas9, så att uppvärmning istället minskade redigeringsaktiviteten. Båda lägena fungerade på flera målgener, med liten inverkan på cellhälsa, och kunde också överföras till CRISPR‑baserade transkriptionsaktivatorer. Forskarna visade dessutom att en helt annan receptormodul—en kortisolkänslig domän från en hormonreceptor—kunde fungera som ett alternativt temperatursensitivt insättningsstycke, särskilt när hormonet var närvarande. Detta tyder på att många naturliga sensordomäner, inte bara ljusreceptorer, kan bli instabila och knapp‑lika när de pressas något över sina vanliga arbetstemperaturer.
Vad detta innebär för framtida terapier och verktyg
För lekmannen är slutsatsen att författarna har byggt ett generellt recept för att förvandla vanliga proteiner till precisa biologiska termostater. Genom att infoga små sensordomäner och finjustera deras stabilitet kan de få proteinaktivitet att stiga eller falla abrupt vid valda temperaturer inom det normala mänskliga intervallet. Eftersom strategin är modulär bör den vara kompatibel med många befintliga optogenetiska och kemogenetiska konstruktioner, och den kan verka direkt på proteinnivå snarare än bara på genuttryck. I längden skulle sådana temperaturresponsiva switchar kunna göra genredigering säkrare och mer kontrollerbar, möjliggöra värmestyrda bakterier som självdestruerar utanför önskade förhållanden, och ge biologer subtila nya sätt att undersöka hur celler svarar på den minsta förändring i värme.
Citering: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Nyckelord: termogenetik, proteinswitchar, CRISPR‑kontroll, allosterisk reglering, temperaturkänslighet