Clear Sky Science · fr
Ingénierie modulaire de protéines allostériques thermoréactives
Transformer la chaleur en un interrupteur marche–arrêt doux
Imaginez pouvoir contrôler l’activité de presque n’importe quelle protéine dans une cellule vivante simplement en l’échauffant de quelques degrés — sans médicaments, sans lumière intense, juste un petit changement de température. Cette étude montre comment des chercheurs peuvent construire de tels « interrupteurs » protéiques sensibles à la chaleur de manière modulaire, en utilisant des éléments qui peuvent être insérés dans de nombreuses protéines différentes. Le résultat est une nouvelle boîte à outils qui pourrait un jour aider à guider des thérapies géniques, à affiner des traitements microbiaux ou à explorer le fonctionnement des cellules, en exploitant la plage de température étroite autour de la chaleur corporelle normale.
Pourquoi la température est une télécommande invisible puissante
Les scientifiques utilisent déjà la lumière et des produits chimiques pour activer ou désactiver des protéines à l’intérieur des cellules, mais ces approches présentent des inconvénients pratiques. La lumière ne pénètre souvent pas profondément dans les tissus et les produits chimiques peuvent se diffuser lentement et affecter de nombreuses parties du corps à la fois. La température, en revanche, pénètre bien les tissus et peut être focalisée très précisément dans l’espace et le temps. Le défi a été que la plupart des outils thermiques existants fonctionnent soit seulement à des températures extrêmes, soit contrôlent surtout l’expression génique de façon indirecte. Les auteurs ont cherché à créer une stratégie générale permettant de prendre une protéine ordinaire et de lui donner une réponse nette à de petits changements de température dans la plage de 37–41 °C — à peu près la différence entre la température corporelle normale et une légère fièvre.
Brancher un petit capteur dans de nombreuses protéines
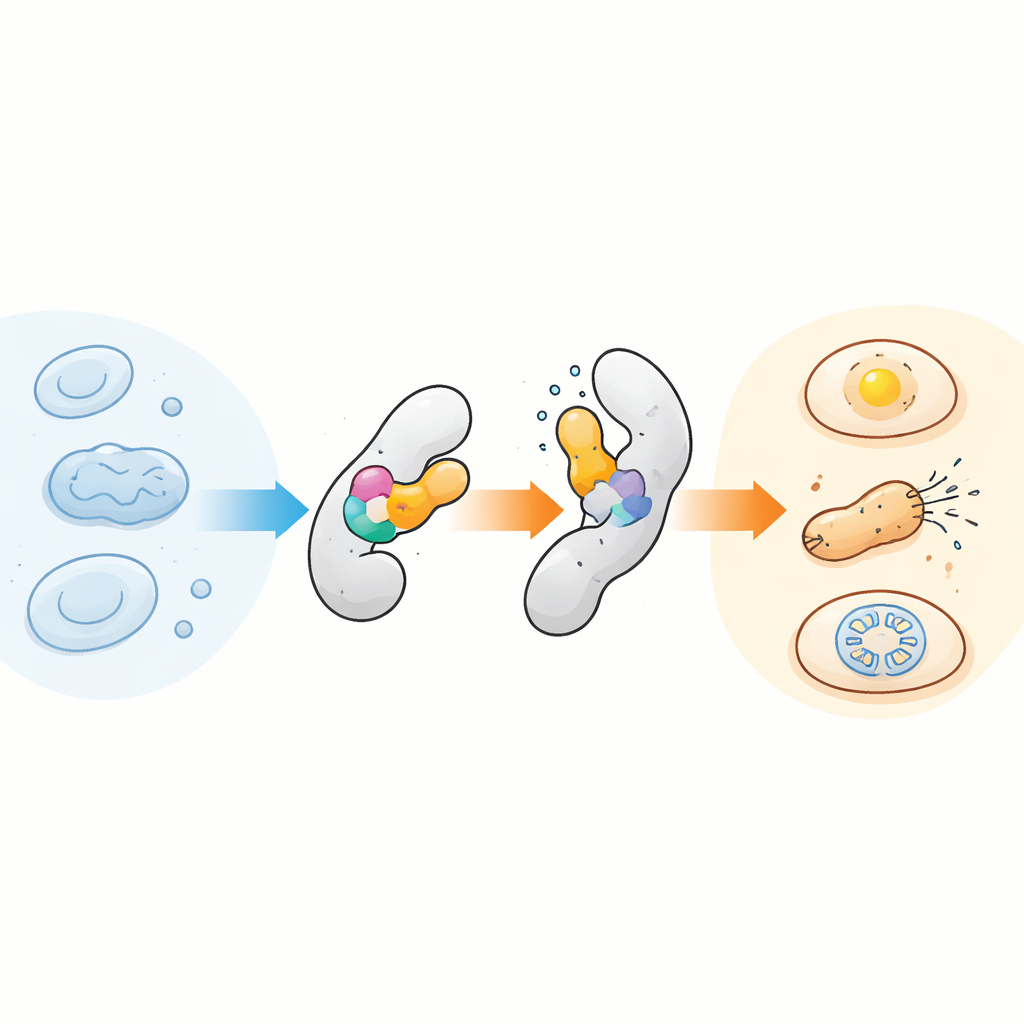
L’idée centrale est d’une simplicité trompeuse : insérer un petit domaine capteur sensible à la température dans une autre protéine de sorte qu’un petit changement structural du capteur soit transmis à la protéine hôte, agissant comme une charnière interne. L’équipe s’est concentrée sur un module bien étudié appelé AsLOV2, à l’origine un capteur de lumière provenant d’avoine, parce qu’il bascule naturellement entre différentes conformations. Ils ont découvert que ce domaine est aussi étonnamment sensible à la température, surtout lorsqu’il est légèrement déstabilisé par des mutations spécifiques. En insérant des versions adaptées d’AsLOV2 à différentes positions des protéines cibles, ils ont créé des protéines chimériques dont l’activité s’allumait ou s’éteignait nettement sur seulement quelques degrés. Chez les bactéries, ils ont d’abord montré cela avec AraC, un facteur de transcription, puis ont fait évoluer des variantes d’AsLOV2 qui rendaient la réponse thermique plus abrupte, modulable et même réversible dans le temps.
Des interrupteurs létaux bactériens aux thermostats moléculaires
Une fois l’approche validée pour une protéine, les auteurs l’ont appliquée à d’autres protéines ayant des fonctions très différentes. L’insertion du capteur dans une enzyme de résistance aux antibiotiques l’a transformée en interrupteur létal déclenché par la chaleur : les bactéries croissaient à 37 °C mais mouraient à 41 °C en présence de l’antibiotique. Une stratégie similaire a attaché le capteur à un composant d’un activateur génique basé sur CRISPR chez les bactéries, permettant de faire varier l’expression génique par un léger chauffage. L’équipe a aussi exploré un artifice connexe dans lequel de courts peptides de signalisation sont masqués ou exposés par des mouvements induits par la chaleur de la queue du capteur, permettant une dégradation protéique dépendante de la température chez les bactéries et un contrôle modeste du trafic protéique entre le noyau et le cytoplasme dans des cellules humaines.
Contrôle thermique de l’édition du génome dans des cellules humaines
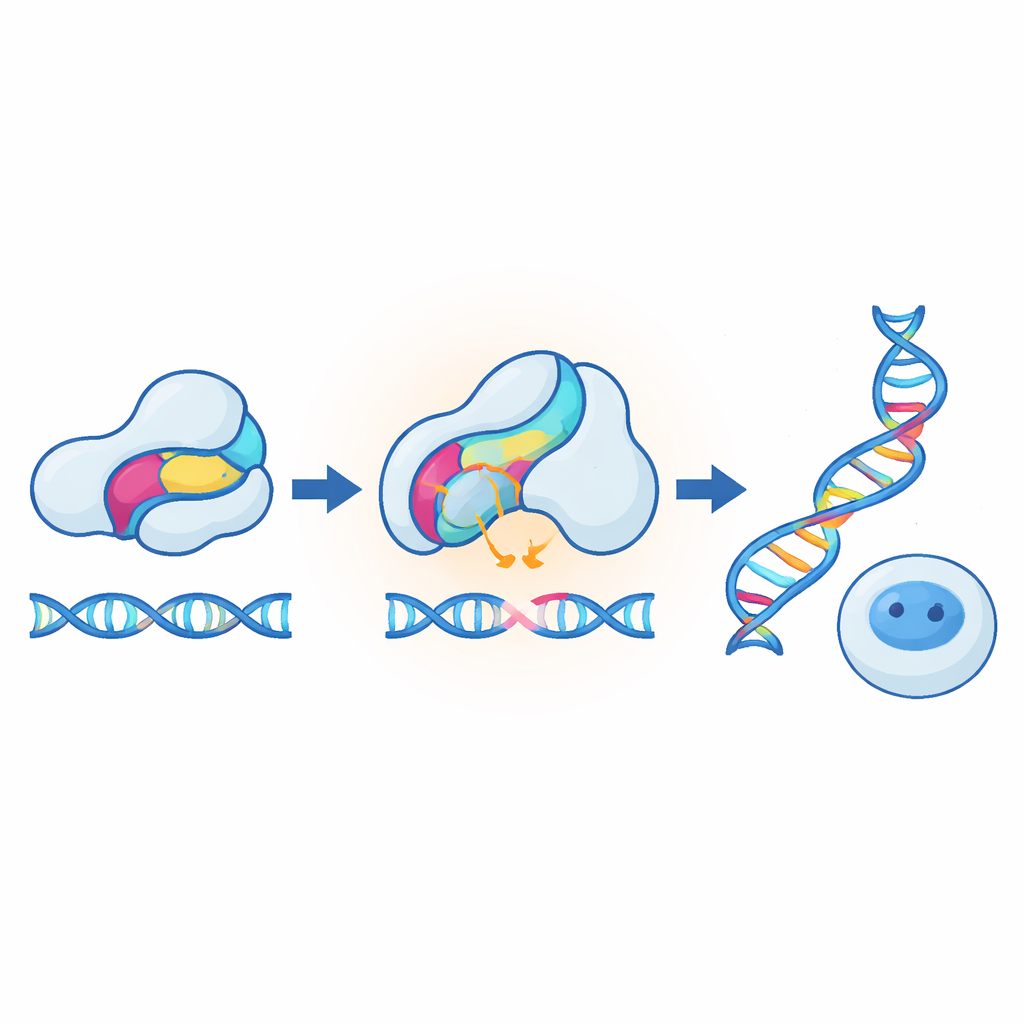
Les démonstrations les plus frappantes proviennent de l’adaptation de la méthode aux outils CRISPR dans des cellules de mammifères. Dans une conception, le capteur a été inséré dans une protéine anti‑CRISPR qui bloque normalement un éditeur du génome ; en chauffant les cellules, l’inhibiteur s’affaiblissait, permettant à l’édition d’augmenter de plusieurs fois entre 37 °C et 40 °C. Dans une autre conception, le capteur a été intégré directement dans Cas9 lui‑même, de sorte que le chauffage réduisait l’édition plutôt que de l’augmenter. Les deux modes ont fonctionné sur plusieurs gènes cibles, avec peu d’impact sur la santé cellulaire, et ont aussi pu être transférés à des activateurs transcriptionnels basés sur CRISPR. Les chercheurs ont ensuite montré qu’un module récepteur complètement différent — un domaine sensible au cortisol provenant d’un récepteur hormonal — pouvait servir d’insert thermosensible alternatif, surtout en présence de l’hormone. Cela suggère que de nombreux domaines capteurs naturels, pas seulement les récepteurs de lumière, peuvent devenir instables et fonctionner comme des interrupteurs lorsqu’ils sont poussés légèrement au‑dessus de leurs températures de fonctionnement habituelles.
Ce que cela signifie pour les thérapies et outils futurs
Pour un non‑spécialiste, l’essentiel est que les auteurs ont établi une recette générale pour transformer des protéines ordinaires en thermostats biologiques précis. En insérant de petits domaines capteurs et en ajustant finement leur stabilité, ils peuvent faire varier l’activité protéique de façon abrupte à des températures choisies dans la plage humaine normale. Parce que la stratégie est modulaire, elle devrait être compatible avec de nombreux dispositifs optogénétiques et chimiogénétiques existants, et elle peut agir directement au niveau de la fonction protéique plutôt que seulement sur l’expression génétique. À long terme, de tels interrupteurs sensibles à la température pourraient contribuer à rendre l’édition génomique plus sûre et plus contrôlable, permettre des bactéries guidées par la chaleur qui s’autodétruisent hors des conditions souhaitées, et offrir aux biologistes de nouvelles façons subtiles d’étudier comment les cellules répondent au moindre changement de chaleur.
Citation: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Mots-clés: thermogénétique, interrupteurs protéiques, contrôle CRISPR, régulation allostérique, détection de température