Clear Sky Science · ru
Модульная разработка термореспонсивных аллостерических белков
Превращая тепло в мягкий выключатель «вкл–выкл»
Представьте, что можно управлять активностью почти любого белка в живой клетке, просто слегка её подогрев на пару градусов — без лекарств и сильного света, лишь небольшое изменение температуры. В этом исследовании показано, как учёные могут модульно собирать такие термочувствительные белковые «переключатели», используя части, которые можно встраивать в разные белки. В результате получился новый набор приёмов, который однажды может помочь направлять генотерапию, тонко настраивать микробные терапии или исследовать клеточные процессы, используя узкий температурный диапазон вокруг нормальной температуры тела.
Почему температура — мощный невидимый пульт
Учёные уже используют свет и химические вещества, чтобы включать и выключать белки внутри клеток, но у этих подходов есть практические ограничения. Свет часто плохо проникает в ткани, а химические вещества распространяются медленно и затрагивают многие участки организма одновременно. Температура, напротив, хорошо проникает в ткани и может быть точно сфокусирована по пространству и времени. Проблема в том, что большинство существующих тепловых инструментов либо работают только при экстремальных температурах, либо в основном управляют экспрессией генов опосредованно. Авторы поставили цель создать общий метод, который позволил бы взять обычный белок и придать ему резкую реакцию на небольшие температурные колебания в диапазоне 37–41 °C — примерно разницу между нормальной температурой тела и лёгкой лихорадкой.
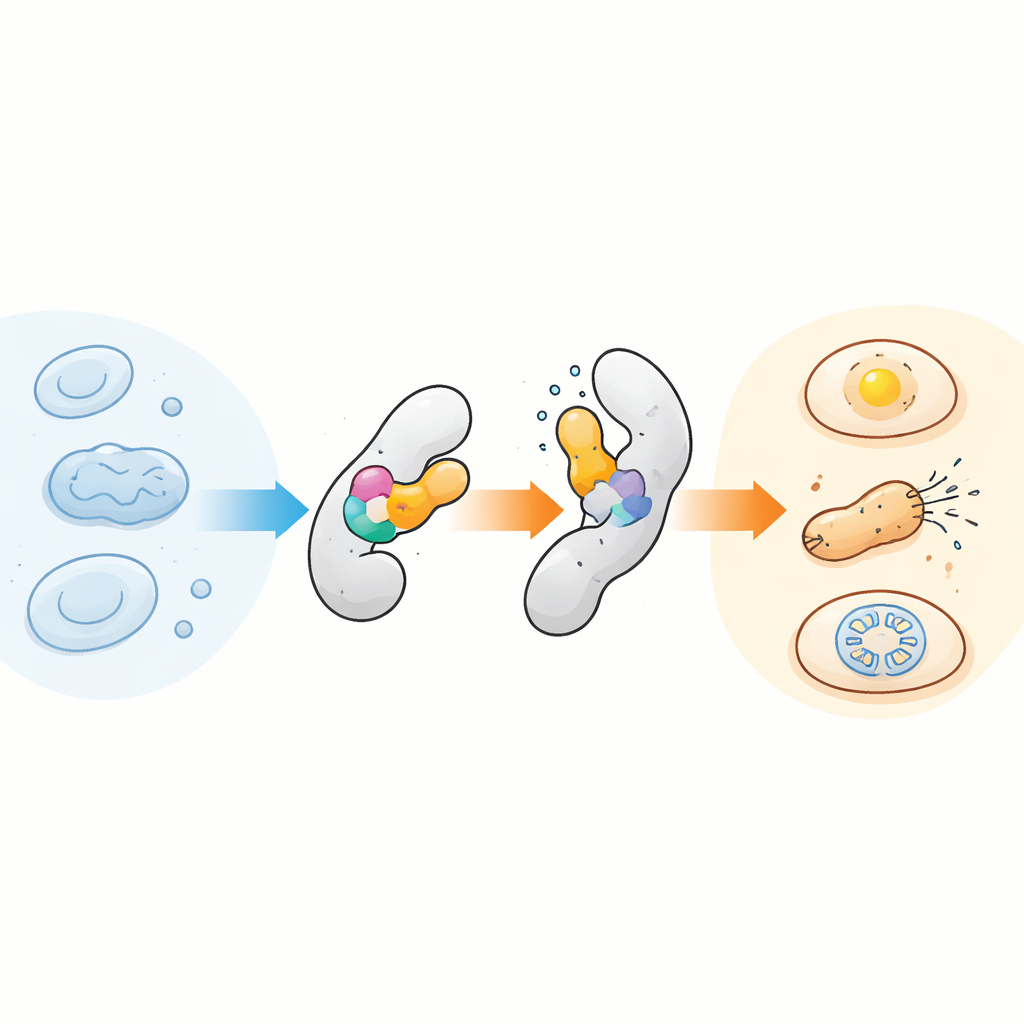
Встраивание крошечного датчика в разные белки
Ключевая идея выглядит обманчиво просто: вставить компактный термочувствительный сенсорный домен в другой белок так, чтобы небольшое структурное изменение датчика передавалось на «хозяина», действуя как внутренний шарнир. Команда сосредоточилась на хорошо изученном модуле AsLOV2, изначально светочувствительном домене у овса, потому что он естественно переключается между формами. Исследователи обнаружили, что этот домен также удивительно чувствителен к температуре, особенно если его слегка дестабилизировать с помощью определённых мутаций. Вставляя специально настроенные варианты AsLOV2 в разные позиции целевых белков, они создали химерные белки, активность которых резко включалась или выключалась всего за несколько градусов. В бактериях это сначала продемонстрировали на AraC — факторе транскрипции, а затем эволюционировали варианты AsLOV2, делающие температурную реакцию круче, настраиваемой и даже обратимой во времени.
От «убийственных» выключателей в бактериях до молекулярных термостатов
Когда подход сработал для одного белка, авторы применили его к другим с совершенно разными функциями. Вставка датчика в фермент, обеспечивающий устойчивость к антибиотикам, превратила его в термозависимый «убийственный» выключатель: бактерии росли при 37 °C, но погибали при 41 °C в присутствии препарата. Похожая стратегия прикрепила датчик к компоненту на базе CRISPR, отвечающему за активацию генов в бактериях, что позволило повышать или понижать экспрессию генов с помощью лёгкого нагрева. Команда также исследовала смежный приём, при котором короткие сигнальные пептиды прячутся или открываются за счёт тепловых движений хвоста датчика, обеспечивая температурно-зависимое разрушение белков в бактериях и умеренный контроль трафика белков между ядром и цитоплазмой в клетках человека.
Терморегулируемое управление редактированием генома в клетках человека
Наиболее впечатляющие примеры получились при адаптации метода к CRISPR-инструментам в млекопитающих. В одном варианте датчик вставляли в анти‑CRISPR белок, который обычно блокирует редактор генома; нагревание клеток ослабляло ингибитор, позволяя редактированию увеличиться в несколько раз между 37 °C и 40 °C. В другом варианте сам Cas9 содержал встроенный датчик, так что нагрев уменьшал активность редактирования, а не усиливал её. Оба режима сработали для нескольких целевых генов с минимальным влиянием на здоровье клеток и могли быть перенесены на CRISPR‑основанные транскрипционные активаторы. Исследователи также показали, что совершенно другой рецепторный модуль — домен, чувствительный к кортизолу из гормонального рецептора — может служить альтернативной термочувствительной вставкой, особенно при наличии гормона. Это указывает на то, что многие природные сенсорные домены, а не только светочувствительные рецепторы, могут становиться нестабильными и вести себя как переключатели при небольшом превышении их обычной рабочей температуры.
Что это значит для будущих терапий и инструментов
Для неспециалиста вывод прост: авторы создали общий рецепт превращения обычных белков в точные биологические термостаты. Вставляя маленькие сенсорные домены и тонко настраивая их стабильность, они могут сделать активность белка резко возрастающей или падающей при выбранных температурах в пределах нормального человеческого диапазона. Поскольку стратегия модульна, она должна быть совместима со многими существующими оптогенетическими и хемогенетическими дизайнами и может работать непосредственно на уровне функции белка, а не только на уровне экспрессии генов. В перспективе такие температурно‑чувствительные переключатели могут сделать редактирование генов безопаснее и управляемее, позволить создавать бактерии, которые самоуничтожаются вне заданных условий, и дать биологам тонкие новые инструменты для изучения реакции клеток на малейшее изменение температуры.
Цитирование: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Ключевые слова: термогенетика, белковые переключатели, управление CRISPR, аллостерическая регуляция, датчики температуры