Clear Sky Science · nl
Modulaire engineering van thermoresponsieve allosterische eiwitten
Warmte als een subtiele aan‑/uit‑schakelaar
Stel je voor dat je de activiteit van vrijwel elk eiwit in een levende cel kunt regelen door het slechts een paar graden te verwarmen—geen geneesmiddelen, geen fel licht, alleen een kleine temperatuurverandering. Deze studie toont hoe onderzoekers dergelijke warmtegevoelige eiwit"schakelaars" modulair kunnen bouwen, met onderdelen die in veel verschillende eiwitten kunnen worden ingebouwd. Het resultaat is een nieuwe gereedschapsset die op termijn gen‑therapieën zou kunnen sturen, microbieële behandelingen nauwkerig afstemmen of helpen begrijpen hoe cellen werken—allemaal door gebruik te maken van het smalle temperatuurbereik rond de normale lichaamstemperatuur.
Waarom temperatuur een krachtig onzichtbaar afstandsbedieningsmiddel is
Wetenschappers gebruiken al licht en chemicaliën om eiwitten in cellen aan of uit te zetten, maar beide benaderingen hebben praktische nadelen. Licht dringt vaak niet diep door weefsels en chemicaliën verspreiden zich langzaam en beïnvloeden veel delen van het lichaam tegelijk. Temperatuur daarentegen dringt goed door weefsels en kan zeer precies in ruimte en tijd worden gericht. De uitdaging was dat de meeste bestaande thermische hulpmiddelen ofwel alleen bij extreme temperaturen werken of vooral indirect genexpressie regelen. De auteurs wilden een algemene strategie ontwikkelen waarmee ze een gewoon eiwit een scherpe respons op kleine temperatuurverschuivingen in het bereik van 37–41 °C konden geven—ongeveer het verschil tussen normale lichaamstemperatuur en een milde koorts.
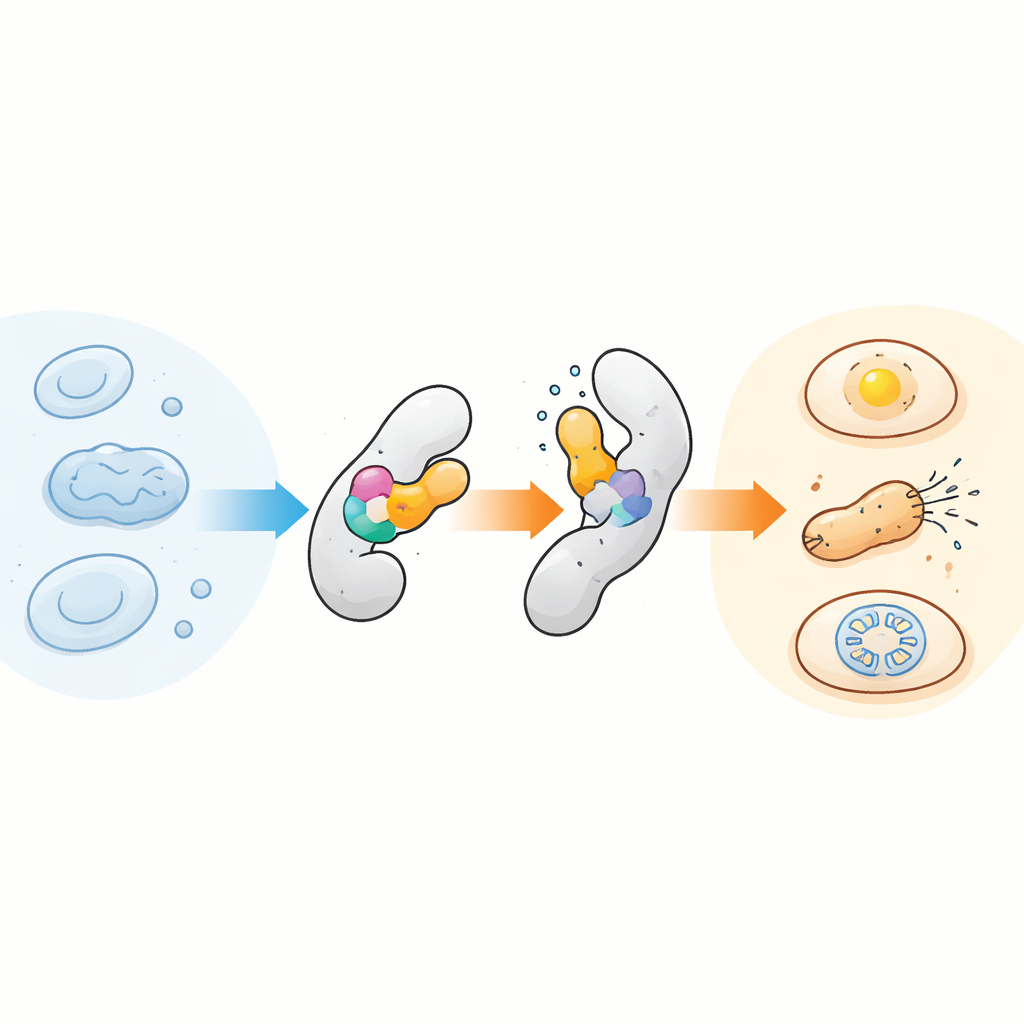
Een klein sensorje in veel eiwitten pluggen
Het kernidee is bedrieglijk eenvoudig: plaats een compact temperatuursensitief senschappje in een ander eiwit zodat een kleine structurele verandering in de sensor wordt doorgegeven aan het gast‑eiwit, als een interne scharnier. Het team richtte zich op een goed bestudeerde module genaamd AsLOV2, oorspronkelijk een lichtsensor uit haver, omdat deze module van vorm verandert. Ze ontdekten dat dit domein ook verrassend gevoelig is voor temperatuur, vooral wanneer het licht gedestabiliseerd wordt door specifieke mutaties. Door aangepaste versies van AsLOV2 op verschillende posities in doelproteïnen in te voegen, creëerden ze chimere eiwitten waarvan de activiteit abrupt aan of uit schakelde over slechts een paar graden. In bacteriën toonden ze dit eerst met AraC, een transcriptiefactor, en evolueerden daarna AsLOV2‑varianten die de temperatuursrespons steiler, verstelbaar en zelfs omkeerbaar over de tijd maakten.
Van bacteriële kill‑switches tot moleculaire thermostaten
Zodra de aanpak voor één eiwit werkte, pasten de auteurs die toe op andere eiwitten met heel verschillende functies. Het invoegen van de sensor in een enzym dat antibioticumresistentie verleent veranderde het in een warmtetriggered kill‑switch: bacteriën groeiden bij 37 °C maar stierven bij 41 °C wanneer het geneesmiddel aanwezig was. Een vergelijkbare strategie koppelde de sensor aan een component van een CRISPR‑gebaseerde genactivator in bacteriën, waardoor genexpressie omhoog of omlaag kon worden bij zachte verhitting. Het team onderzocht ook een gerelateerde truc waarbij korte signaalpeptiden door warmtegerelateerde bewegingen van de sensorstaart worden verborgen of blootgelegd, waardoor temperatuurafhankelijke eiwitafbraak in bacteriën mogelijk werd en bescheiden controle van eiwitverkeer tussen kern en cytoplasma in humane cellen.
Warmtegestuurde controle van genbewerking in menselijke cellen
De meest opvallende demonstraties kwamen van het aanpassen van de methode aan CRISPR‑middelen in zoogdiercellen. In één ontwerp werd de sensor ingebouwd in een anti‑CRISPR‑eiwit dat normaal gesproken een genbewerker blokkeert; verwarming van de cellen verzwakte de remmer, waardoor de bewerking meerdere keren toenam tussen 37 °C en 40 °C. In een ander ontwerp werd de sensor direct in Cas9 ingebouwd, zodat verwarming de bewerking juist uitschakelde in plaats van inschakelde. Beide benaderingen werkten op meerdere doelgenen, met weinig effect op de gezondheid van de cellen, en konden ook worden toegepast op CRISPR‑gebaseerde transcriptionele activatoren. De onderzoekers lieten verder zien dat een geheel andere receptormodule—een cortisol‑sensing domein uit een hormoonreceptor—als alternatief temperatuurgevoelig inzetstuk kon dienen, vooral wanneer het hormoon aanwezig was. Dit suggereert dat veel natuurlijke sensordomeinen, niet alleen lichtreceptoren, instabiel kunnen worden en schakelachtig kunnen reageren wanneer ze iets boven hun gebruikelijke bedrijfstemperaturen worden geduwd.
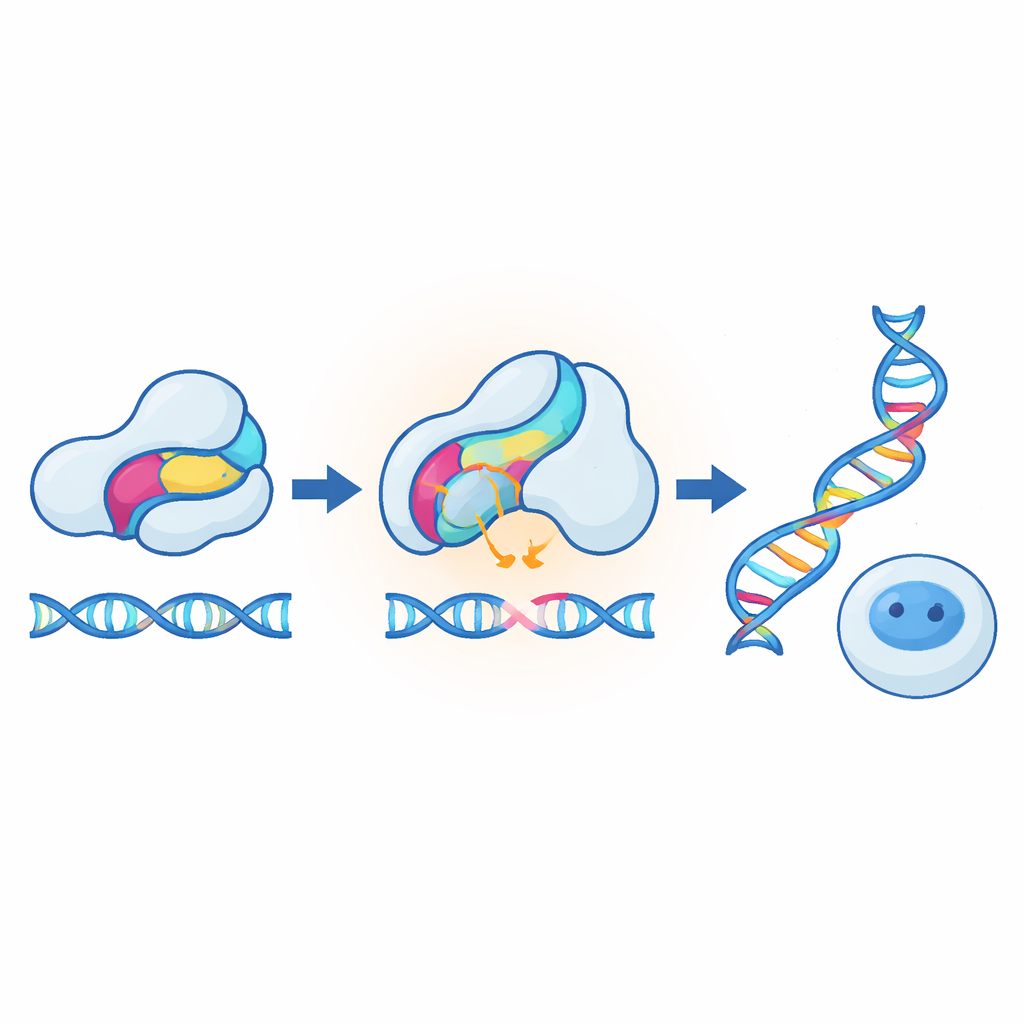
Wat dit betekent voor toekomstige therapieën en instrumenten
Voor leken komt de kern erop neer dat de auteurs een algemene receptuur hebben ontwikkeld om gewone eiwitten om te zetten in precieze biologische thermostaten. Door kleine sensordomeinen in te voegen en hun stabiliteit fijn af te stemmen, kunnen ze de eiwitactiviteit abrupt laten stijgen of dalen bij gekozen temperaturen binnen het normale menselijke bereik. Omdat de strategie modulair is, zou ze compatibel moeten zijn met veel bestaande optogenetische en chemogenetische ontwerpen, en ze kan direct op eiwitniveau werken in plaats van alleen op genexpressie. Op de lange termijn kunnen dergelijke temperatuurgevoelige schakelaars helpen om genbewerking veiliger en beter bestuurbaar te maken, hitte‑georiënteerde bacteriën mogelijk maken die zichzelf buiten gewenste omstandigheden vernietigen, en biologen voorzien van subtiele nieuwe middelen om te onderzoeken hoe cellen reageren op de geringste verandering in warmte.
Bronvermelding: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Trefwoorden: thermogenetica, eiwitschakelaars, CRISPR‑controle, allosterische regulatie, temperatuursensing