Clear Sky Science · es
Ingeniería modular de proteínas alostéricas termorresponsivas
Convertir el calor en un interruptor suave de encendido/apagado
Imagínese poder controlar la actividad de casi cualquier proteína en una célula viva simplemente calentándola un par de grados: sin fármacos, sin luz intensa, solo un pequeño cambio de temperatura. Este estudio muestra cómo los investigadores pueden construir tales "interruptores" proteicos sensibles al calor de forma modular, usando piezas que pueden enchufarse en muchas proteínas distintas. El resultado es un nuevo conjunto de herramientas que, algún día, podría ayudar a guiar terapias génicas, afinar tratamientos microbianos o explorar cómo funcionan las células, todo aprovechando el estrecho rango de temperatura alrededor del calor corporal normal.
Por qué la temperatura es un mando invisible y potente
Los científicos ya usan luz y productos químicos para activar o desactivar proteínas dentro de las células, pero ambos tienen inconvenientes prácticos. La luz a menudo no penetra profundamente en los tejidos, y los productos químicos pueden difundirse despacio y afectar a muchas partes del organismo a la vez. La temperatura, en cambio, penetra bien en los tejidos y puede aplicarse con gran precisión espacial y temporal. El problema ha sido que la mayoría de las herramientas térmicas existentes funcionan solo a temperaturas extremas o controlan la expresión génica de forma indirecta. Los autores se propusieron crear una estrategia general que les permitiera tomar una proteína corriente y darle una respuesta marcada a pequeños cambios de temperatura en el rango de 37–41 °C, aproximadamente la diferencia entre la temperatura corporal normal y una fiebre leve.
Insertar un minúsculo sensor en muchas proteínas
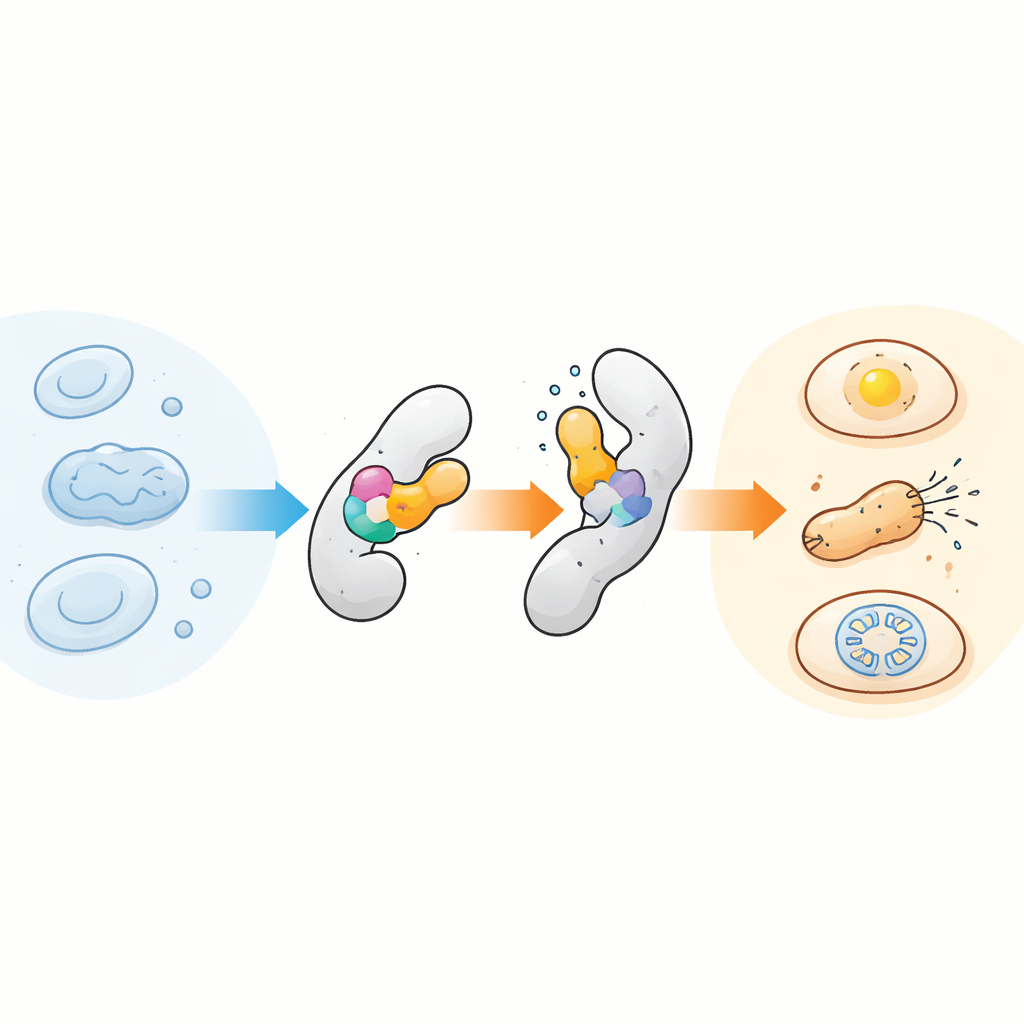
La idea central es engañosamente simple: insertar un dominio sensor compacto y sensible a la temperatura dentro de otra proteína de modo que un pequeño cambio estructural en el sensor se transmita a la proteína hospedadora, actuando como una bisagra interna. El equipo se centró en un módulo bien estudiado llamado AsLOV2, originalmente un sensor de luz de la avena, porque cambia de forma de manera natural. Descubrieron que este dominio también es sorprendentemente sensible a la temperatura, especialmente cuando se desestabiliza ligeramente mediante mutaciones específicas. Insertando versiones adaptadas de AsLOV2 en distintas posiciones de proteínas objetivo, crearon proteínas quiméricas cuya actividad se encendía o apagaba de forma abrupta en solo unos pocos grados. En bacterias, lo demostraron primero con AraC, un factor de transcripción, y luego evolucionaron variantes de AsLOV2 que hicieron la respuesta térmica más pronunciada, ajustable e incluso reversible con el tiempo.
De interruptores letales bacterianos a termostatos moleculares
Una vez que el enfoque funcionó para una proteína, los autores lo aplicaron a otras con funciones muy distintas. Insertar el sensor en una enzima de resistencia a antibióticos la convirtió en un interruptor letal activado por calor: las bacterias crecían a 37 °C pero morían a 41 °C al exponerse al fármaco. Una estrategia similar acopló el sensor a un componente de un activador génico basado en CRISPR en bacterias, permitiendo regular la expresión génica mediante un calentamiento suave. El equipo también exploró un truco relacionado en el que péptidos cortos de señalización quedan ocultos o expuestos por movimientos inducidos por calor de la cola del sensor, posibilitando degradación proteica dependiente de la temperatura en bacterias y un control modesto del tráfico proteico entre núcleo y citoplasma en células humanas.
Control afinado por calor de la edición del genoma en células humanas
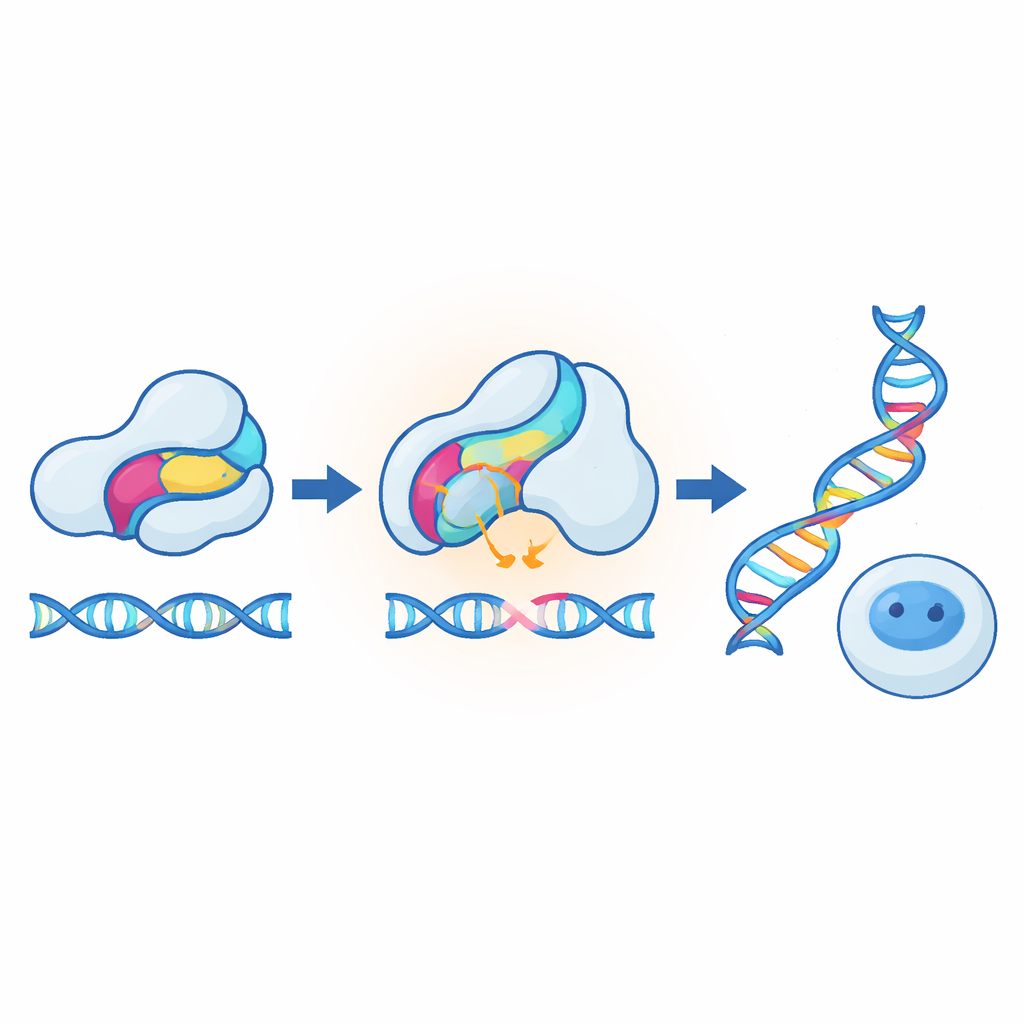
Las demostraciones más llamativas provinieron de adaptar el método a herramientas CRISPR en células de mamífero. En un diseño, el sensor se insertó en una proteína anti‑CRISPR que normalmente bloquea a un editor genómico; al calentar las células, el inhibidor se debilitaba y la edición aumentaba varios pliegues entre 37 °C y 40 °C. En otro diseño, el sensor se integró directamente en la propia Cas9, de modo que el calentamiento reducía la edición en lugar de aumentarla. Ambos modos funcionaron sobre múltiples genes diana, con poco impacto en la salud celular, y también pudieron transferirse a activadores transcripcionales basados en CRISPR. Los investigadores mostraron además que un módulo receptor completamente distinto —un dominio sensible al cortisol de un receptor hormonal— podía servir como inserto alternativo sensible a la temperatura, especialmente cuando la hormona estaba presente. Esto sugiere que muchos dominios sensores naturales, no solo los receptores de luz, pueden volverse inestables y funcionar como interruptores cuando se les lleva ligeramente por encima de sus temperaturas de operación habituales.
Qué significa esto para futuras terapias y herramientas
Para el público general, la conclusión es que los autores han desarrollado una receta general para convertir proteínas ordinarias en termostatos biológicos precisos. Insertando pequeños dominios sensores y ajustando finamente su estabilidad, pueden hacer que la actividad proteica aumente o disminuya bruscamente a temperaturas escogidas dentro del rango humano normal. Debido a que la estrategia es modular, debería ser compatible con muchos diseños optogenéticos y químogenéticos existentes, y puede actuar directamente a nivel de la función proteica en lugar de solo la expresión génica. A largo plazo, estos interruptores sensibles a la temperatura podrían ayudar a hacer la edición génica más segura y controlable, permitir bacterias guiadas por calor que se autodestruyan fuera de las condiciones deseadas y proporcionar a los biólogos nuevas y sutiles maneras de sondear cómo responden las células al más mínimo cambio de temperatura.
Cita: Kroell, AS., Hoffmann, K.H., Motzkus, N.A. et al. Modular engineering of thermoresponsive allosteric proteins. Nat Chem Biol 22, 751–758 (2026). https://doi.org/10.1038/s41589-026-02151-y
Palabras clave: termogenética, interruptores proteicos, control CRISPR, regulación alostérica, detección de temperatura