Clear Sky Science · tr
Yüksek içerikli CRISPR aktivasyon taramaları, kanser hücrelerini hedefe yönelik T hücresi sitotoksisitesine duyarlı hâle getirmek için sentetik olarak öldürücü RNA tabanlı mekanizmaları belirliyor
Vücudun Suikastçilerini Yeniden Kanserin Üzerine Çevirmek
Bağışıklık sistemimiz, kanser hücrelerini olağanüstü bir hassasiyetle tanıyıp yok edebilen profesyonel “vurucu” hücreler olan T hücreleri ile donanmıştır. Yine de birçok tümör bu saldırılardan sıyrılmayı öğrenir ve günümüz immünoterapilerinin gücünü azaltır. Bu çalışma yükselen bir fikri araştırıyor: yalnızca kanserin kaçmasına yardımcı olan genleri engellemek yerine, sağlıklı hücreleri büyük ölçüde dokunmadan bırakarak kanser hücrelerinin T hücresi saldırısına son derece savunmasız hâle gelmesi için kanser hücreleri içinde belirli RNA mesajlarını etkinleştirebilir miyiz?
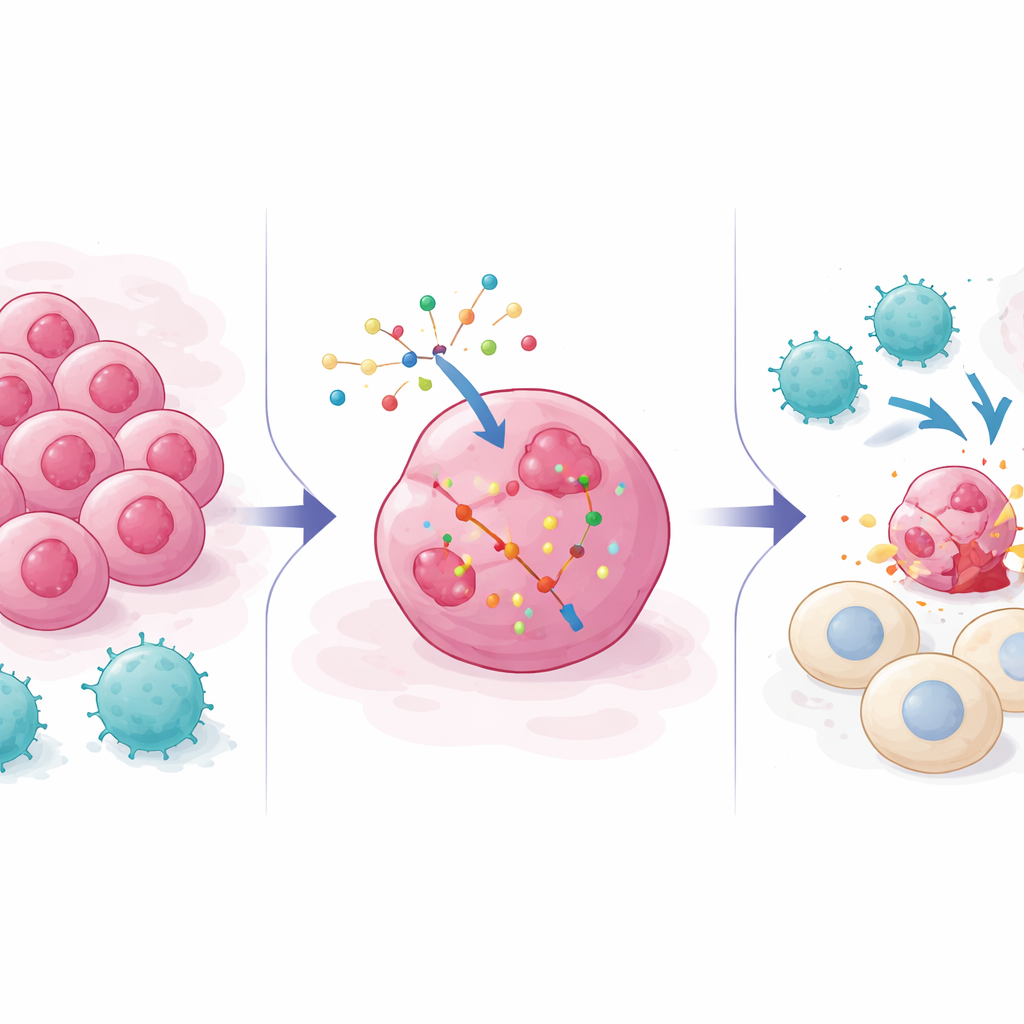
Kanser Hücrelerinin Bağışıklık Vurucu Ekibinden Nasıl Kaçtıkları
Güncel kanser tedavileri, kontrol noktası inhibitörlerinden tasarlanmış T hücresi terapilerine kadar, tümör hücrelerindeki ayırt edici molekülleri tanıyan ve sonra onları yok eden CD8 T hücrelerine büyük ölçüde dayanır. Ancak tümörler sıklıkla uyum sağlar: T hücrelerinin aradığı işaretleri saklayabilir, interferon gibi alarm sinyallerini zayıflatabilir veya hücre ölümünü engelleyen hayatta kalma yollarını yükseltebilir. Önceki genetik taramalar çoğunlukla genleri kapatan “knockout”ları kullandı; hangi genlerin tümörlerin immün saldırıya direnmesine yardımcı olduğunu görmek için genleri devre dışı bıraktılar. Bu çabalar birçok kaçış yolunu haritalandırdı ama RNA tabanlı ilaçlar gibi etkinliği kaldırmak yerine ekleyen veya artıran araçlarla kanser hücrelerini ters yönde — T hücrelerine karşı daha duyarlı hâle — nasıl iteceğimizi göstermedi.
Binlerce Geni Gizli Zayıf Noktalar İçin Taramak
Araştırmacılar, genler için programlanabilir bir ses düğmesi gibi davranan CRISPR aktivasyon teknolojisini kullanarak melanom hücrelerinde neredeyse 3.000 geni sistematik olarak yükseltti ve bunları ortak bir tümör antijenini tanıyacak şekilde mühendislik yapılmış T hücrelerine maruz bıraktı. Hangi genetik değişikliklerin kanser hücrelerinin daha fazla veya daha az öldüğünü izleyerek, iki ana grup belirlediler: kanser hücrelerini koruyan “direnç” genleri ve onları T hücreleri için çok daha kolay hedef hâline getiren “duyarlılık” genleri. Duyarlılık genleri arasında CASP3 ve BID gibi iyi bilinen hücre ölüm oyuncuları ile SAFB ve TSPYL2 gibi RNA işlenmesi ve 3B genom organizasyonunun daha az belirgin düzenleyicileri ve Wnt ligandları gibi sinyal molekülleri vardı. Bireysel hedeflerin test edilmesi, bu genleri yükseltmenin kanser hücrelerini ya koruyabileceğini ya da farklı kanser türlerinde ve kanser yapıcı virüslerle enfekte hücrelerde bile yok edilmeye hazır hâle getirebileceğini doğruladı.
RNA Tabanlı Sentetik Letalite: Sadece Nişan Alındığında Tehlikeli
Çalışmadan ortaya çıkan merkezi kavramlardan biri “immün RNA tabanlı sentetik letalitedir.” CASP3 gibi bazı genler, yalnız büyüyen kanser hücrelerinde aşırı eksprese edildiklerinde özellikle zararlı değildir. Ancak T hücreleri hedefleriyle etkileşime girdikten sonra, ekstra CASP3 proteini uykuda olan bir formdan hızlıca apoptozu — programlı hücre ölüm yolunu — tetikleyen güçlü bir idam ediciye dönüştürülür. Ekip, CASP3 RNA’sının tümör hücrelerine verilmesinin izole büyümelerini bozmadığını ama T hücresi aracılı öldürmeyi belirgin şekilde artırdığını ve kaspaz aktivitesinin engellenmesinin bu hücreleri kurtarabileceğini gösterdi. SAFB gibi diğer genler daha da seçiciydi: SAFB’yi yükseltmek kanser hücresinin günlük transkriptomunu zar zor değiştirirken, T hücrelerinin kullandığı granzyme–perforin yoluyla özgül olarak öldürmeyi dramatik şekilde artırdı ve yaygın inflamatuar moleküllere yanıtları büyük ölçüde dokunulmamış bıraktı.
Tümörlerin İçine Hücre Hücre Bakmak
Bu duyarlılık ve direnç genlerinin gerçek dokuda nasıl çalıştığını anlamak için yazarlar CRISPR aktivasyonunu, binlerce bireysel hücrenin RNA profillerini ve genetik bozulmalarını aynı anda okuyan yüksek verimli bir yöntem olan Perturb-seq ile birleştirdiler. Bunu daha sonra bozulma barkodlarını ve gen aktivitesini doğrudan tek hücre çözünürlüğünde sağlam tümör dilimlerinde tespit eden “in situ Perturb-seq”e genişlettiler. Bu mekânsal haritalar, tümörlerin T hücresi saldırısından kurtulmak için kullandığı gen ağlarını ortaya koydu; bunlar arasında hücre dışı matriks bileşenleri ve hücre yüzeyi reseptörlerini içeren merkez noktalar vardı. Ayrıca kanser hücresi bozulmalarının yakınlardaki immün ve stromal hücreleri nasıl yeniden şekillendirdiğini açıkladılar. Örneğin belirli Wnt ligandlarını aşırı eksprese etmeye zorlanan kanser hücreleri, daha etkin bir durumda olan T hücreleriyle çevriliydi ve laboratuvar deneyleri çözünür Wnt3a’nın insan T hücresi öldürmesini ve sitokin üretimini güçlendirebileceğini doğruladı.
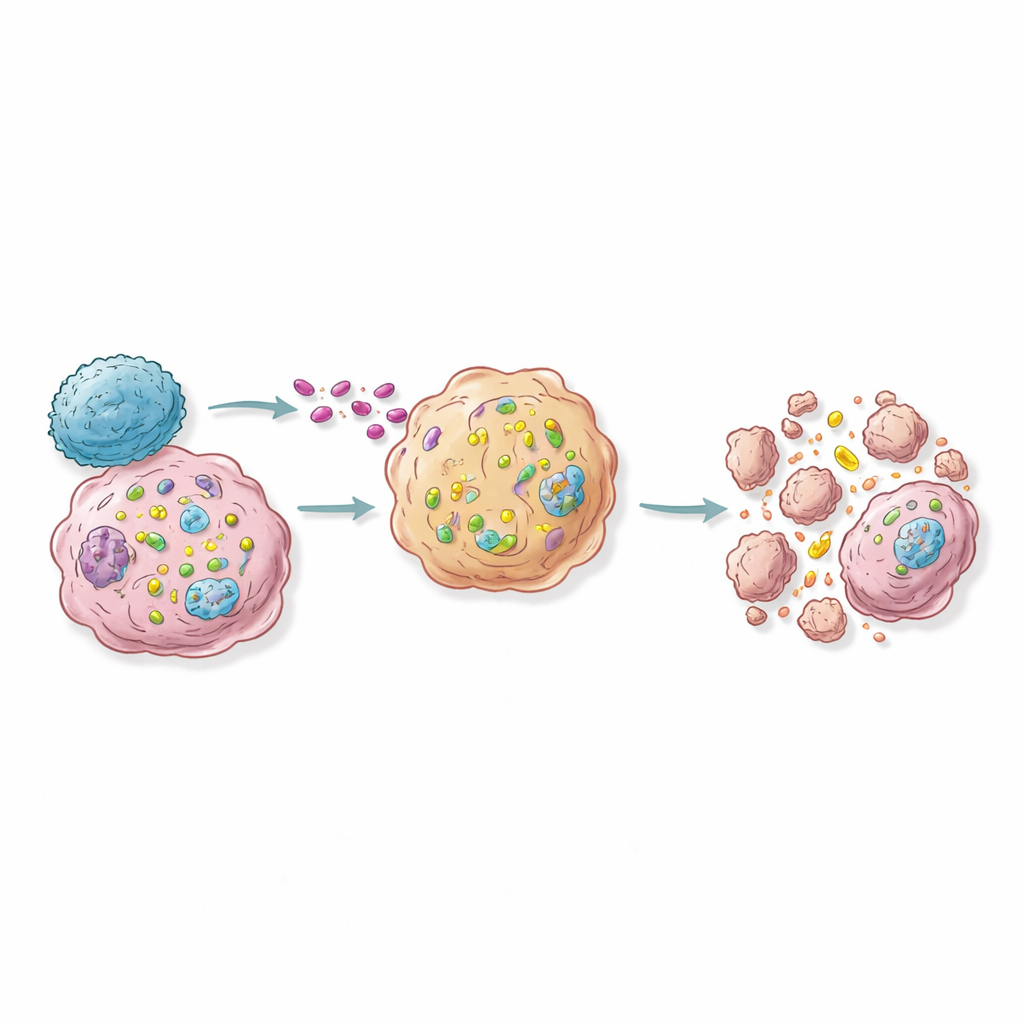
Gen Haritalarından Gelecek RNA İmmünoterapilerine
Fare modellerinde, önde gelen birkaç “duyarlılık” geninin yalnızca bir tümör hücresi fraksiyonunda aktive edilmesi tümör büyümesini yavaşlatmak veya hatta önlemek ve değiştirilen hücrelerin ötesinde bir dalga etkisini göstermek için yeterliydi; yakındaki lenf düğümleri immün hücrelerle dolup taşmıştı. Çalışma bir sonraki nesil terapiler için bir yol haritası öneriyor: tümörlerdeki kilit duyarlılık genlerinin aktivitesini seçici olarak yükselten RNA molekülleri veya gen-aktivasyon yapılarını teslim etmek ya da bu yolları kullanacak şekilde terapötik T hücrelerini mühendislik yapmak. Bir okur için çıkarım, bilim insanlarının kanser hücrelerini yeniden kablolamayı öğreniyor olmasıdır; böylece vücudun kendi T hücreleri geldiğinde bu hücreler içten bir tür kapanla döşenmiş hâle geliyor. Bağışıklığı geniş çapta güçlendirmek—ki bu ciddi yan etkilere yol açabilir—yerine, bu strateji yalnızca tehlikeli hücreleri hassas bir immün saldırıya ölümcül derecede duyarlı hâle getirmeyi amaçlıyor.
Atıf: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Anahtar kelimeler: kanser immünoterapisi, T hücresi öldürmesi, CRISPR aktivasyonu, RNA terapötikleri, sentetik letalite