Clear Sky Science · ru
Высокопроизводительные CRISPR-активационные скрининги выявляют синтетически летальные РНК‑механизмы, повышающие чувствительность раковых клеток к прицельной цитотоксичности Т‑клеток
Включая в организме «убийц» против рака
Наша иммунная система оснащена профессиональными «киллерами» — Т‑клетками, которые способны распознавать и уничтожать раковые клетки с поразительной точностью. Тем не менее многие опухоли учатся уклоняться от этих атак, ослабляя эффективность современных иммунотерапий. В этом исследовании рассматривается новая идея: вместо того чтобы лишь блокировать гены, помогающие опухоли ускользнуть, что если мы сможем включать специфические РНК‑сообщения внутри раковых клеток, делая их чрезвычайно уязвимыми для атаки Т‑клеток — при этом здоровые клетки останутся в основном невредимыми?
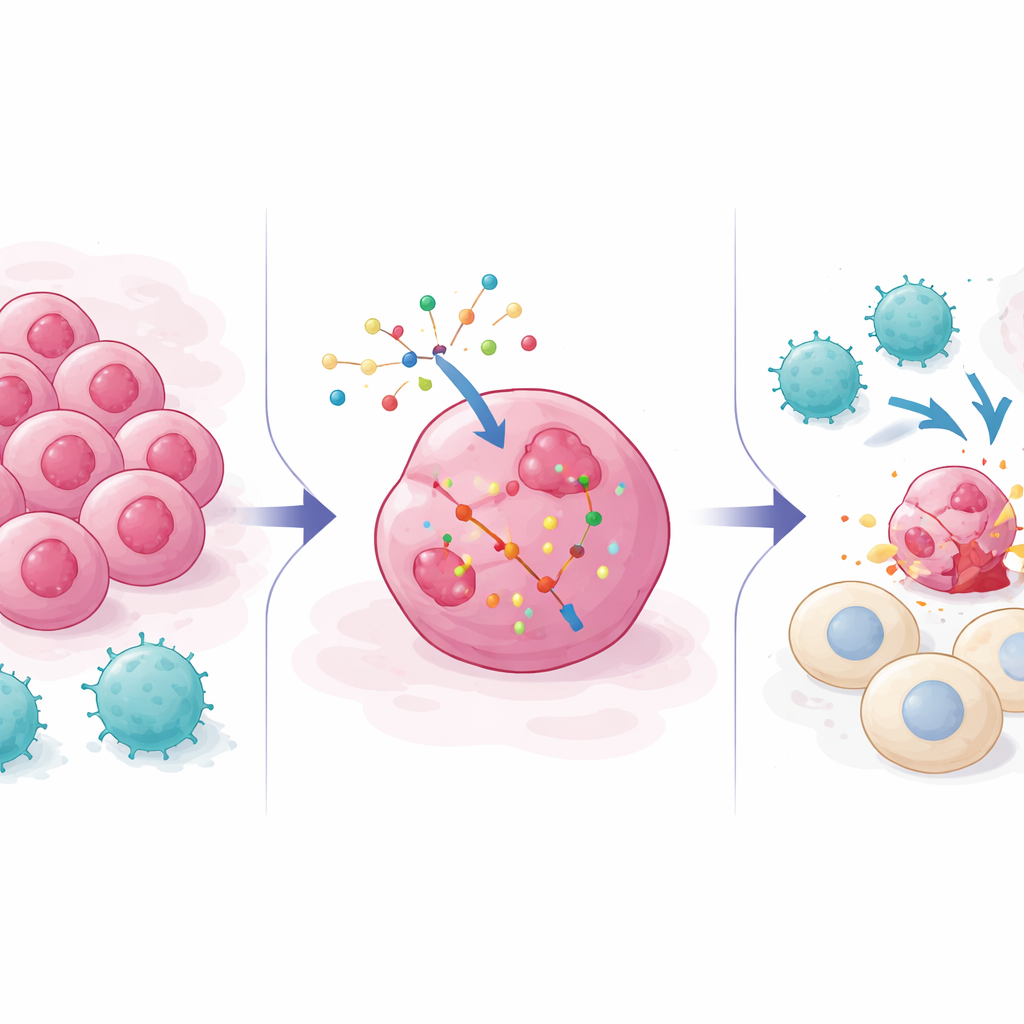
Почему раковые клетки избегают «ударной бригады» иммунитета
Современные методы лечения рака — от ингибиторов контрольных точек до генетически модифицированных Т‑клеточных терапий — во многом опираются на CD8 Т‑клетки, которые распознают характерные молекулы на опухолевых клетках и затем их убивают. Но опухоли часто адаптируются: они могут скрывать маркеры, по которым распознают Т‑клетки, ослаблять сигналы тревоги, такие как интерфероны, или усиливать пути выживания, блокирующие гибель клеток. Предыдущие генетические скрининги в основном использовали «выключения» (knockout), чтобы определить, какие гены помогают опухолям сопротивляться иммунной атаке. Эти работы выявили множество путей ухода от иммунитета, но не показали, как направленно подтолкнуть раковые клетки в обратную сторону — к повышенной чувствительности к Т‑клеткам — с помощью инструментов вроде РНК‑лекарств, которые добавляют или усиливают активность генов, а не удаляют её.
Скрининг тысяч генов в поисках скрытых уязвимостей
Исследователи использовали CRISPR‑активацию, технологию, действующую как программируемая «регулятор громкости» для генов, чтобы системно повысить экспрессию почти 3000 генов в клетках меланомы при одновременном воздействии на них Т‑клеток, запрограммированных распознавать общий опухолевый антиген. Отслеживая, какие генетические изменения увеличивали или уменьшали гибель раковых клеток, они выделили две основные группы: гены «сопротивления», защищающие опухоли, и гены «сенситизации», делающие их гораздо более уязвимыми для Т‑клеточного уничтожения. К сенситизирующим генам отнесли известные участники путей клеточной гибели, такие как CASP3 и BID, а также менее очевидные регуляторы РНК‑обработки и трехмерной организации генома, например SAFB и TSPYL2, и сигнальные молекулы, такие как лигандные белки Wnt. Тестирование отдельных кандидатов подтвердило, что их повышенная экспрессия может либо защищать раковые клетки, либо подготавливать их к уничтожению, даже в различных типах рака и в клетках, инфицированных онкогенными вирусами.
РНК‑основанная синтетическая летальность: опасно только при «прицеле»
Ключевая концепция, вытекающая из работы, — «иммунная РНК‑основанная синтетическая летальность». Некоторые гены, например CASP3, сами по себе не наносят серьезного вреда при сверхэкспрессии в изолированных раковых клетках. Однако когда Т‑клетки вступают в контакт с мишенями, дополнительный белок CASP3 быстро активируется из неактивной формы в мощного исполнителя, запускающего апоптоз — программируемую гибель клетки. Команда показала, что доставка CASP3‑РНК в опухолевые клетки не мешала их росту в изоляции, но значительно усиливала Т‑клеточное уничтожение, и что блокада активности каспаз могла спасти эти клетки. Другие гены, например SAFB, вели себя ещё более выборочно: увеличение SAFB практически не меняло повседневный транскриптом клетки, но значительно усиливало гибель именно через путь гранзим–перфорин, используемый Т‑клетками, оставляя в основном нетронутыми ответы на обычные воспалительные молекулы.
Заглядывая в опухоль по одной клетке
Чтобы понять, как действуют эти сенситизирующие и сопротивляющиеся гены в реальной ткани, авторы объединили CRISPR‑активацию с Perturb‑seq — высокопроизводительным методом, который одновременно считывает РНК‑профили и генетические возмущения тысяч отдельных клеток. Затем они расширили подход до «in situ Perturb‑seq», который обнаруживает штрих‑коды возмущений и активность генов прямо в интактных срезах опухоли с разрешением на уровне отдельных клеток. Эти пространственные карты показали сети генов, которые опухоли приспосабливают для выживания при атаке Т‑клеток, включая узлы, связанные с компонентами внеклеточного матрикса и поверхностными рецепторами. Они также продемонстрировали, как изменения в опухолевых клетках перестраивают соседние иммунные и стромальные клетки. Например, опухолевые клетки с вынужденной сверхэкспрессией некоторых Wnt‑лигандов оказывались окружены более активными Т‑клетками, а лабораторные эксперименты подтвердили, что растворимый Wnt3a может существенно усилить убивающую и цитокиновую активность человеческих Т‑клеток.
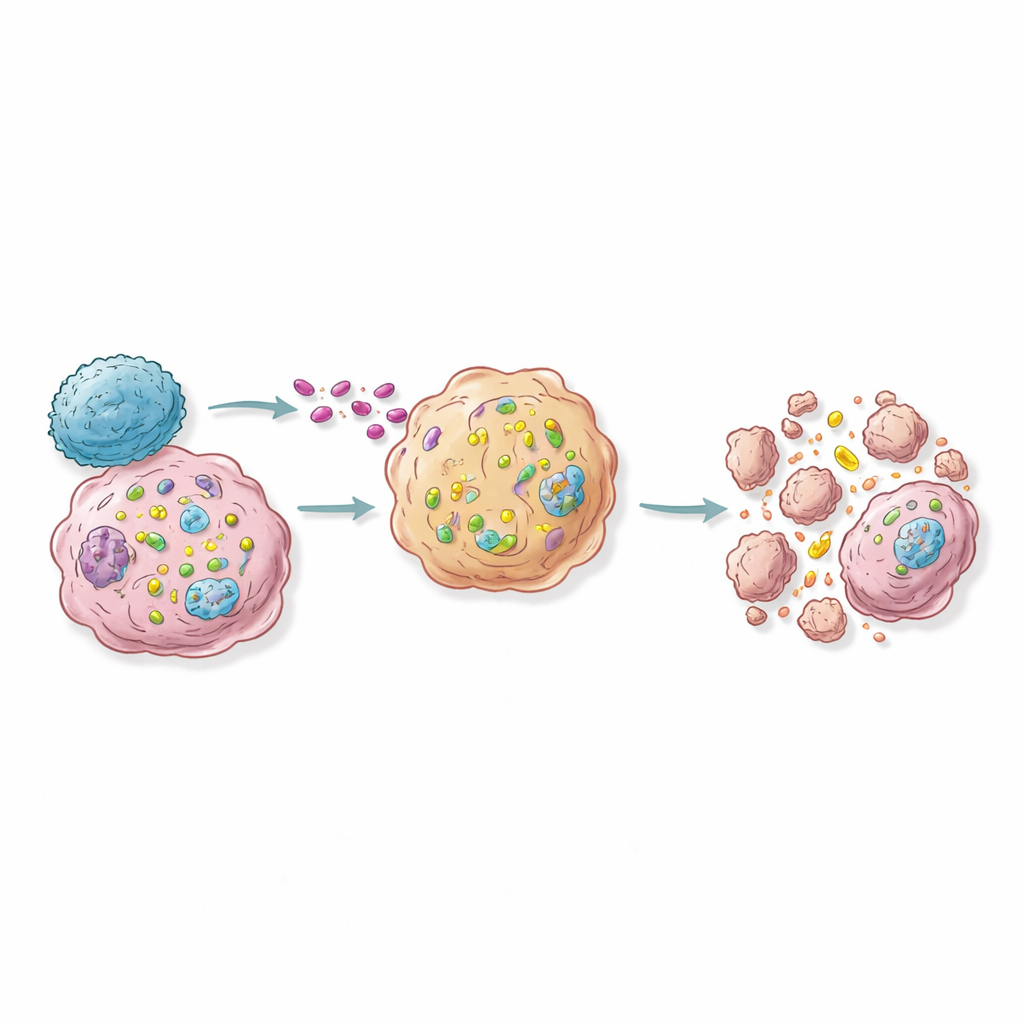
От генетических карт к будущим РНК‑иммунотерапиям
В модельных экспериментах на мышах активация нескольких ведущих «сенситизирующих» генов лишь в части клеток опухоли оказалась достаточной, чтобы замедлить или даже предотвратить рост опухоли и увеличить близлежащие лимфатические узлы, заполненные иммунными клетками, что указывает на эффект волны за пределами модифицированных клеток. Исследование предлагает дорожную карту для следующих поколений терапий: доставлять РНК‑молекулы или конструкты, активирующие гены, которые селективно повышают активность ключевых сенситизирующих генов в опухолях, либо проектировать терапевтические Т‑клетки так, чтобы они использовали эти пути. Для неспециалиста вывод таков: учёные учатся перепрограммировать раковые клетки так, чтобы, когда собственные Т‑клетки организма придут на место, эти клетки оказались внутренне «подложенными бомбами». Вместо общего усиления иммунитета — что может вызывать серьёзные побочные эффекты — эта стратегия стремится сделать фатально чувствительными только опасные клетки для точечного иммунного удара.
Цитирование: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Ключевые слова: иммунотерапия рака, убийство Т‑клетками, CRISPR‑активация, РНК‑терапевтика, синтетическая летальность