Clear Sky Science · ja
ハイコンテンツCRISPR活性化スクリーニングが、標的化されたT細胞の細胞傷害性に対するがん細胞の感受性を高める合成致死性RNA機構を同定
体内の「暗殺者」を再びがんに向ける
私たちの免疫系には、がん細胞を精密に認識して殺すプロの「ヒット細胞」であるT細胞が備わっています。しかし多くの腫瘍はこれらの攻撃をかわす術を身につけ、現行の免疫療法の効果を弱めてしまいます。本研究は新興の発想を探ります。すなわち、がんの“逃避”を助ける遺伝子をただ阻害するのではなく、がん細胞内の特定のRNAメッセージを能動的にオンにすることで、正常細胞を大きく傷つけることなくT細胞攻撃に対して極めて脆弱にできないか、という考えです。
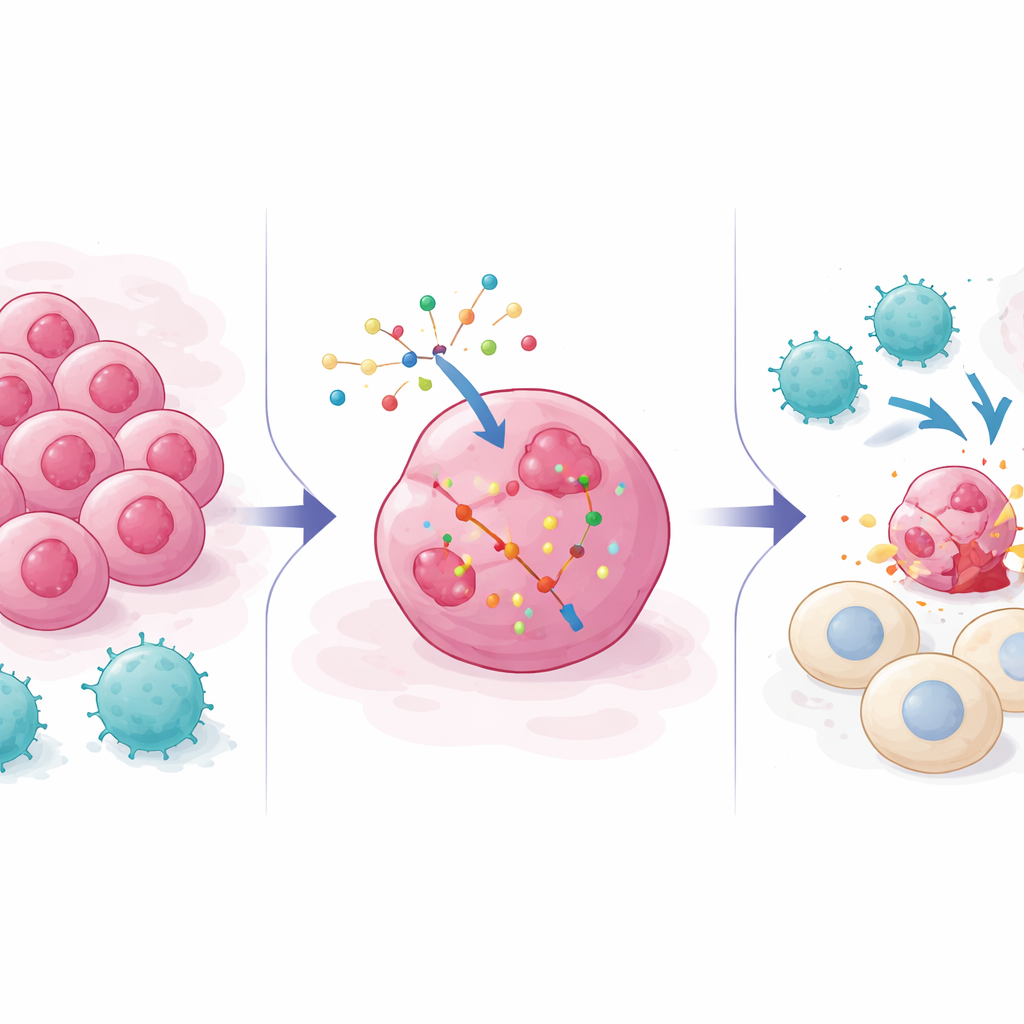
なぜがん細胞は免疫の追手から逃れるのか
チェックポイント阻害剤から改変T細胞療法まで、現代のがん治療は腫瘍細胞上の目印を認識して殺すCD8 T細胞に大きく依存しています。しかし腫瘍は適応します:T細胞が探すマーカーを隠したり、インターフェロンなどの警報信号を抑えたり、細胞死を阻む生存経路を高めたりします。従来の遺伝学的スクリーニングは主に「ノックアウト」を用い、遺伝子をオフにしてどれが腫瘍の免疫耐性を支えるかを調べてきました。そうした努力は多くの逃避経路を解明しましたが、RNAベースの薬剤のように遺伝子活性を加えたり高めたりするツールで、がん細胞を逆にT細胞に対してより感受性が高い方向へ押しやる方法は示していませんでした。
何千もの遺伝子を走査して隠れた弱点を探る
研究者たちはCRISPR活性化という、遺伝子の音量つまみのように機能する技術を使い、メラノーマ細胞で約3,000個の遺伝子を系統的に活性化しながら、共通の腫瘍抗原を認識するよう改変したT細胞に晒しました。どの遺伝子変化ががん細胞の死を増やすか減らすかを追跡することで、「耐性」遺伝子(がん細胞を守る)と「感作」遺伝子(T細胞にとって殺しやすくする)の2つの主要群を同定しました。感作遺伝子にはCASP3やBIDといった既知の細胞死関連因子のほか、SAFBやTSPYL2のようなRNA処理や3次元ゲノム構造のあまり明白でない制御因子、Wntリガンドのようなシグナル分子も含まれていました。個別のヒットを検証したところ、これらの遺伝子を上げればがん細胞を保護したり、逆に破壊に備えさせたりでき、異なるがん種やがん原ウイルスに感染した細胞でも同様の効果が確認されました。
RNAベースの合成致死性:標的に入るとだけ危険になる
本研究から浮かび上がった中心概念は「免疫RNAベースの合成致死性」です。たとえばCASP3のような遺伝子は、単独で増強されても単体のがん細胞にとって特に有害ではありません。しかしT細胞が標的に接触すると、余分に存在するCASP3タンパク質が不活性な形から急速に活性化され、アポトーシス—プログラムされた細胞死—を駆動する強力な実行因子に変わります。チームはCASP3のRNAを腫瘍細胞へ送達しても単独では増殖を損なわないが、T細胞媒介の殺傷を著しく増強すること、そしてカスパーゼ活性を阻害すればこれらの細胞を救えることを示しました。SAFBのような他の遺伝子はさらに選択的に振る舞いました:SAFBを上げても日常的なトランスクリプトームはほとんど変わらない一方で、T細胞が用いるグランザイム–パーフォリン経路を介した殺傷を劇的に高め、一般的な炎症性分子への応答にはほとんど影響を与えませんでした。
腫瘍の内部を一細胞ずつ覗く
これらの感作・耐性遺伝子が実際の組織でどのように働くかを理解するため、著者らはCRISPR活性化とPerturb-seqを組み合わせました。Perturb-seqは何千もの個々の細胞のRNAプロファイルと遺伝的撹乱を同時に読み出すハイスループット手法です。さらに彼らはこれを「in situ Perturb-seq」に拡張し、切片化していない腫瘍組織中で撹乱バーコードと遺伝子活性を単一細胞分解能で直接検出しました。これらの空間マップは、腫瘍がT細胞攻撃から生き残るために取り込む遺伝子ネットワークを明らかにし、細胞外マトリックス成分や細胞表面受容体を含むハブを示しました。また、がん細胞の撹乱が周囲の免疫細胞や間質細胞をどのように再構成するかも明らかになりました。たとえば特定のWntリガンドを過剰発現するよう強制されたがん細胞は、より活性化状態にあるT細胞に囲まれており、実験室レベルの検証では可溶性Wnt3aがヒトT細胞の殺傷力とサイトカイン産生を強化しうることが確認されました。
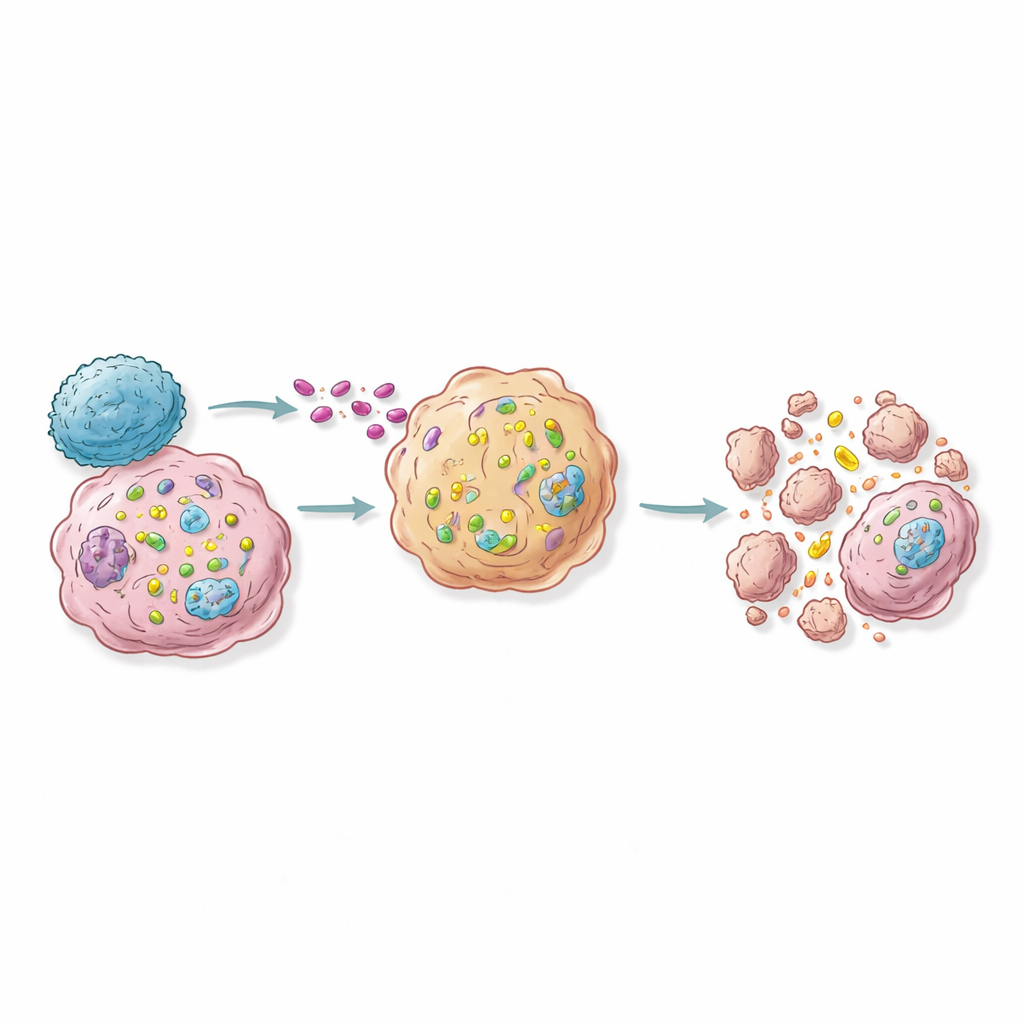
遺伝子マップから次世代のRNA免疫療法へ
マウスモデルでは、トップの「感作」遺伝子の一握りを腫瘍細胞の一部だけで活性化するだけで、腫瘍の成長が遅延または阻止され、免疫細胞が詰まった近傍のリンパ節が拡大することが示され、修飾された細胞を越えた波及効果が示唆されました。本研究は次世代治療へのロードマップを示唆します:腫瘍内で選択的に主要な感作遺伝子の活性を高めるRNA分子や遺伝子活性化コンストラクトを送達する、あるいは治療用T細胞をこれらの経路を利用するように設計するなどです。一般の方への要点は、研究者たちががん細胞を書き換える方法を学んでおり、体内のT細胞が到達したときにこれらの細胞が内部から「地雷」を仕掛けられた状態になるようにできる、ということです。免疫を広く増強して深刻な副作用を招くのではなく、この戦略は危険な細胞だけを正確な免疫攻撃に対して致命的に感受性にすることを目指します。
引用: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
キーワード: 癌免疫療法, T細胞による殺傷, CRISPR活性化, RNA治療薬, 合成致死性