Clear Sky Science · pt
Telas de ativação CRISPR de alto conteúdo identificam mecanismos sinteticamente letais baseados em RNA para sensibilizar células cancerosas à citotoxicidade dirigida por células T
Reativando os Assassinos do Corpo Contra o Câncer
Nosso sistema imune dispõe de “células de ataque” profissionais chamadas células T, capazes de reconhecer e eliminar células cancerosas com notável precisão. Ainda assim, muitos tumores aprendem a escapar desses ataques, enfraquecendo a eficácia das imunoterapias atuais. Este estudo explora uma ideia emergente: em vez de apenas bloquear genes que ajudam o câncer a escapar, e se pudéssemos ativar mensagens específicas de RNA dentro das células tumorais para torná-las extremamente vulneráveis ao ataque das células T — preservando, em grande parte, as células saudáveis?
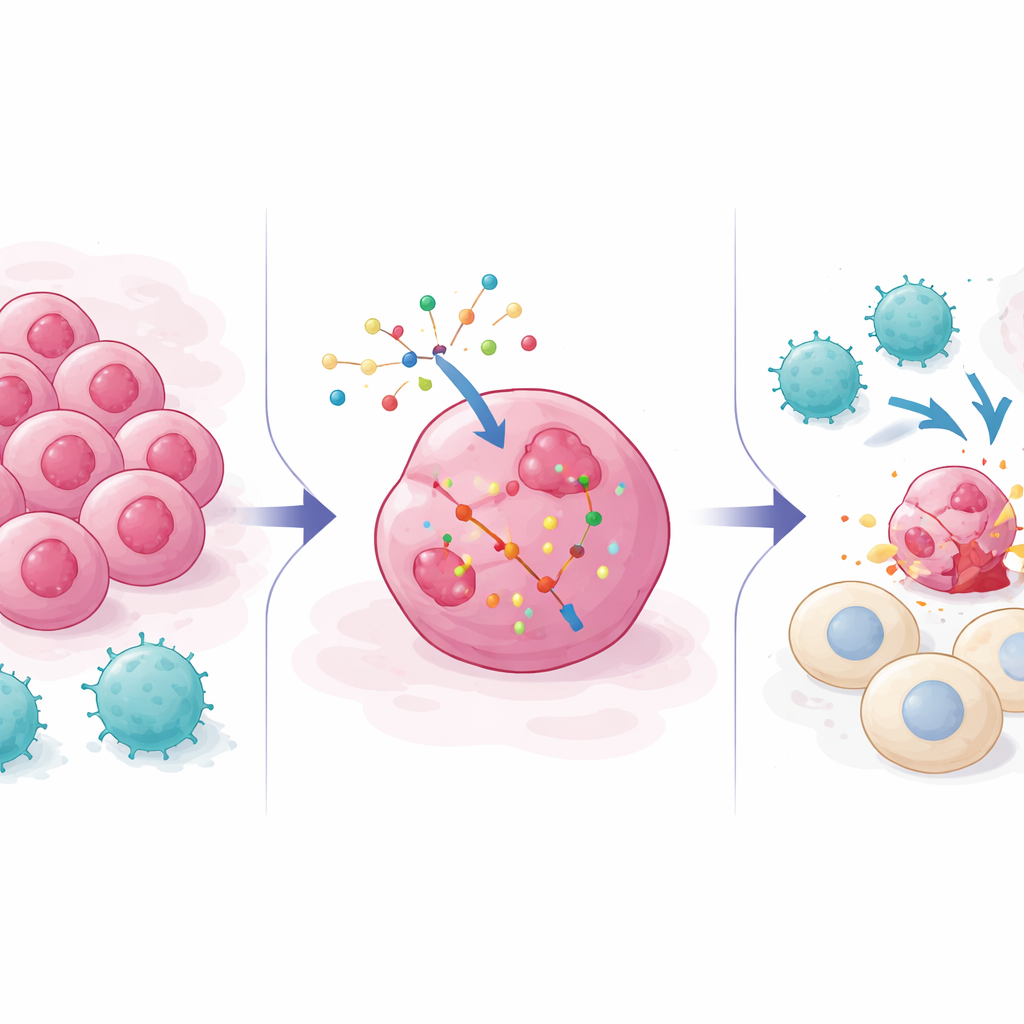
Por que as Células Cancerosas Escapam da Equipe de Ataque Imune
Os tratamentos modernos contra o câncer, desde inibidores de checkpoint até terapias com células T modificadas, dependem muito de células T CD8 que reconhecem moléculas indicadoras nas células tumorais e as eliminam. Mas os tumores costumam se adaptar: podem esconder os marcadores que as células T procuram, suprimir sinais de alarme como interferons ou ativar vias de sobrevivência que bloqueiam a morte celular. Triagens genéticas anteriores usaram majoritariamente “knockouts”, desligando genes para ver quais ajudam os tumores a resistir ao ataque imune. Esses esforços mapearam muitas rotas de escape, mas não mostraram como empurrar as células cancerosas na direção oposta — rumo a uma maior sensibilidade às células T — usando ferramentas como fármacos baseados em RNA que acrescentam ou aumentam atividade gênica em vez de a remover.
Varrendo Milhares de Genes em Busca de Pontos Fracos Ocultos
Os pesquisadores usaram ativação CRISPR, uma tecnologia que funciona como um botão de volume programável para genes, para aumentar sistematicamente quase 3.000 genes em células de melanoma enquanto as expunham a células T projetadas para reconhecer um antígeno tumoral compartilhado. Ao rastrear quais mudanças genéticas faziam as células cancerosas morrerem mais ou menos, identificaram dois grupos principais: genes de “resistência” que protegiam as células tumorais, e genes “sensibilizantes” que as tornavam muito mais fáceis de serem eliminadas pelas células T. Entre os genes sensibilizantes estavam conhecidos mediadores da morte celular, como CASP3 e BID, além de reguladores menos óbvios do processamento de RNA e da organização 3D do genoma, como SAFB e TSPYL2, e moléculas de sinalização como ligantes Wnt. Testes de alvos individuais confirmaram que aumentar a expressão desses genes podia tanto proteger as células cancerosas quanto prepará-las para destruição, mesmo em diferentes tipos de câncer e em células infectadas por vírus oncoproteicos.
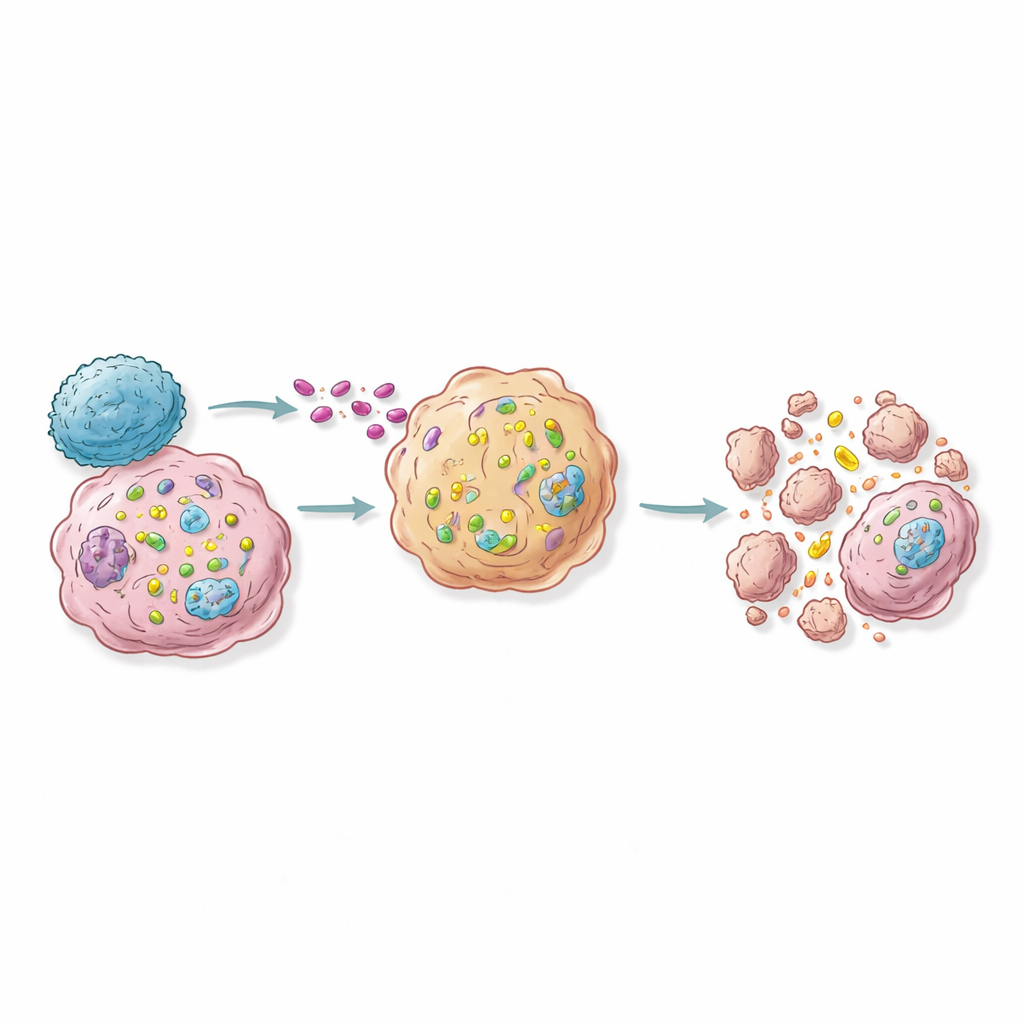
Letalidade Sintética Baseada em RNA: Perigosa Apenas no Alvo
Um conceito central que emerge do trabalho é a “letalidade sintética imune baseada em RNA.” Alguns genes, como CASP3, não são especialmente nocivos quando superexpressos em células tumorais em isolamento. Contudo, uma vez que as células T se engajam com seus alvos, a proteína CASP3 adicional é rapidamente convertida de uma forma dormente em um executor poderoso que desencadeia a apoptose — a via de morte celular programada. A equipe demonstrou que entregar RNA de CASP3 às células tumorais não prejudicava seu crescimento isoladamente, mas aumentava significativamente a morte mediada por células T, e que bloquear a atividade das caspases podia resgatar essas células. Outros genes, como SAFB, comportaram-se de forma ainda mais seletiva: aumentar SAFB mal alterava o transcriptoma cotidiano da célula cancerosa, mas aumentava dramaticamente a morte especificamente via via granzima–perfurina usada pelas células T, deixando intactas as respostas a moléculas inflamatórias comuns.
Observando Tumores Célula a Célula
Para entender como esses genes sensibilizantes e de resistência funcionam em tecido real, os autores combinaram ativação CRISPR com Perturb-seq, um método de alto rendimento que lê perfis de RNA e perturbações genéticas de milhares de células individuais ao mesmo tempo. Em seguida, estenderam isso para a “Perturb-seq in situ”, que detecta códigos de barras de perturbação e atividade gênica diretamente em fatias tumorais intactas com resolução unicelular. Esses mapas espaciais revelaram redes de genes que os tumores cooptam para sobreviver ao ataque das células T, incluindo hubs envolvendo componentes da matriz extracelular e receptores de superfície celular. Também mostraram como perturbações nas células cancerosas remodelam células imunes e estromais próximas. Por exemplo, células tumorais forçadas a superexpressar certos ligantes Wnt foram cercadas por células T em um estado mais ativado, e experimentos de laboratório confirmaram que Wnt3a solúvel podia potencializar fortemente a morte e a produção de citocinas por células T humanas.
De Mapas Genéticos a Futuras Imunoterapias de RNA
Em modelos murinos, ativar um punhado dos principais genes “sensibilizantes” em apenas uma fração das células tumorais foi suficiente para retardar ou até prevenir o crescimento tumoral e para ampliar gânglios linfáticos próximos repletos de células imunes, indicando um efeito em cascata além das células modificadas. O estudo sugere um roteiro para terapias de próxima geração: entregar moléculas de RNA ou constructos ativadores de genes que elevem seletivamente a atividade de genes sensibilizantes-chave nos tumores, ou projetar células T terapêuticas para explorar essas vias. Para o público leigo, a conclusão é que os cientistas estão aprendendo a reprogramar as células cancerosas de modo que, quando as próprias células T do corpo chegarem, essas células passem a estar armadas por dentro. Em vez de aumentar a imunidade de forma ampla — o que pode causar efeitos colaterais graves — essa estratégia visa tornar apenas as células perigosas fatalmente sensíveis a um ataque imune preciso.
Citação: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Palavras-chave: imunoterapia contra o câncer, morte por células T, ativação CRISPR, terapêuticos de RNA, letalidade sintética