Clear Sky Science · pl
Skrypty wysokoprzepustowych ekranów aktywacji CRISPR identyfikują syntetycznie letalne mechanizmy oparte na RNA, uczulające komórki nowotworowe na celowaną cytotoksyczność limfocytów T
Skłanianie ciałowych zabójców z powrotem przeciw rakowi
Nasz układ odpornościowy dysponuje wyspecjalizowanymi „komórkami zabójcami” zwanymi limfocytami T, które potrafią rozpoznać i precyzyjnie zniszczyć komórki nowotworowe. Wiele nowotworów jednak uczy się omijać te ataki, osłabiając skuteczność współczesnych immunoterapii. W tym badaniu badacze analizują pojawiającą się koncepcję: zamiast jedynie blokować geny wspierające ucieczkę raka, co by było gdybyśmy mogli włączać określone przekazy RNA w komórkach nowotworowych, aby uczynić je wyjątkowo podatnymi na atak limfocytów T — przy jednoczesnym pozostawieniu komórek zdrowych w dużej mierze nienaruszonych?
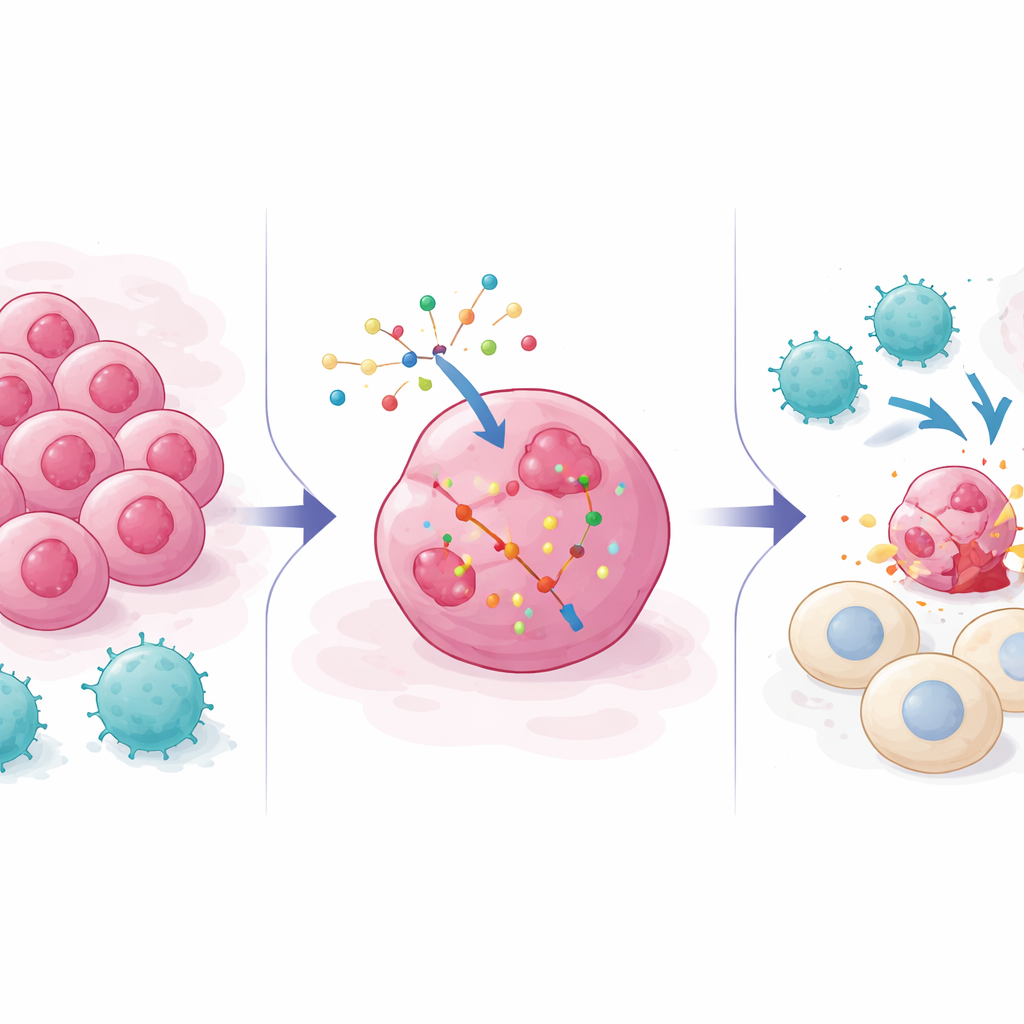
Dlaczego komórki nowotworowe uciekają przed oddziałem uderzeniowym immunologicznym
Współczesne terapie przeciwrakowe, od inhibitorów punktów kontrolnych po modyfikowane limfocyty T, w dużej mierze opierają się na limfocytach CD8 rozpoznających charakterystyczne cząsteczki na komórkach guza, po czym je zabijających. Jednak guzy często się dostosowują: mogą ukrywać markery rozpoznawane przez limfocyty T, tłumić sygnały alarmowe, takie jak interferony, albo wzmacniać szlaki przeżycia blokujące śmierć komórkową. Poprzednie ekrany genetyczne w większości używały „wyciszeń” (knockoutów), wyłączając geny, by sprawdzić, które z nich pomagają guzom opierać się atakowi immunologicznemu. Te badania zmapowały wiele dróg ucieczki, ale nie pokazały, jak popchnąć komórki nowotworowe w przeciwną stronę — ku większej wrażliwości na limfocyty T — przy użyciu narzędzi takich jak leki oparte na RNA, które zwiększają lub wzmacniają aktywność genów zamiast je usuwać.
Przeszukiwanie tysięcy genów w poszukiwaniu ukrytych słabych punktów
Badacze zastosowali aktywację CRISPR, technologię działającą jak programowalny regulator głośności genów, by systematycznie zwiększyć aktywność prawie 3 000 genów w komórkach czerniaka, równocześnie wystawiając je na działanie limfocytów T zaprojektowanych do rozpoznawania wspólnego antygenu nowotworowego. Śledząc, które zmiany genetyczne powodowały częstsze lub rzadsze śmierci komórek nowotworowych, zidentyfikowali dwie główne grupy: geny „oporności”, które chroniły komórki nowotworowe, oraz geny „uczulenia”, które czyniły je znacznie łatwiejszym celem dla limfocytów T. Do genów uczulających należały znane elementy ścieżek śmierci komórkowej, takie jak CASP3 i BID, a także mniej oczywiste regulatory obróbki RNA i organizacji 3D genomu, jak SAFB i TSPYL2, oraz cząsteczki sygnalizacyjne typu Wnt. Testy pojedynczych trafień potwierdziły, że zwiększenie aktywności tych genów może albo chronić komórki nowotworowe, albo przygotować je do zniszczenia, także w różnych typach nowotworów i w komórkach zakażonych wirusami onkogennymi.
Syntetyczna śmiertelność oparta na RNA: groźne tylko na celowniku
Centralna koncepcja wyłaniająca się z pracy to „immunologiczna syntetyczna śmiertelność oparta na RNA”. Niektóre geny, jak CASP3, nie są szczególnie szkodliwe, gdy są nadekspresjonowane w komórkach nowotworowych rosnących samotnie. Jednak w momencie zaangażowania limfocytów T, dodatkowe białko CASP3 jest szybko aktywowane z formy uśpionej do potężnego wykonawcy uruchamiającego apoptozę — zaprogramowaną śmierć komórkową. Zespół wykazał, że dostarczenie RNA CASP3 do komórek nowotworowych nie hamowało ich wzrostu w izolacji, ale znacząco zwiększało zabijanie przez limfocyty T, a blokada aktywności kaspaz mogła uratować te komórki. Inne geny, jak SAFB, zachowywały się jeszcze selektywniej: zwiększenie SAFB ledwie zmieniało codzienny transkryptom komórki nowotworowej, a mimo to dramatycznie wzmagało zabijanie specyficznie przez szlak granzyme–perforin używany przez limfocyty T, pozostawiając odpowiedzi na powszechne czynniki zapalne w dużej mierze nietknięte.
Zaglądając do guzów komórka po komórce
Aby zrozumieć, jak działają te geny uczulające i oporności w rzeczywistej tkance, autorzy połączyli aktywację CRISPR z Perturb-seq, wysokoprzepustową metodą odczytującą profile RNA i perturbacje genetyczne tysięcy pojedynczych komórek jednocześnie. Następnie rozszerzyli to do „in situ Perturb-seq”, które wykrywa znaczniki perturbacji i aktywność genów bezpośrednio w niezmienionych plasterkach guza z rozdzielczością pojedynczych komórek. Te przestrzenne mapy ujawniły sieci genów, które guzy przejmują, by przetrwać atak limfocytów T, w tym węzły obejmujące składniki macierzy pozakomórkowej i receptory powierzchniowe. Odkryto też, jak perturbacje w komórkach nowotworowych przekształcają pobliskie komórki odpornościowe i zrębowe. Na przykład komórki nowotworowe zmuszone do nadekspresji niektórych ligandów Wnt były otoczone limfocytami T w bardziej aktywowanym stanie, a doświadczenia laboratoryjne potwierdziły, że rozpuszczalny Wnt3a może wzmocnić zabijanie ludzkich limfocytów T i produkcję cytokin.
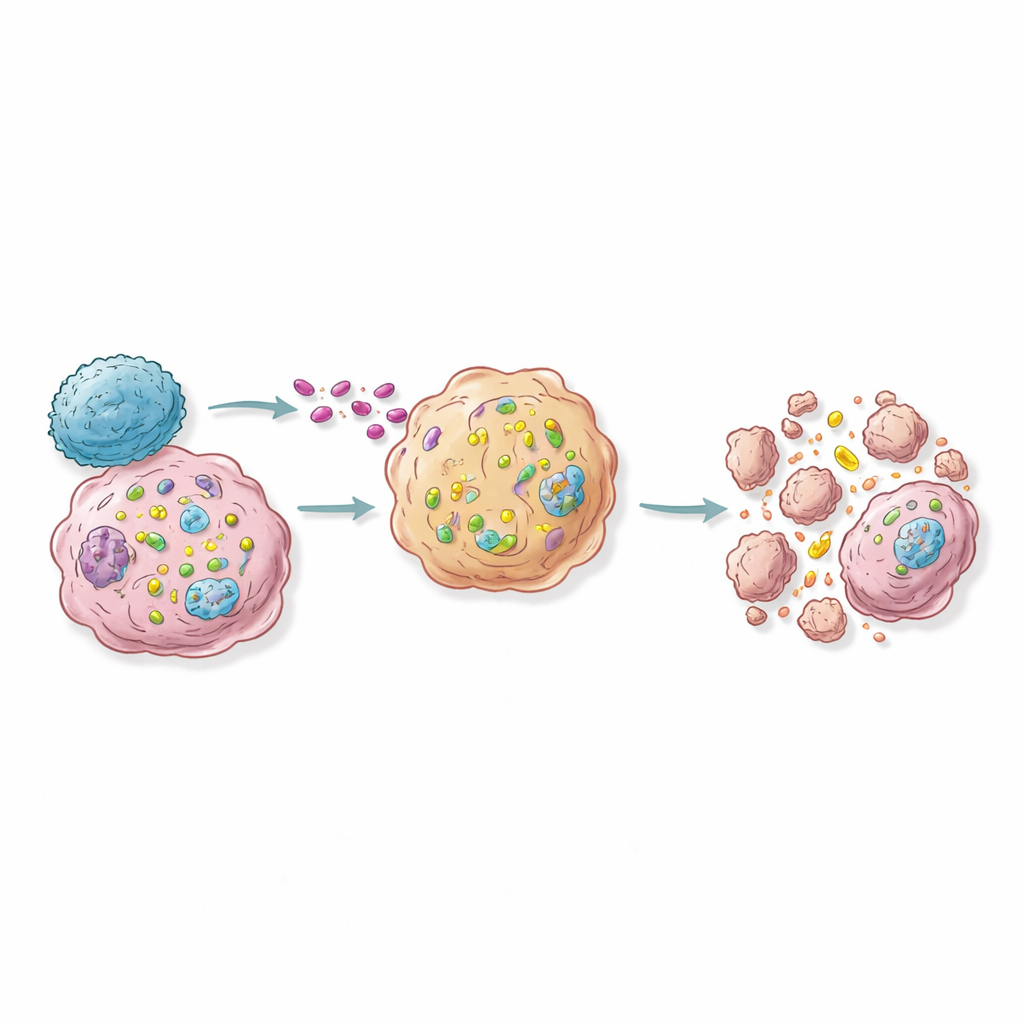
Od map genów do przyszłych immunoterapii RNA
W modelach mysich aktywacja garstki najlepszych genów „uczulających” w zaledwie ułamku komórek guza wystarczyła, by spowolnić lub nawet zapobiec wzrostowi guza oraz powiększyć pobliskie węzły chłonne wypełnione komórkami odpornościowymi, co wskazuje na efekt fali wykraczający poza zmodyfikowane komórki. Badanie sugeruje mapę drogową dla terapii następnej generacji: dostarczać cząsteczki RNA lub konstrukt aktywujący geny, które selektywnie podnoszą aktywność kluczowych genów uczulających w guzach, albo inżynierować terapeutyczne limfocyty T, by wykorzystywały te szlaki. Dla czytelnika niezwiązanego z tematem kluczowa myśl jest taka, że naukowcy uczą się przestawiać wewnętrzne okablowanie komórek nowotworowych, tak aby, gdy nadejdą własne limfocyty T organizmu, te komórki były wewnętrznie podminowane. Zamiast szeroko wzmacniać odporność — co może powodować poważne skutki uboczne — ta strategia ma na celu sprawić, by tylko niebezpieczne komórki stały się śmiertelnie wrażliwe na precyzyjny atak immunologiczny.
Cytowanie: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Słowa kluczowe: immunoterapia raka, zabijanie przez limfocyty T, aktywacja CRISPR, terapie oparte na RNA, syntetyczna śmiertelność