Clear Sky Science · it
Schermi ad alta risoluzione CRISPR di attivazione identificano meccanismi letali sintetici basati su RNA per rendere le cellule tumorali sensibili alla citotossicità mirata delle cellule T
Riattivare gli assassini naturali del corpo contro il cancro
Il nostro sistema immunitario dispone di “cellule assassine” professioniste chiamate cellule T, in grado di riconoscere e uccidere le cellule tumorali con notevole precisione. Tuttavia molti tumori imparano a schivare questi attacchi, attenuando l’efficacia delle immunoterapie odierne. Questo studio esplora un’idea emergente: invece di limitarsi a bloccare i geni che aiutano il cancro a sfuggire, cosa succederebbe se potessimo attivare specifici messaggi RNA all’interno delle cellule tumorali per renderle estremamente vulnerabili all’attacco delle cellule T—lasciando in gran parte risparmiate le cellule sane?
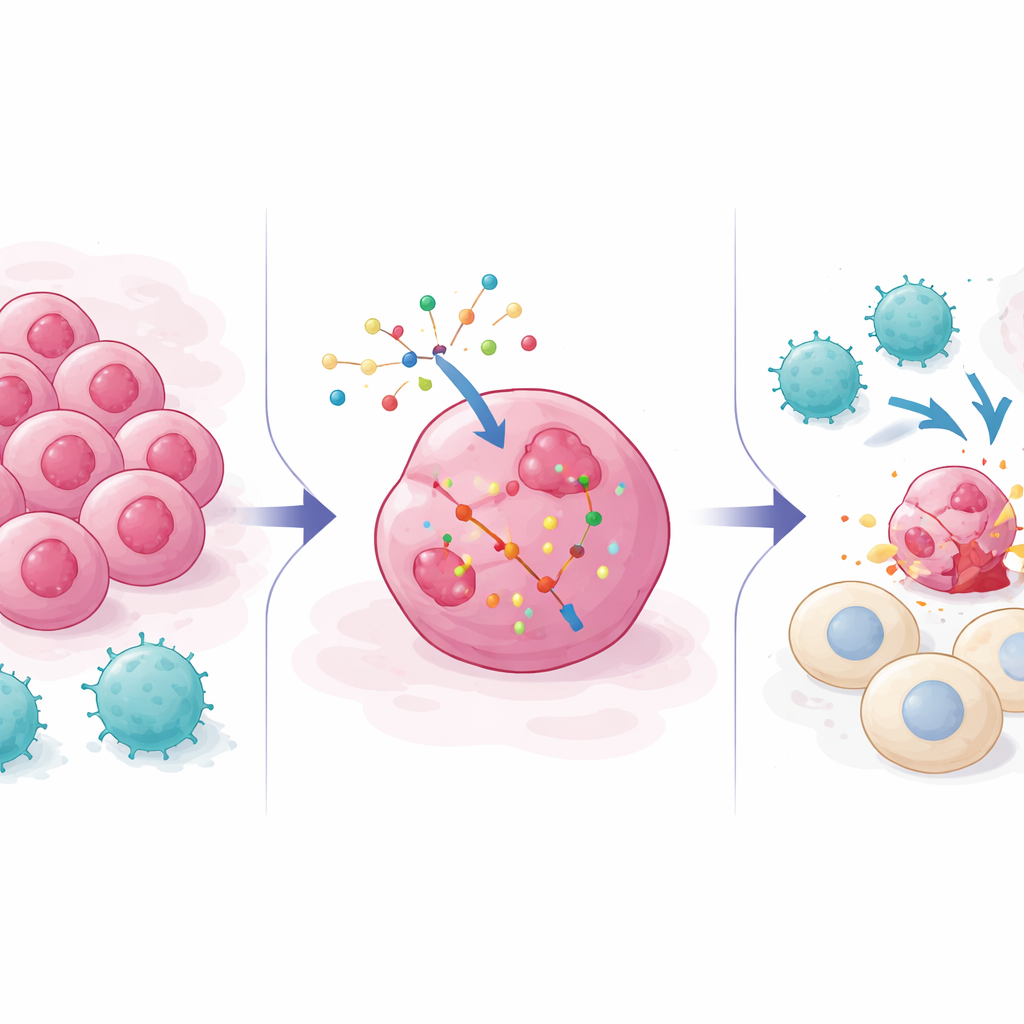
Perché le cellule tumorali sfuggono alla squadra d’assalto immunitaria
I trattamenti anticancro moderni, dagli inibitori dei checkpoint alle terapie con cellule T ingegnerizzate, si basano in larga misura sulle cellule T CD8 che riconoscono molecole caratteristiche sulle cellule tumorali e le uccidono. Ma i tumori spesso si adattano: possono nascondere proprio i marcatori che le cellule T cercano, attenuare segnali d’allarme come gli interferoni o aumentare percorsi di sopravvivenza che bloccano la morte cellulare. I precedenti criblaggi genetici hanno usato principalmente “knockout”, spegnendo i geni per vedere quali aiutano i tumori a resistere all’attacco immunitario. Quegli sforzi hanno mappato molte vie di fuga ma non hanno mostrato come spingere le cellule tumorali nella direzione opposta—verso una maggiore sensibilità alle cellule T—usando strumenti come farmaci a base di RNA che aggiungono o potenziano l’attività genica anziché rimuoverla.
Scansionare migliaia di geni alla ricerca di punti deboli nascosti
I ricercatori hanno usato l’attivazione CRISPR, una tecnologia che funziona come una manopola programmabile del volume per i geni, per aumentare sistematicamente l’espressione di quasi 3.000 geni in cellule di melanoma mentre le esponevano a cellule T ingegnerizzate per riconoscere un antigene tumorale comune. Monitorando quali cambiamenti genetici facevano morire le cellule tumorali più o meno frequentemente, hanno identificato due gruppi principali: geni di “resistenza” che proteggevano le cellule tumorali e geni “sensibilizzanti” che le rendevano molto più facili da uccidere per le cellule T. Tra i geni sensibilizzanti figuravano noti mediatori della morte cellulare come CASP3 e BID, oltre a regolatori meno ovvi del processamento dell’RNA e dell’organizzazione 3D del genoma, come SAFB e TSPYL2, e molecole di segnalazione come ligandi Wnt. La verifica di singoli bersagli ha confermato che aumentare l’espressione di questi geni poteva sia proteggere le cellule tumorali sia predisporle alla distruzione, persino in diversi tipi di cancro e in cellule infettate da virus oncogeni.
Lethalità sintetica basata su RNA: pericolosa solo nel mirino
Un concetto centrale emerso dal lavoro è la “letalità sintetica immunitaria basata su RNA”. Alcuni geni, come CASP3, non sono particolarmente dannosi quando sovraespressi in cellule tumorali che crescono isolatamente. Tuttavia, una volta che le cellule T interagiscono con i loro bersagli, l’eccesso di proteina CASP3 viene rapidamente convertito da una forma dormiente in un potente esecutore che guida l’apoptosi—la via di morte cellulare programmata. Il team ha dimostrato che fornire RNA di CASP3 alle cellule tumorali non comprometteva la loro crescita in isolamento ma aumentava notevolmente l’uccisione mediata dalle cellule T, e che bloccare l’attività delle caspasi poteva salvare queste cellule. Altri geni come SAFB si comportavano in modo ancora più selettivo: aumentare SAFB cambiava di poco il trascrittoma quotidiano della cellula tumorale, ma potenziava in modo drammatico l’uccisione specificamente attraverso la via granzyme–perforina usata dalle cellule T, lasciando per lo più intatte le risposte a molecole infiammatorie comuni.
Osservare i tumori una cellula alla volta
Per capire come questi geni sensibilizzanti e di resistenza funzionano nel tessuto reale, gli autori hanno combinato l’attivazione CRISPR con Perturb-seq, un metodo ad alto rendimento che legge i profili di RNA e le perturbazioni genetiche di migliaia di singole cellule contemporaneamente. Hanno poi esteso questo approccio all’“in situ Perturb-seq”, che rileva i codici a barre delle perturbazioni e l’attività genica direttamente in fette tumorali intatte con risoluzione a cellula singola. Queste mappe spaziali hanno rivelato reti di geni che i tumori cooptano per sopravvivere all’attacco delle cellule T, inclusi nodi che coinvolgono componenti della matrice extracellulare e recettori di superficie. Hanno anche messo in luce come le perturbazioni nelle cellule tumorali rimodellano le cellule immunitarie e stromali vicine. Per esempio, le cellule tumorali costrette a sovraesprimere certi ligandi Wnt erano circondate da cellule T in uno stato più attivato, e esperimenti di laboratorio hanno confermato che il Wnt3a solubile poteva potenziare l’uccisione e la produzione di citochine delle cellule T umane.
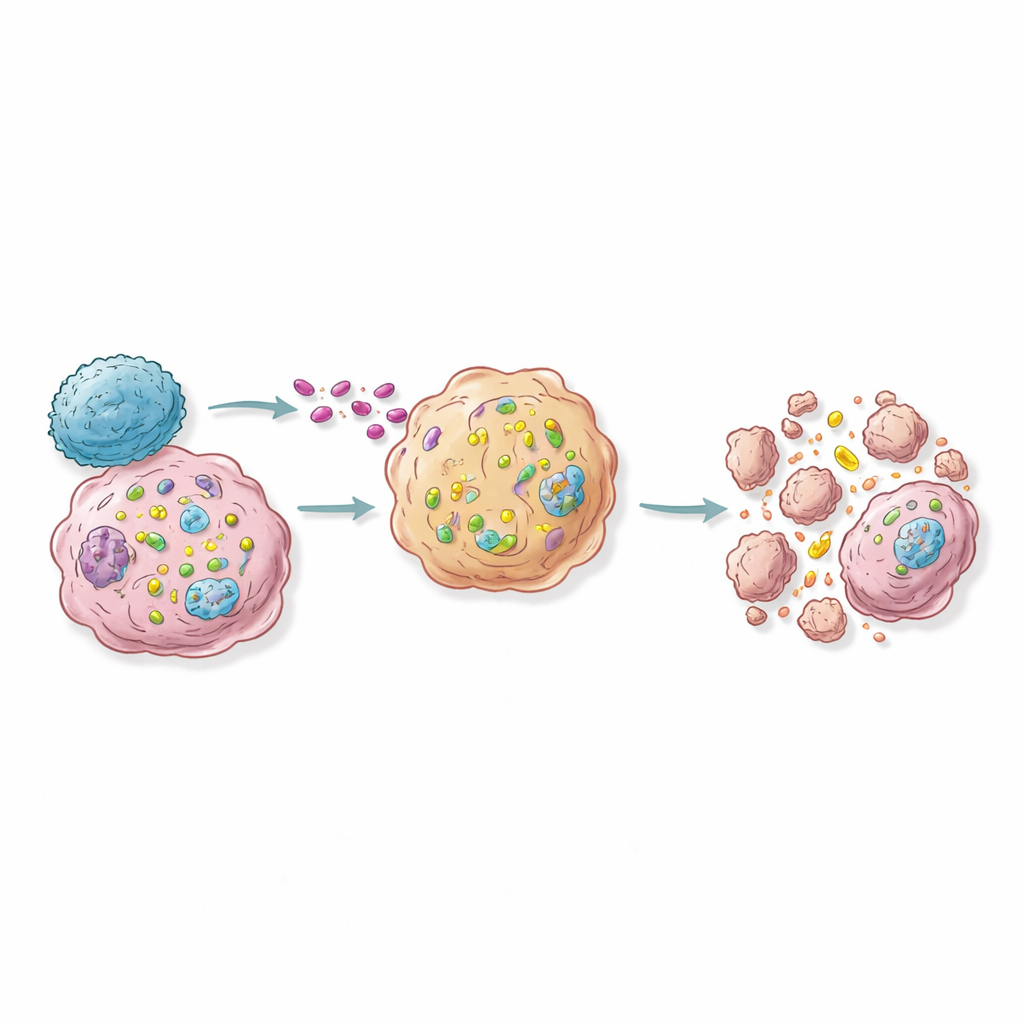
Dalle mappe geniche alle future immunoterapie a base di RNA
Nei modelli murini, attivare un piccolo numero dei principali geni “sensibilizzanti” in solo una frazione delle cellule tumorali è stato sufficiente a rallentare o perfino prevenire la crescita tumorale e ad ingrandire i linfonodi vicini pieni di cellule immunitarie, indicando un effetto a catena oltre le cellule modificate. Lo studio suggerisce una tabella di marcia per terapie di nuova generazione: fornire molecole di RNA o costrutti che attivano geni che aumentino selettivamente l’attività dei principali geni sensibilizzanti nei tumori, o ingegnerizzare cellule T terapeutiche per sfruttare queste vie. Per il lettore non specialista, la conclusione è che gli scienziati stanno imparando a riconfigurare le cellule tumorali in modo che, quando arrivano le cellule T del corpo, quelle cellule diventino trappole mortali dall’interno. Piuttosto che potenziare l’immunità in modo ampio—azione che può causare effetti collaterali gravi—questa strategia mira a rendere fatali alla giusta mira solo le cellule pericolose.
Citazione: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Parole chiave: immunoterapia del cancro, uccisione da parte delle cellule T, attivazione CRISPR, terapici a base di RNA, letalità sintetica