Clear Sky Science · nl
High-content CRISPR-activatieschermen identificeren synthetisch dodelijke RNA-gebaseerde mechanismen om kankercellen gevoeliger te maken voor gerichte T-celcytotoxiciteit
De lijfelijke sluipmoordenaars opnieuw op kanker richten
Ons immuunsysteem beschikt over gespecialiseerde “moordcellen” genaamd T-cellen die kankercellen met opmerkelijke precisie kunnen herkennen en doden. Toch leren veel tumoren deze aanvallen te ontwijken, waardoor de effectiviteit van hedendaagse immunotherapieën vermindert. Deze studie onderzoekt een opkomend idee: in plaats van alleen genen te blokkeren die kanker helpen ontkomen, wat als we specifieke RNA-boodschappen binnen kankercellen konden inschakelen om ze uitermate vatbaar te maken voor T-celaanvallen—terwijl gezonde cellen grotendeels gespaard blijven?
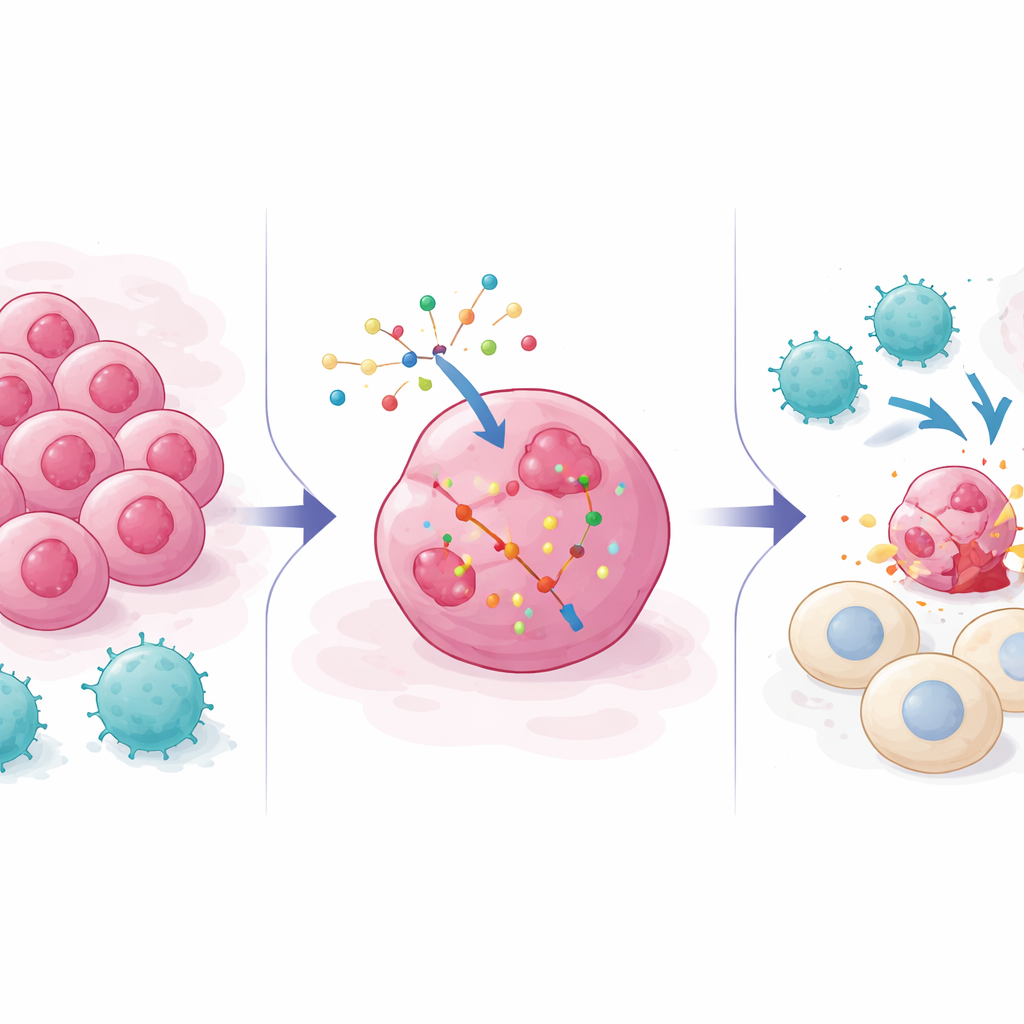
Waarom kankercellen het immuunkorps ontlopen
Moderne kankerbehandelingen, van checkpointremmers tot ontworpen T-celtherapieën, vertrouwen sterk op CD8 T-cellen die kenmerkende moleculen op tumorcellen herkennen en deze vervolgens doden. Maar tumoren passen zich vaak aan: ze kunnen de markers verbergen waar T-cellen naar zoeken, alarmsignalen zoals interferonen dempen, of overlevingsroutes opvoeren die celdood blokkeren. Eerdere genetische schermen gebruikten meestal “knock-outs”, waarbij genen werden uitgeschakeld om te zien welke genen tumoren beschermen tegen immuunaanvallen. Die inspanningen brachten veel ontsnappingsroutes in kaart, maar lieten niet zien hoe je kankercellen in de tegenovergestelde richting kunt duwen—naar grotere gevoeligheid voor T-cellen—met hulpmiddelen zoals RNA-gebaseerde geneesmiddelen die genactiviteit toevoegen of versterken in plaats van verwijderen.
Duisenden genen scannen op verborgen zwakke plekken
De onderzoekers gebruikten CRISPR-activatie, een technologie die werkt als een programmeerbare volumeknop voor genen, om systematisch bijna 3.000 genen in melanomacellen op te voeren terwijl ze werden blootgesteld aan T-cellen die zo waren ontworpen dat ze een gedeeld tumorantigeen herkennen. Door bij te houden welke genetische veranderingen ervoor zorgden dat kankercellen vaker of juist minder vaak stierven, identificeerden ze twee hoofdgroepen: “resistentiegenen” die kankercellen beschermden, en “sensibiliserende” genen die ze veel makkelijker door T-cellen te doden maakten. Tot de sensibiliserende genen behoorden bekende spelers in celdood zoals CASP3 en BID, maar ook minder voor de hand liggende regelaars van RNA-verwerking en 3D-genoomorganisatie, zoals SAFB en TSPYL2, en signaalmoleculen zoals Wnt-liganden. Tests van individuele hits bevestigden dat het opschroeven van deze genen kankercellen ofwel kon afschermen ofwel kon voorbereiden op vernietiging, zelfs in verschillende kankersoorten en in cellen geïnfecteerd met kankerveroorzakende virussen.
RNA-gebaseerde synthetische lethality: alleen dodelijk in de vuurlijn
Een centraal concept dat uit het werk naar voren komt is “immuun RNA-gebaseerde synthetische lethality.” Sommige genen, zoals CASP3, zijn niet bijzonder schadelijk als ze overgeëxpresseerd worden in kankercellen die alleen groeien. Zodra T-cellen echter hun doelwit aanspreken, wordt het extra CASP3-eiwit snel omgezet van een inactieve vorm in een krachtige uitvoerder die apoptose aanjaagt—het geprogrammeerde celdoodpad. Het team toonde aan dat het afleveren van CASP3-RNA in tumorcellen hun groei in isolatie niet aantastte, maar de door T-cellen gemedieerde doding aanzienlijk versterkte, en dat het blokkeren van caspase-activiteit deze cellen kon redden. Andere genen zoals SAFB gedroegen zich nog selectiever: het opvoeren van SAFB veranderde het dagelijkse transcriptoom van de kankercel nauwelijks, maar vergrootte dramatisch de doding specifiek via het granzyme–perforinepad dat T-cellen gebruiken, terwijl reacties op gangbare ontstekingsmoleculen grotendeels onaangetast bleven.
In tumoren kijken, één cel tegelijk
Om te begrijpen hoe deze sensibiliserende en resistente genen in echt weefsel werken, combineerden de auteurs CRISPR-activatie met Perturb-seq, een hoogdoorvoer methode die de RNA-profielen en genetische perturbaties van duizenden individuele cellen tegelijk uitleest. Ze breidden dit vervolgens uit naar “in situ Perturb-seq”, die perturbatie-barcodes en genactiviteit direct in intacte tumorstukken op enkelcelsresolutie detecteert. Deze ruimtelijke kaarten onthulden netwerken van genen die tumoren aanwenden om T-celaanvallen te overleven, inclusief knooppunten met extracellulaire matrixcomponenten en celoppervlaktereceptoren. Ze toonden ook hoe perturbaties in kankercellen nabije immuun- en stromale cellen herschikken. Bijvoorbeeld, kankercellen die gedwongen werden bepaalde Wnt-liganden te overexpressen, werden omringd door T-cellen in een meer geactiveerde toestand, en laboratoriumexperimenten bevestigden dat oplosbare Wnt3a menselijke T-celdoding en cytokineproductie kon versterken.
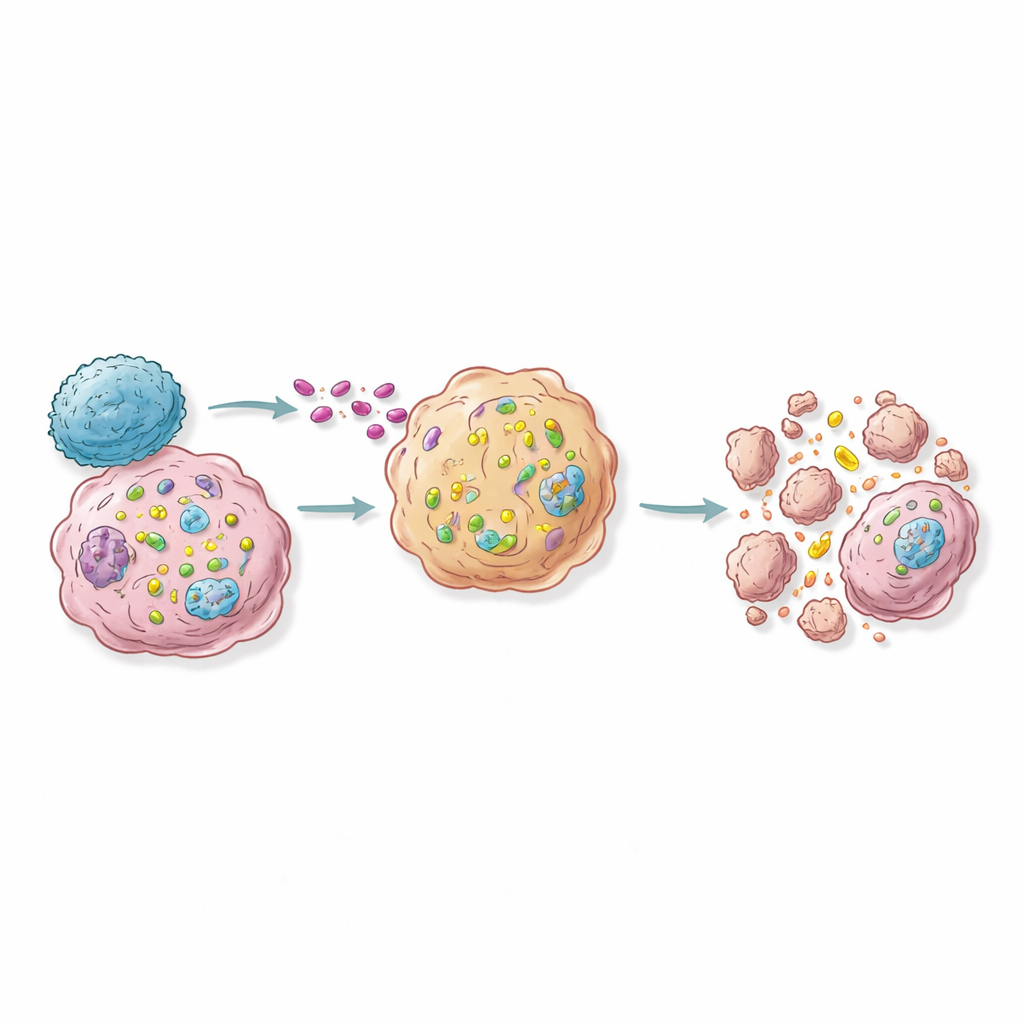
Van genkaarten naar toekomstige RNA-immunotherapieën
In muismodellen was het activeren van een handvol top-“sensibiliserende” genen in slechts een fractie van de tumorcellen voldoende om de tumorgroei te vertragen of zelfs te voorkomen en om nabijgelegen lymfeklieren gevuld met immuuncellen te vergroten, wat wijst op een rimpeleffect voorbij de gewijzigde cellen. De studie suggereert een routekaart voor next-generation therapieën: lever RNA-moleculen of gen-activatieconstructen die selectief de activiteit van sleutel-sensibiliserende genen in tumoren verhogen, of ontwerp therapeutische T-cellen om deze paden uit te buiten. Voor de leek is de conclusie dat wetenschappers leren hoe ze kankercellen zo kunnen herbedraden dat, wanneer de eigen T-cellen van het lichaam arriveren, die cellen van binnenuit geactiveerde valstrikken worden. In plaats van het immuunsysteem algemeen op te voeren—wat ernstige bijwerkingen kan veroorzaken—streeft deze strategie ernaar alleen de gevaarlijke cellen dodelijk gevoelig te maken voor een precieze immuunaanval.
Bronvermelding: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Trefwoorden: kankerimmunotherapie, T-celdoding, CRISPR-activatie, RNA-therapeutica, synthetische lethality