Clear Sky Science · ar
شاشات تنشيط CRISPR عالية المحتوى تكشف آليات مميتة تركيبياً معتمدة على الحمض النووي الريبي لتحسس الخلايا السرطانية لسُمّية الخلايا التائية المستهدفة
إعادة تشغيل قاتلي الجسم ضد السرطان
الجهاز المناعي مزود بخلايا «قتّالة» متخصصة تُسمى الخلايا التائية قادرة على التعرف على الخلايا السرطانية وقتلها بدقة ملحوظة. ومع ذلك تتعلم العديد من الأورام التهرُّب من هذه الهجمات، مما يضعف فعالية علاجات المناعة الحالية. تستكشف هذه الدراسة فكرة ناشئة: بدلاً من حصر النهج في حجب الجينات التي تساعد السرطان على الهروب، ماذا لو استطعنا تفعيل رسائل حمض نووي ريبي محددة داخل الخلايا السرطانية لجعلها حساسة للغاية لهجوم الخلايا التائية — مع ترك الخلايا السليمة إلى حد كبير دون أذى؟
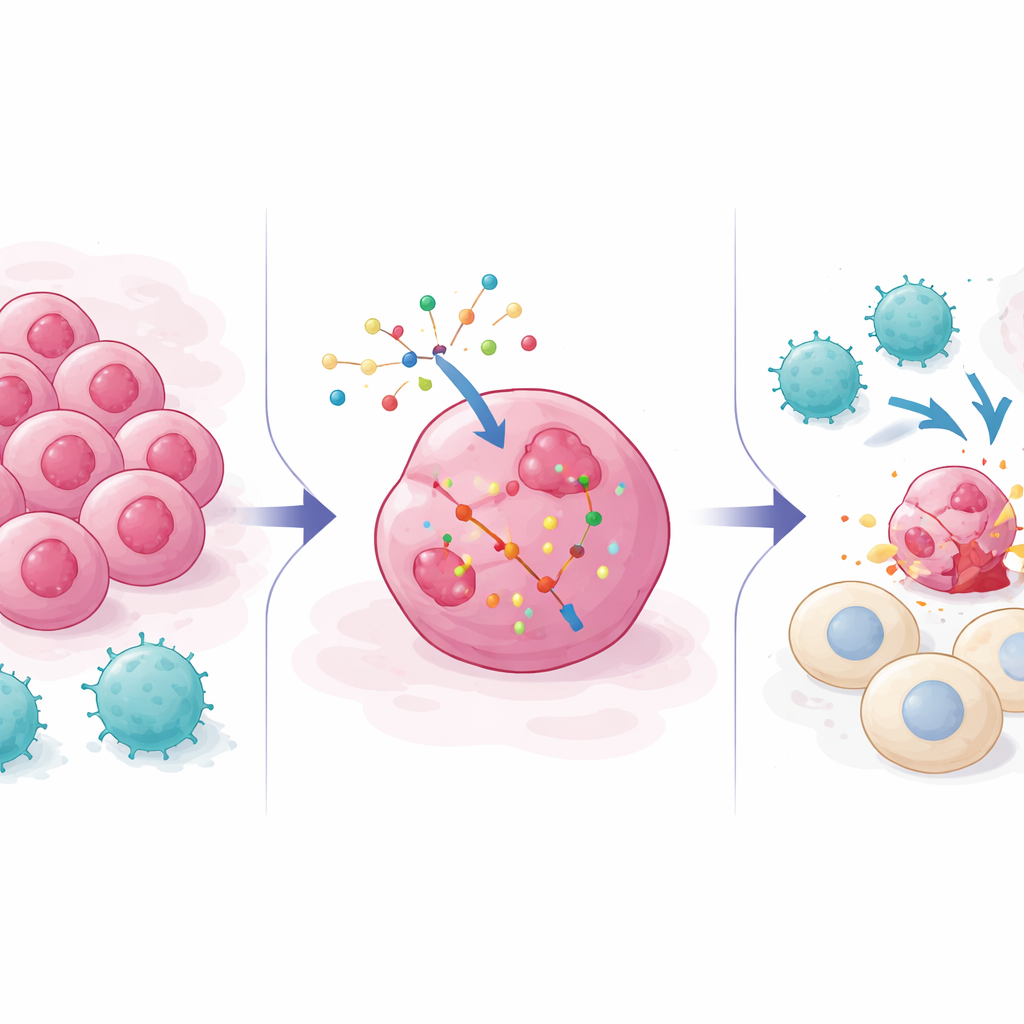
لماذا تهرب الخلايا السرطانية من فرقة الاغتيال المناعية
تعتمد علاجات السرطان الحديثة، من مثبِّطات نقاط التفتيش إلى علاجات الخلايا التائية المهندسة، بشكل كبير على الخلايا التائية CD8 التي تتعرف على جزيئات مميزة على الخلايا الورمية ثم تقتلها. لكن الأورام غالباً ما تتكيّف: يمكنها إخفاء العلامات التي تبحث عنها الخلايا التائية، أو كتم إشارات التنبيه مثل الإنترفيرونات، أو رفع مسارات بقاء تعيق موت الخلية. كانت الشاشات الجينية السابقة تستخدم في الغالب «إيقاف الجينات» لرؤية أيها يساعد الأورام على مقاومة الهجوم المناعي. هذه الجهود رسمت كثيراً من طرق الهروب لكنها لم تُظهِر كيف يمكن دفع الخلايا السرطانية في الاتجاه المعاكس—نحو حساسية أكبر للخلايا التائية—باستخدام أدوات مثل أدوية قائمة على الحمض النووي الريبي التي تضيف أو تعزز نشاط الجينات بدلاً من إزالتها.
مسح آلاف الجينات بحثاً عن نقاط ضعف مخفية
استخدم الباحثون تنشيط CRISPR، وهي تكنولوجيا تعمل مثل مقبض صوت برمجي للجينات، لرفع مستوى نحو 3000 جين في خلايا الميلانوما أثناء تعريضها لخلايا تائية مهندسة تتعرف على مستضد ورمي مشترك. من خلال تتبع التغيرات الجينية التي جعلت الخلايا السرطانية تموت أكثر أو أقل، عرّفوا مجموعتين رئيسيتين: جينات «المقاومة» التي تحمي الخلايا السرطانية، وجينات «التحسس» التي تجعلها أسهل بكثير لقتل الخلايا التائية. شملت جينات التحسس عوامل معروفة للموت الخلوي مثل CASP3 وBID، بالإضافة إلى منظمات أقل وضوحاً في معالجة الـRNA وتنظيم الجينوم ثلاثي الأبعاد، مثل SAFB وTSPYL2، وجزيئات إشارية مثل ليغاندات Wnt. أكدت اختبارات النَّتائج الفردية أن رفع هذه الجينات يمكن أن يقي الخلايا السرطانية أو يهيئها للتدمير، حتى في أنواع سرطانات مختلفة وفي خلايا مصابة بفيروسات ممرِضة للسرطان.
الفتك التركيبي المعتمد على الحمض النووي الريبي: خطر يظهر فقط تحت القصف
مفهوم محوري ظهر من العمل هو «الفتك التركيبي المناعي المعتمد على RNA». بعض الجينات، مثل CASP3، لا تكون ضارة بشكل خاص عند الإفراط في التعبير عنها في خلايا سرطانية تنمو بمفردها. ومع ذلك، بمجرد أن تتفاعل الخلايا التائية مع أهدافها، يتحول بروتين CASP3 الإضافي بسرعة من شكل خامد إلى منفذ قوي يقود الاستماتة—مسار موت الخلية المبرمج. أظهر الفريق أن إيصال RNA لـCASP3 إلى الخلايا الورمية لم يعيق نموها في عزلة لكنه عزز بشكل ملحوظ القتل الوسيط بالخلايا التائية، وأن حجب نشاط الكاسبازات يمكن أن ينقذ هذه الخلايا. تصرفت جينات أخرى مثل SAFB بانتقائية أكبر: رفع SAFB غيّر قليلاً النسق اليومي للرواسب الجينية للخلايا السرطانية، ومع ذلك عزز القتل بدرجة كبيرة وبشكل خاص عبر مسار الغرانزيم–بِرفورِن الذي تستخدمه الخلايا التائية، بينما ترك الاستجابات للجزيئات الالتهابية الشائعة إلى حد كبير دون تغيير.
التطلع داخل الأورام خلية خلية
لفهم كيف تعمل هذه الجينات المحسسة والمقاومة في الأنسجة الحقيقية، جمع المؤلفون بين تنشيط CRISPR وPerturb-seq، وهي طريقة عالية الإنتاجية تقرأ ملفات RNA والاضطرابات الجينية لآلاف الخلايا الفردية دفعة واحدة. ثم مددوا ذلك إلى «Perturb-seq في الموقع»، التي تكشف شفرات الاضطراب ونشاط الجينات مباشرة في شرائح الورم السليمة على مستوى خلية مفردة. كشفت هذه الخرائط المكانية شبكات من الجينات التي تستغلها الأورام للبقاء أمام هجوم الخلايا التائية، بما في ذلك محاور تشمل مكونات المصفوفة خارج الخلوية ومستقبلات سطح الخلية. كما كشفت كيف تعيد اضطرابات الخلايا السرطانية تشكيل الخلايا المناعية والطرابية القريبة. على سبيل المثال، كانت الخلايا السرطانية التي جُبرت على الإفراط في التعبير عن بعض ليغاندات Wnt محاطة بخلايا تائية في حالة مفعَّلة أكثر، وأكدت التجارب المختبرية أن Wnt3a القابلة للذوبان يمكن أن تضاعف قتل الخلايا التائية البشرية وإنتاج السيتوكينات.
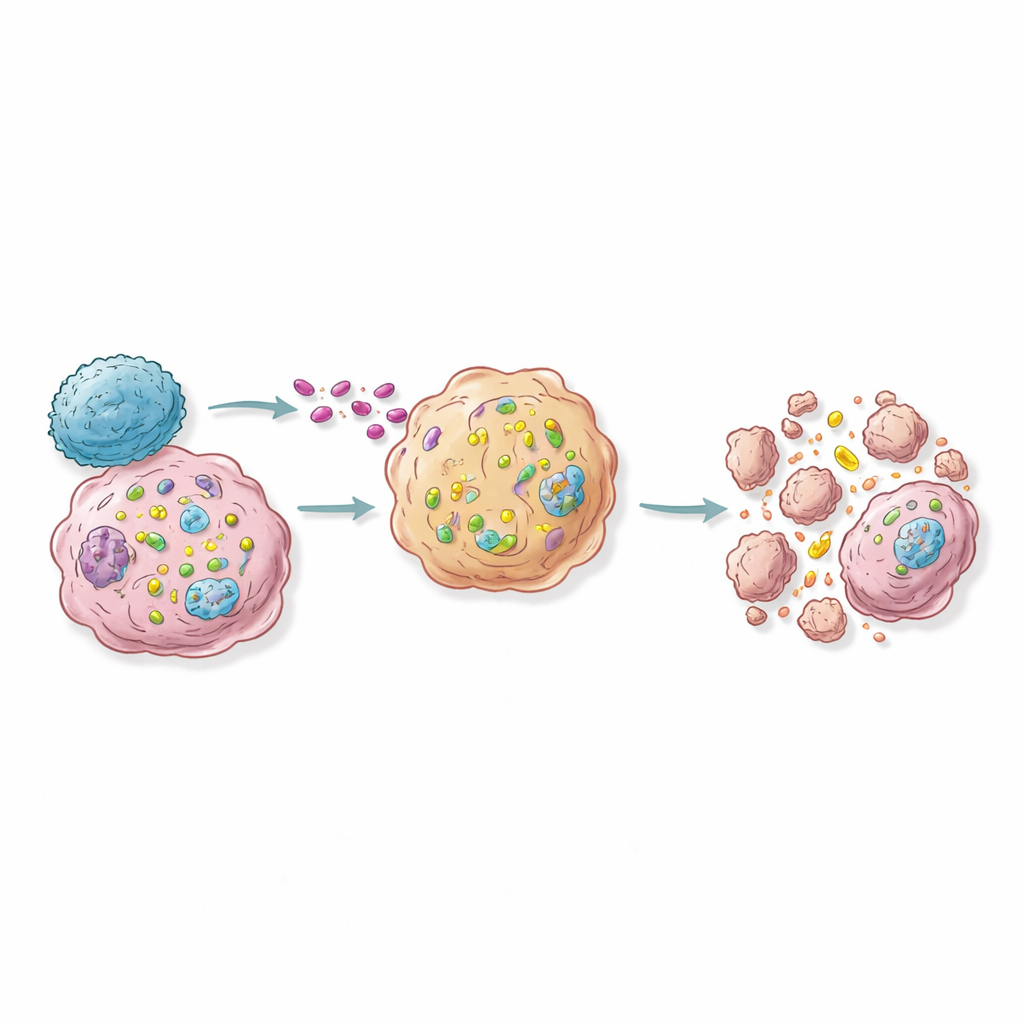
من خرائط الجينات إلى علاجات مناعية مستقبلية قائمة على الـRNA
في نماذج الفئران، كان تفعيل حفنة من جينات «التحسس» العليا في جزء بسيط فقط من خلايا الورم كافياً لإبطاء النمو أو حتى منعه ولتكبير العقد الليمفاوية القريبة المليئة بالخلايا المناعية، مما يشير إلى تأثير متسلسل يتجاوز الخلايا المعدلة. تقترح الدراسة خارطة طريق للعلاجات من الجيل القادم: إيصال جزيئات RNA أو بنى مفعلة للجينات ترفع بشكل انتقائي نشاط جينات التحسس الرئيسية في الأورام، أو هندسة خلايا تائية علاجية لاستغلال هذه المسارات. للخلاصة العامة، الدرس هو أن العلماء يتعلمون كيف يعيدون برمجة الخلايا السرطانية بحيث تصبح، عند وصول الخلايا التائية الطبيعية للجسم، منشأة مُحشوة بالفخاخ من الداخل. بدلاً من تعزيز المناعة على نطاق واسع—وهو ما قد يسبب آثاراً جانبية خطيرة—يهدف هذا النهج إلى جعل الخلايا الضارة فقط حساسة فتكياً لضربة مناعية دقيقة.
الاستشهاد: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
الكلمات المفتاحية: المناعة المناعية للسرطان, قتل الخلايا التائية, تنشيط CRISPR, علاجات قائمة على الحمض النووي الريبي, الفتك التركيبي