Clear Sky Science · fr
Des cribles CRISPR d’activation à haute teneur identifient des mécanismes synthétiquement létaux basés sur l’ARN pour sensibiliser les cellules cancéreuses à la cytotoxicité ciblée des cellules T
Rendre aux assassins du corps leur rôle contre le cancer
Notre système immunitaire comprend des « cellules tueuses » professionnelles appelées cellules T, capables de reconnaître et d’éliminer les cellules cancéreuses avec une précision remarquable. Pourtant, de nombreuses tumeurs apprennent à esquiver ces attaques, compromettant l’efficacité des immunothérapies actuelles. Cette étude explore une idée émergente : plutôt que de se contenter de bloquer des gènes qui permettent au cancer d’échapper à l’attaque, et si l’on pouvait activer des messages ARN spécifiques dans les cellules cancéreuses pour les rendre extrêmement vulnérables à l’action des cellules T — tout en épargnant en grande partie les cellules saines ?
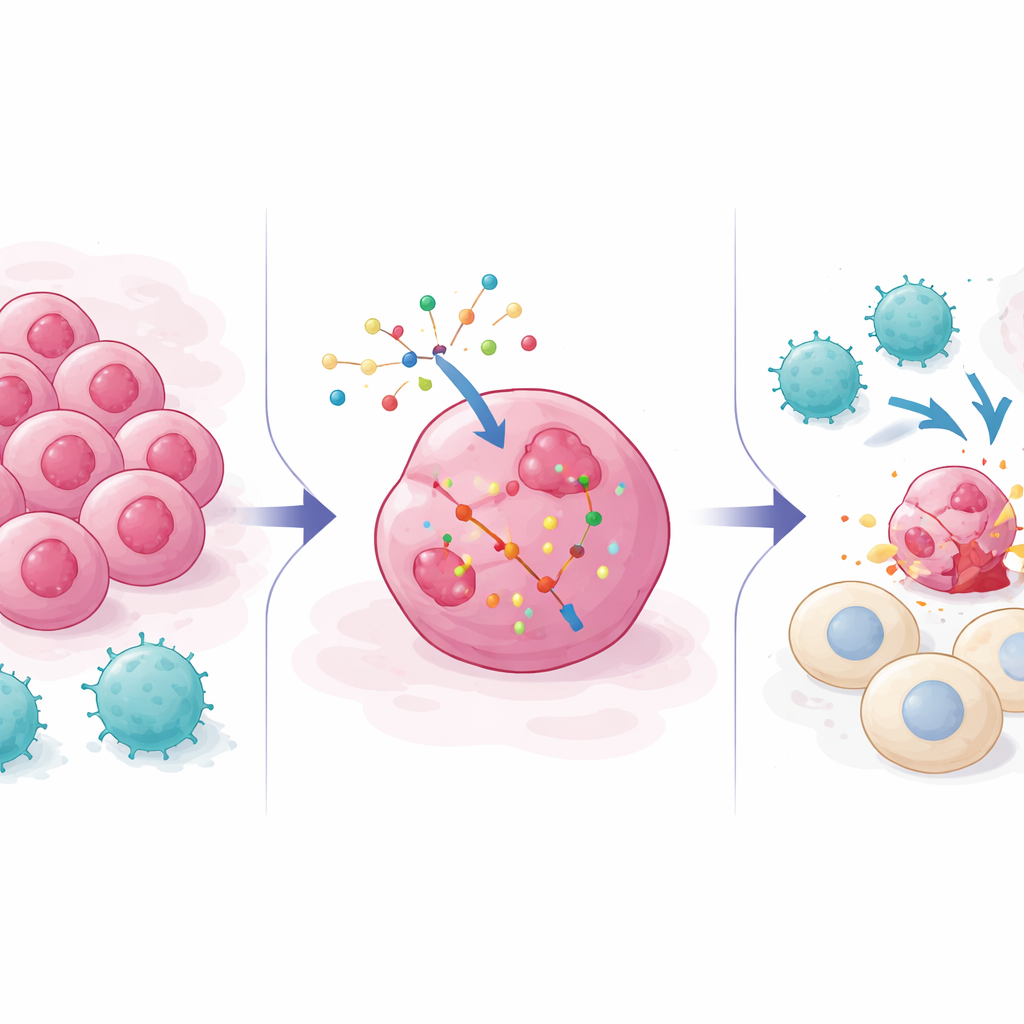
Pourquoi les cellules cancéreuses échappent à l’escouade d’assassins immunitaires
Les traitements modernes du cancer, des inhibiteurs de points de contrôle aux thérapies cellulaires T modifiées, reposent largement sur les cellules T CD8 qui reconnaissent des molécules caractéristiques à la surface des cellules tumorales puis les tuent. Mais les tumeurs s’adaptent souvent : elles peuvent dissimuler les marqueurs que recherchent les cellules T, atténuer les signaux d’alarme comme les interférons, ou activer des voies de survie qui empêchent la mort cellulaire. Les cribles génétiques précédents utilisaient principalement des « knockouts », éteignant des gènes pour voir lesquels aidaient les tumeurs à résister à l’attaque immunitaire. Ces travaux ont cartographié de nombreuses voies d’évasion mais n’ont pas montré comment pousser les cellules cancéreuses dans l’autre sens — vers une sensibilité accrue aux cellules T — en utilisant des outils comme des médicaments à base d’ARN qui ajoutent ou renforcent l’activité génique plutôt que de l’éliminer.
Scanner des milliers de gènes à la recherche de points faibles cachés
Les chercheurs ont utilisé l’activation CRISPR, une technologie qui fonctionne comme un bouton de volume programmable pour les gènes, afin d’augmenter systématiquement l’expression de près de 3 000 gènes dans des cellules de mélanome tout en les exposant à des cellules T modifiées pour reconnaître un antigène tumoral partagé. En suivant quels changements génétiques faisaient mourir les cellules cancéreuses plus ou moins souvent, ils ont identifié deux groupes principaux : des gènes de « résistance » qui protégeaient les cellules cancéreuses, et des gènes « sensibilisants » qui les rendaient beaucoup plus faciles à éliminer par les cellules T. Parmi les gènes sensibilisants figuraient des acteurs bien connus de la mort cellulaire comme CASP3 et BID, ainsi que des régulateurs moins évidents du traitement de l’ARN et de l’organisation 3D du génome, tels que SAFB et TSPYL2, et des molécules de signalisation comme les ligands Wnt. Le test des candidats individuels a confirmé que l’augmentation de l’expression de ces gènes pouvait soit protéger les cellules cancéreuses, soit les préparer à la destruction, y compris dans différents types de cancer et dans des cellules infectées par des virus oncogènes.
Létalité synthétique basée sur l’ARN : dangereuse seulement dans la ligne de mire
Un concept central issu de ce travail est la « létalité synthétique immunitaire basée sur l’ARN ». Certains gènes, comme CASP3, ne sont pas particulièrement nuisibles lorsqu’ils sont surexprimés dans des cellules cancéreuses isolées. Cependant, une fois que les cellules T engagent leurs cibles, la protéine CASP3 supplémentaire est rapidement activée, passant d’une forme dormante à un exécuteur puissant qui déclenche l’apoptose — la voie de mort cellulaire programmée. L’équipe a montré que l’apport d’ARN codant CASP3 dans les cellules tumorales n’altérait pas leur croissance en isolation mais augmentait nettement la destruction médiée par les cellules T, et que bloquer l’activité des caspases pouvait sauver ces cellules. D’autres gènes comme SAFB se comportaient de façon encore plus sélective : l’augmentation de SAFB modifiait à peine le transcriptome quotidien des cellules cancéreuses, mais amplifiait de façon spectaculaire l’élimination spécifiquement via la voie granzyme–perforine employée par les cellules T, tout en laissant globalement intactes les réponses aux molécules inflammatoires communes.
Observer les tumeurs une cellule à la fois
Pour comprendre comment ces gènes sensibilisants et de résistance fonctionnent dans un tissu réel, les auteurs ont combiné l’activation CRISPR avec le Perturb-seq, une méthode à haut débit qui lit les profils ARN et les perturbations génétiques de milliers de cellules individuelles simultanément. Ils ont ensuite étendu cela au « Perturb-seq in situ », qui détecte les codes-barres de perturbation et l’activité génique directement dans des tranches tumorales intactes avec résolution unicellulaire. Ces cartographies spatiales ont révélé des réseaux de gènes que les tumeurs détournent pour survivre à l’attaque des cellules T, incluant des nœuds impliquant des composants de la matrice extracellulaire et des récepteurs de surface cellulaire. Elles ont aussi montré comment les perturbations dans les cellules cancéreuses reconfigurent les cellules immunitaires et stromales voisines. Par exemple, des cellules cancéreuses forcées de surexprimer certains ligands Wnt étaient entourées de cellules T dans un état plus activé, et des expériences en laboratoire ont confirmé que la Wnt3a soluble pouvait renforcer fortement l’élimination par les cellules T humaines et la production de cytokines.
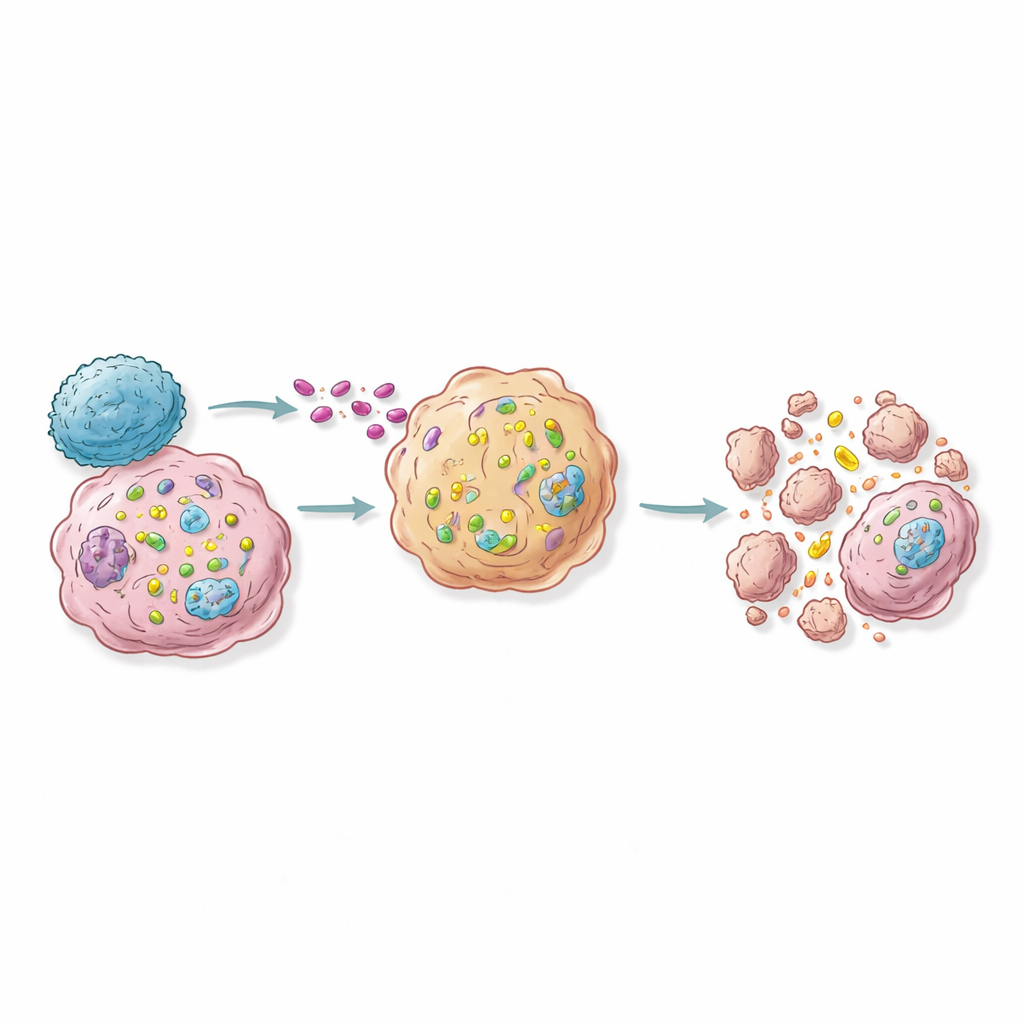
Des cartes géniques aux futures immunothérapies à base d’ARN
Chez la souris, l’activation d’une poignée de gènes « sensibilisants » prioritaires dans seulement une fraction des cellules tumorales suffisait à ralentir voire empêcher la croissance tumorale et à augmenter la taille des ganglions lymphatiques voisins remplis de cellules immunitaires, indiquant un effet de ruissellement au-delà des cellules modifiées. L’étude propose une feuille de route pour les thérapies de nouvelle génération : délivrer des molécules d’ARN ou des constructions activatrices de gènes qui augmentent sélectivement l’activité de gènes sensibilisants clés dans les tumeurs, ou concevoir des cellules T thérapeutiques pour exploiter ces voies. Pour un non-spécialiste, la conclusion est que les scientifiques apprennent à reprogrammer les cellules cancéreuses de sorte que, lorsque les propres cellules T de l’organisme arrivent, ces cellules deviennent piégées de l’intérieur. Plutôt que de stimuler l’immunité de façon globale — ce qui peut provoquer des effets indésirables graves — cette stratégie vise à rendre seulement les cellules dangereuses fatalement sensibles à une attaque immunitaire précise.
Citation: Akana, R.V., Yoe, J., Laveroni, O. et al. High-content CRISPR activation screens identify synthetically lethal RNA-based mechanisms to sensitize cancer cells to targeted T cell cytotoxicity. Nat Genet 58, 841–853 (2026). https://doi.org/10.1038/s41588-026-02561-7
Mots-clés: immunothérapie du cancer, cytotoxicité des cellules T, activation CRISPR, thérapeutiques à base d’ARN, létalité synthétique