Clear Sky Science · tr
Çok omik verilerle ortaya konan biallelik MRPL42 varyantı, birleşik oksidatif fosforilasyon yetmezliği sendromuna neden oluyor
Hücrenin Enerji Santralleri İşlevini Yitirdiğinde
Mitokondriler genellikle hücrelerimizin enerji santralleri olarak anılır; yakıtı, kalbin atmasını ve beynin çalışmasını sürdüren enerjiye sessizce dönüştürürler. Bu makale, ciddi hastalık geçiren bir yenidoğanın öyküsünü izliyor; araştırmacıların mitokondri içindeki protein üretim makinesinde küçük bir kusuru keşfetmesine yol açan olayları. Birkaç gelişmiş laboratuvar tekniğini birleştirerek, araştırmacılar tek bir kalıtsal değişikliğin hücresel enerji üretimini nasıl bozabildiğini ve ölümcül çoklu sistem hastalığına nasıl yol açtığını gösteriyorlar.
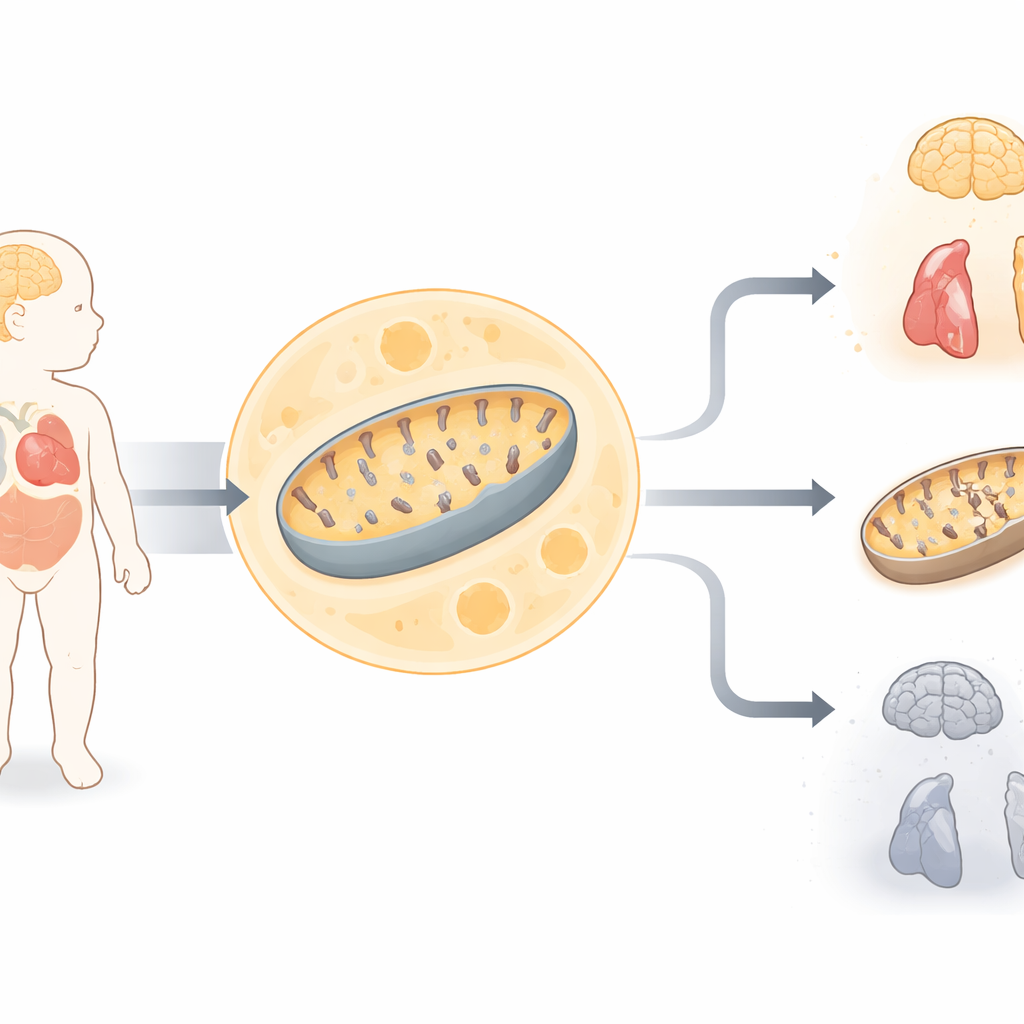
Ciddi Durumdaki Bir Yenidoğan
Çalışma, ilk bakışta normal görünen ancak hızla ağır tıbbi sorunlar geliştiren akraba ebeveynlerden doğan bir kız bebeğe odaklanıyor. Kasları zayıftı, solunum güçlüğü, nöbetler, işitme sorunları, kalpte değişiklikler ve kanda yüksek laktik asit seviyeleri vardı—hücrelerin enerji üretmede zorlandığını gösteren belirgin bir işaret. Beyin görüntülemeleri geniş çapta beyin dokusu kaybını ortaya koydu ve deri hücrelerinde yapılan testler, mitokondrilerindeki iki büyük enerji üreten enzim kompleksinin düşük performans gösterdiğini saptadı. Bu ipuçları, şiddetli bir mitokondriyal enerji metabolizması bozukluğuna işaret ediyordu, ancak doğum öncesi yapılan standart genetik testler bilinen bir neden bulamamıştı.
Gizli Bir Gen Hatası Arayışı
Rutin testlerin ötesine geçmek için ekip “çok‑omik” bir strateji kullandı—çocuğun hücrelerindeki DNA’yı, DNA’dan kopyalanan RNA mesajlarını ve tüm protein setini okudular. Tüm genom dizilemesi, mitokondri içindeki büyük protein yapım biriminin (ribozomun) küçük bir parçasını kodlayan MRPL42 adlı genin her iki kopyasında da nadir bir değişiklik ortaya koydu. Tek başına bu DNA değişikliği belirsiz sınıflandırıldı çünkü MRPL42 daha önce insan hastalığıyla ilişkilendirilmemişti. Ancak RNA dizilemesi, değişmiş gen mesajının büyük ölçüde hatalı parçalanmış olduğunu gösterdi: kritik bir bölüm moleküllerin yaklaşık beşte dördünde atlanmış, bu da okuma çerçevesinin kaymasına ve erken durma sinyaline yol açmıştı. Yalnızca az bir miktar normal mesaj ve dolayısıyla bir miktar normal protein hâlâ üretiliyordu.
Eksik Bir Parça Enerji Santralini Nasıl Zayıflatıyor
Hastanın deri hücrelerindeki protein ve görüntüleme çalışmaları, bu hatalı mesajın pratikte ne anlama geldiğini ortaya koydu. MRPL42 protein düzeyleri normalin yaklaşık dörtte birine düşmüş ve mitokondri ağı sağlıklı hücrelere göre daha parçalanmış görünüyordu. Ayrıntılı protein taramaları, mitokondriyal ribozomun hem büyük hem de küçük parçalarının birçok yapı taşının azaldığını gösterdi; bu da tüm yapının daha az kararlı olduğunu düşündürüyor. Paralel olarak, enerji üreten kompleks I ve IV bileşenlerinin pek çoğu ve daha az düzeyde kompleks III öğeleri azalmışken, kompleks II değişmeden kalmıştı. Oksijen kullanımı ölçümleri, hücrelerin soluma ve hücresel enerji parası ATP’yi üretme yeteneğinin belirgin şekilde bozulduğunu doğruladı.
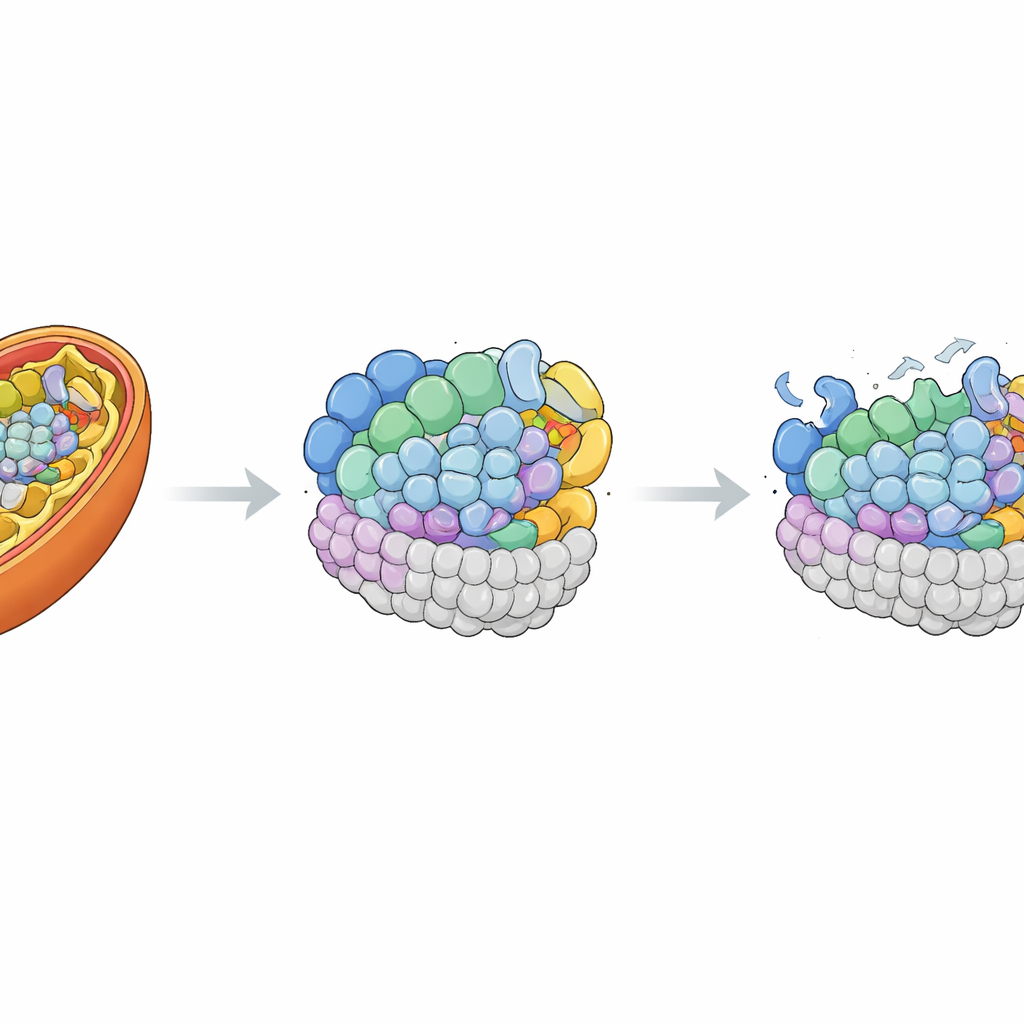
Eksik Parçayı Geri Koymak
MRPL42 kusurunun gerçekten sorumlu olduğunu kanıtlamak için araştırmacılar, zararsız bir viral taşıyıcı kullanarak hastanın hücrelerine normal bir gen kopyası yeniden tanıttılar. Bu, MRPL42 düzeylerini kontrol hücrelerinin üzerine çıkardı ve mitokondri ağının normal tübüler şeklini kısmen geri getirdi. Önemli olarak, mitokondriyal ribozomun ve kompleks I ile IV'ün kaybolan birçok protein bileşeni normal seviyelere doğru toparlandı. Ekip mitokondriyal solunumu yeniden ölçtüğünde, maksimum solunum kapasitesi ve yedek kapasitenin neredeyse normale döndüğünü ve temel enerji dönüşümünün de iyileştiğini buldu. Bu kurtarma deneyleri, çocuğun hücresel kusurlarını işlevsel MRPL42 eksikliğine güçlü biçimde bağladı.
Hastalar ve Bilim İçin Anlamı
Toplamda, çalışma MRPL42 genindeki biallelik (iki kopyalı) işlev kaybı değişikliğinin çoklu mitokondriyal enerji komplekslerinin başarısız olduğu şiddetli, sıklıkla ölümcül bir bozukluğa yol açabileceğini gösteriyor. Genin tamamen vazgeçilmez olmadığı, biraz protein oluştuğu için gelişmenin doğuma kadar ulaşabildiği görülüyor; ancak mitokondriyal ribozomu normal enerji üretimini destekleyecek kadar kararlı tutmak için kritik önemde. Aileler için bu çalışma, yıkıcı bir hastalığa moleküler bir açıklama ve doğru genetik danışmanlığa giden bir yol sağlıyor. Daha geniş açıdan ise DNA dizilemesi, RNA analizi ve protein profillemenin ne denli entegre şekilde yeni hastalık genlerini açığa çıkarabileceğini ve hücre makinelerindeki küçük kusurların tüm organları ve nihayetinde bütün vücudu nasıl etkilediğini netleştirebileceğini vurguluyor.
Atıf: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Anahtar kelimeler: mitokondriyal hastalık, oksidatif fosforilasyon, ribozomal protein, çok-omik, genetik varyant