Clear Sky Science · ru
Биаллельный вариант MRPL42 вызывает синдром комбинированной недостаточности окислительного фосфорилирования, выявленный с помощью мультиомики
Когда энергетические станции клетки дают сбой
Митохондрии часто называют электростанциями наших клеток: они тихо превращают топливо в энергию, которая поддерживает работу сердца и работу мозга. В этой статье рассказывается история новорождённой, чья тяжелая болезнь привела учёных к обнаружению небольшой неисправности в белковом аппарате митохондрий. Сочетая несколько передовых лабораторных методов, исследователи показали, как одна наследственная замена в одном гене может дестабилизировать клеточное производство энергии и вызывать фатальное множественное поражение органов.
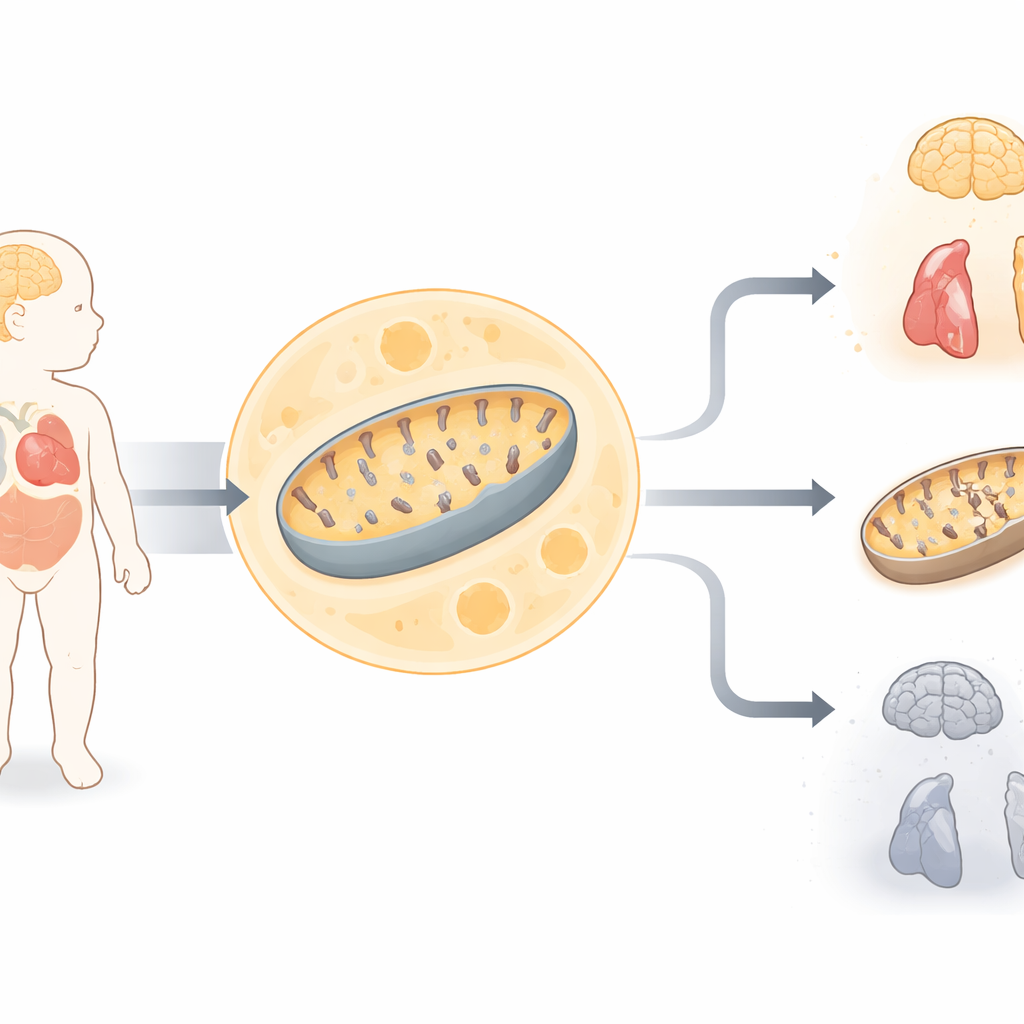
Новорожденная в серьёзной опасности
Исследование сосредоточено на девочке, рожденной от родственных родителей, которая по первому впечатлению выглядела нормально, но быстро развила серьёзные медицинские проблемы. У неё была мышечная слабость, затруднённое дыхание, судороги, проблемы со слухом, изменения в работе сердца и высокий уровень молочной кислоты в крови — характерный признак того, что клетки испытывают трудности с выработкой энергии. Сканирование мозга показало обширную потерю ткани мозга, а анализ кожных клеток выявил снижение активности двух основных ферментных комплексов митохондрий, производящих энергию. Эти подсказки указывали на тяжёлое расстройство митохондриального энергетического метаболизма, но стандартные генетические тесты до рождения не обнаружили известной причины.
В поисках скрытой ошибки в гене
Чтобы выйти за рамки рутинного тестирования, команда применила стратегию «мультиомики» — чтение ДНК, РНК‑сообщений, скопированных с ДНК, и полного набора белков в клетках ребёнка. Секвенирование всего генома выявило редкое изменение в обеих копиях гена MRPL42, который кодирует небольшую часть большого белкового аппарата (рибосомы) внутри митохондрий. Сам по себе этот вариант ДНК классифицировали как вариант неопределённой значимости, поскольку ранее MRPL42 не связывали с человеческими заболеваниями. Однако секвенирование РНК показало, что изменённое РНК‑сообщение в основном неправильно сплайсится: критический участок пропускается примерно в четырех из пяти молекул, что вызывает сдвиг рамки считывания и ранний стоп‑кодон. Только малая часть нормального сообщения, а следовательно и некоторого нормального белка, всё же образуется.
Как недостающий фрагмент ослабляет «электростанцию»
Исследования белков и визуализация в кожных клетках пациентки показали, что означает этот дефект на практике. Уровни белка MRPL42 были снижены примерно до четверти нормы, а митохондриальная сеть выглядела более фрагментированной, чем в здоровых клетках. Детальные белковые профили выявили сокращение многих компонентов митохондриальной рибосомы — как её большой, так и малой субъединиц — что говорит о меньшей стабильности всей структуры. Параллельно сократилось множество компонентов энергетических комплексов I и IV, а в меньшей степени — комплекса III, тогда как комплекс II оставался неизменным. Измерения потребления кислорода подтвердили, что способность клеток «дыхать» и синтезировать АТФ, валюту клеточной энергии, была существенно нарушена.
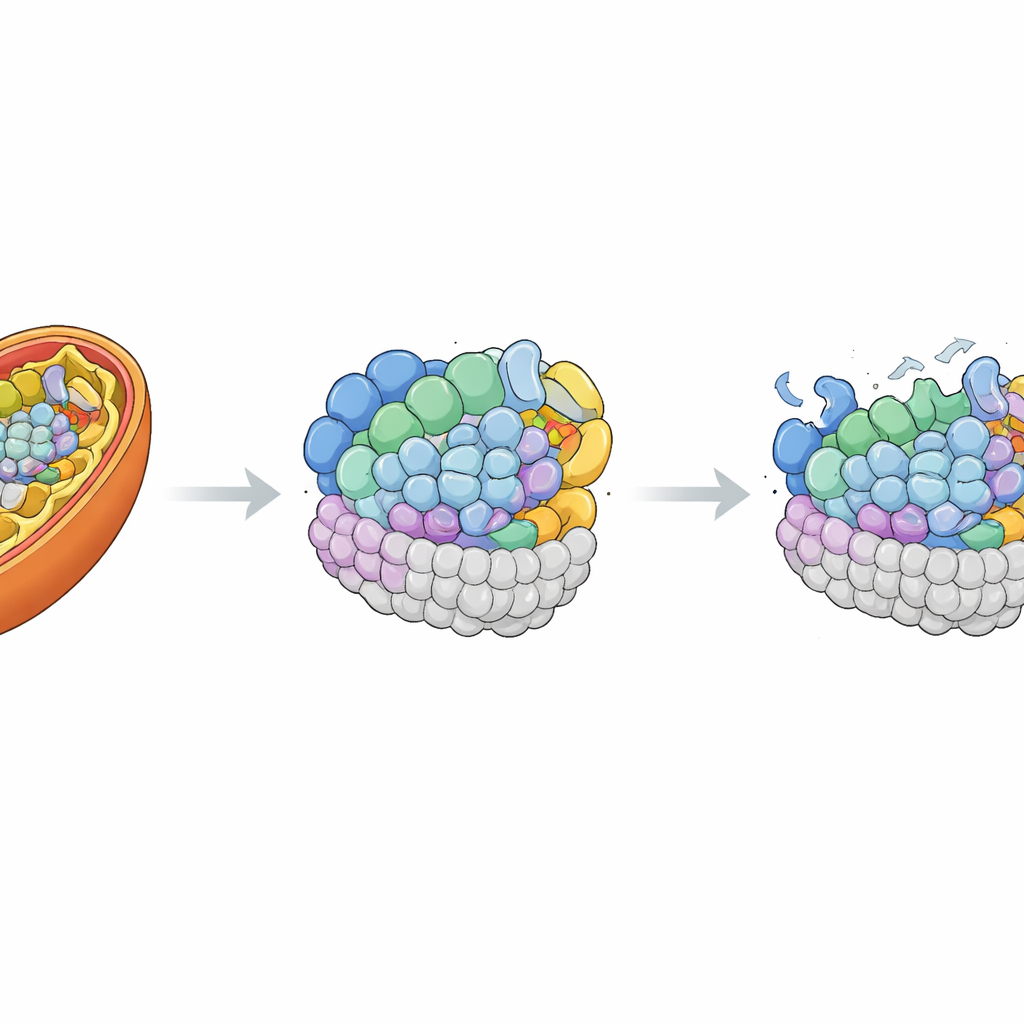
Восстановление отсутствующей детали
Чтобы доказать, что дефект MRPL42 действительно является причиной, исследователи вновь ввели нормальную копию гена в клетки пациентки с помощью безопасного вирусного носителя. Это повысило уровни MRPL42 выше, чем в контрольных клетках, и частично вернуло нормальную трубчатую форму митохондриальной сети. Важно, что многие утраченные белковые компоненты митохондриальной рибосомы и комплексов I и IV восстановились в сторону нормальных величин. При повторных измерениях дыхательной функции митохондрий максимальная дыхательная способность и резервная ёмкость почти нормализовались, а базовый энергетический оборот также улучшился. Эти эксперименты по «спасению» сильно связали клеточные дефекты ребёнка с нехваткой функционального MRPL42.
Что это значит для пациентов и науки
В целом исследование показывает, что биаллельное (в обеих копиях) утратой функции изменение в MRPL42 может вызывать тяжёлое, часто фатальное расстройство, при котором нарушается работа нескольких митохондриальных энергетических комплексов. Ген, по‑видимому, не абсолютно необходим — какой‑то белок всё же образуется, что позволяет развиваться до рождения — но он критически важен для поддержания стабильности митохондриальной рибосомы на уровне, достаточном для нормальной выработки энергии. Для семей эта работа даёт молекулярное объяснение разрушительной болезни и путь к точному генетическому консультированию. В более широком смысле она подчёркивает, насколько мощно интегрированное секвенирование ДНК, анализ РНК и профилирование белков может выявлять новые гены заболеваний и прояснять, как незначительные дефекты в клеточном механизме распространяют влияние на целые органы и, в конечном счёте, на весь организм.
Цитирование: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Ключевые слова: митохондриальное заболевание, окислительное фосфорилирование, рибосомный белок, мультиомика, генетический вариант