Clear Sky Science · de
Eine biallelische MRPL42‑Variante verursacht ein kombiniertes Syndrom der oxidativen Phosphorylierung, aufgedeckt durch Multi‑Omics
Wenn die Kraftwerke der Zelle versagen
Mitochondrien werden oft als Kraftwerke unserer Zellen bezeichnet, weil sie still und effizient Brennstoff in die Energie umwandeln, die Herzen schlagen und Gehirne denken lässt. Dieser Artikel verfolgt die Geschichte eines Neugeborenen, dessen schwere Erkrankung Wissenschaftler dazu brachte, einen winzigen Fehler in der Proteinfertigungsmaschinerie der Mitochondrien aufzudecken. Durch die Kombination mehrerer hochmoderner Labortechniken zeigen die Forschenden, wie eine einzelne vererbte Veränderung in einem Gen die zelluläre Energieproduktion destabilisieren und eine tödliche Multiorgankrankheit auslösen kann.
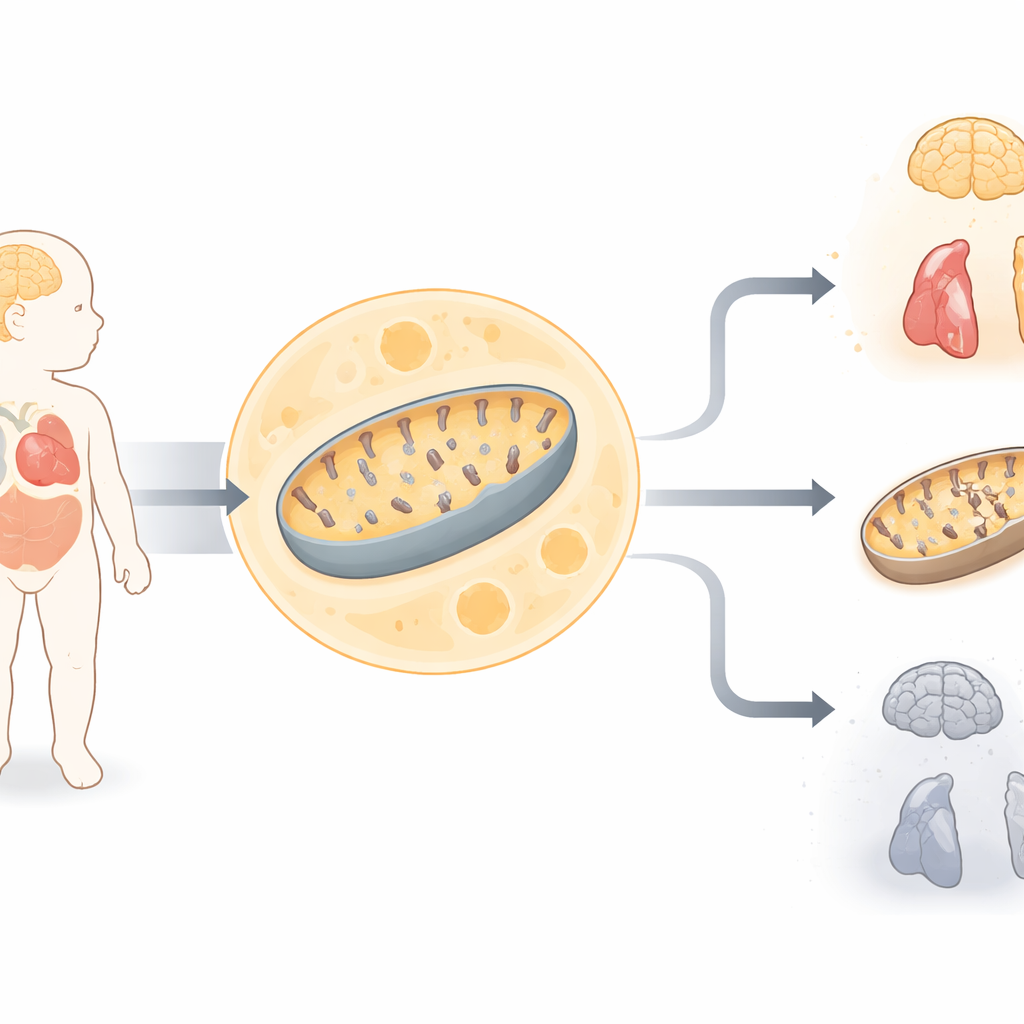
Ein Neugeborenes in ernsthafter Gefahr
Die Studie konzentriert sich auf ein Mädchen, das von verwandten Eltern geboren wurde und auf den ersten Blick normal schien, jedoch rasch schwere gesundheitliche Probleme entwickelte. Sie zeigte Muskelschwäche, Atembeschwerden, Anfälle, Hörstörungen, Herzveränderungen und erhöhte Laktatwerte im Blut — ein typisches Zeichen dafür, dass die Zellen Mühe haben, Energie zu erzeugen. Gehirnaufnahmen zeigten weitreichenden Gewebeverlust, und Untersuchungen an Hautzellen belegten, dass zwei wichtige energieproduzierende Enzymkomplexe in ihren Mitochondrien unterperformten. Diese Hinweise deuteten auf eine schwere Störung des mitochondrialen Energiestoffwechsels hin, doch die routinemäßigen genetischen Tests vor der Geburt hatten keine bekannte Ursache gefunden.
Auf der Suche nach einem verborgenen Gendefekt
Um über die Routineuntersuchungen hinauszugehen, verwendete das Team eine „Multi‑Omics“‑Strategie — die DNA, die von der DNA kopierten RNA‑Botschaften und die gesamte Proteinausstattung der Zellen des Kindes zu lesen. Die Ganzgenomsequenzierung offenbarte eine seltene Veränderung in beiden Kopien eines Gens namens MRPL42, das ein kleines Bauteil der großen Proteinfertigungs‑Einheit (Ribosom) innerhalb der Mitochondrien kodiert. Allein betrachtet wurde diese DNA‑Veränderung als ungewiss eingestuft, weil MRPL42 bislang nicht mit menschlicher Krankheit in Verbindung gebracht worden war. Die RNA‑Sequenzierung zeigte jedoch, dass die veränderte Gennachricht überwiegend fehlgespleißt war: Ein kritischer Abschnitt wurde bei etwa vier von fünf Molekülen übersprungen, was zu einem Leserasterwechsel und einem vorzeitigen Stoppcodon führte. Nur ein kleiner Teil normaler Botschaften und damit etwas normales Protein wurde weiterhin produziert.
Wie ein fehlendes Bauteil das Kraftwerk schwächt
Protein‑ und Bildgebungsstudien an den Hautzellen der Patientin zeigten, was diese fehlerhafte Botschaft praktisch bedeutete. Die MRPL42‑Proteinmengen waren auf etwa ein Viertel des Normalwerts reduziert, und das mitochondriale Netzwerk erschien fragmentierter als in gesunden Zellen. Detaillierte Proteinerhebungen zeigten, dass viele Bausteine des mitochondrialen Ribosoms — sowohl des großen als auch des kleinen Untereinheitenteils — verringert waren, was darauf hindeutet, dass die gesamte Struktur weniger stabil ist. Parallel dazu waren zahlreiche Komponenten der energieerzeugenden Komplexe I und IV und in geringerem Umfang auch des Komplexes III vermindert, während Komplex II unverändert blieb. Messungen des Sauerstoffverbrauchs bestätigten, dass die Fähigkeit der Zellen zu atmen und ATP, die Energieeinheit der Zelle, herzustellen, deutlich eingeschränkt war.
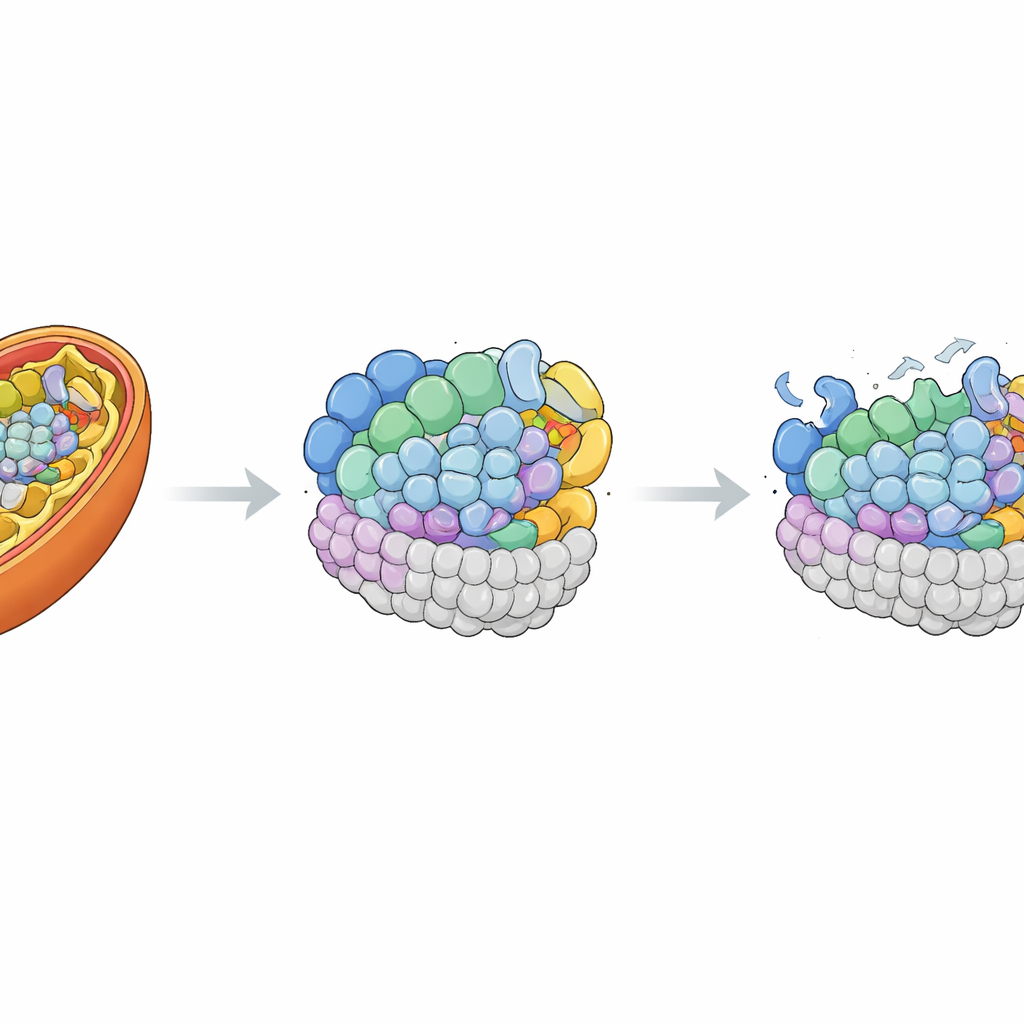
Das fehlende Bauteil wieder einsetzen
Um zu beweisen, dass der MRPL42‑Defekt tatsächlich verantwortlich war, führten die Forschenden eine normale Kopie des Gens mit einem harmlosen viralen Träger in die Zellen der Patientin ein. Dadurch stiegen die MRPL42‑Spiegel über das Niveau der Kontrollzellen und die normale tubuläre Form des mitochondrialen Netzwerks wurde teilweise wiederhergestellt. Wichtiger noch: Viele der verlorenen Proteinkomponenten des mitochondrialen Ribosoms sowie der Komplexe I und IV erholten sich wieder in Richtung normaler Mengen. Bei erneuten Messungen der mitochondrialen Atmung stellte das Team fest, dass die maximale Atemkapazität und die Reservekapazität nahezu normalisiert waren und auch der grundlegende Energieumsatz sich verbesserte. Diese Rettungsversuche verbanden die zellulären Defekte der Patientin klar mit dem Mangel an funktionalem MRPL42.
Was das für Patienten und die Wissenschaft bedeutet
Insgesamt zeigt die Studie, dass eine biallelische (zwei Kopien) Funktionsverlust‑Veränderung in MRPL42 eine schwere, oft tödliche Erkrankung verursachen kann, bei der mehrere mitochondriale Energiekomplexe ausfallen. Das Gen scheint nicht absolut essentiell zu sein — es bildet noch etwas Protein, sodass die Entwicklung bis zur Geburt möglich ist —, ist aber entscheidend dafür, das mitochondriale Ribosom ausreichend stabil zu halten, um eine normale Energieproduktion zu ermöglichen. Für betroffene Familien liefert diese Arbeit eine molekulare Erklärung für eine verheerende Krankheit und eine Grundlage für präzise genetische Beratung. Allgemeiner unterstreicht sie, wie tiefgehend integrierte DNA‑Sequenzierung, RNA‑Analyse und Proteinprofilierung neue Krankheitsgene aufdecken und erklären können, wie winzige Fehler in der zellulären Maschinerie sich ausweiten und ganze Organe und schließlich den gesamten Körper beeinträchtigen.
Zitation: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Schlüsselwörter: mitochondriale Erkrankung, oxidative Phosphorylierung, ribosomales Protein, Multi‑Omics, genetische Variante