Clear Sky Science · fr
Une variante biallélique de MRPL42 provoque un syndrome de déficit combiné de la phosphorylation oxydative révélé par le multi-omique
Lorsque les centrales énergétiques de la cellule défaillent
Les mitochondries sont souvent décrites comme les centrales énergétiques de nos cellules, convertissant discrètement le carburant en énergie qui maintient les cœurs qui battent et les cerveaux qui réfléchissent. Cet article retrace l’histoire d’un nouveau-né dont la maladie grave a conduit des scientifiques à découvrir une minuscule défaillance dans la machinerie de fabrication des protéines des mitochondries. En combinant plusieurs techniques de pointe en laboratoire, les chercheurs montrent comment un seul changement hérité dans un gène peut déstabiliser la production d’énergie cellulaire et provoquer une maladie multisystémique fatale.
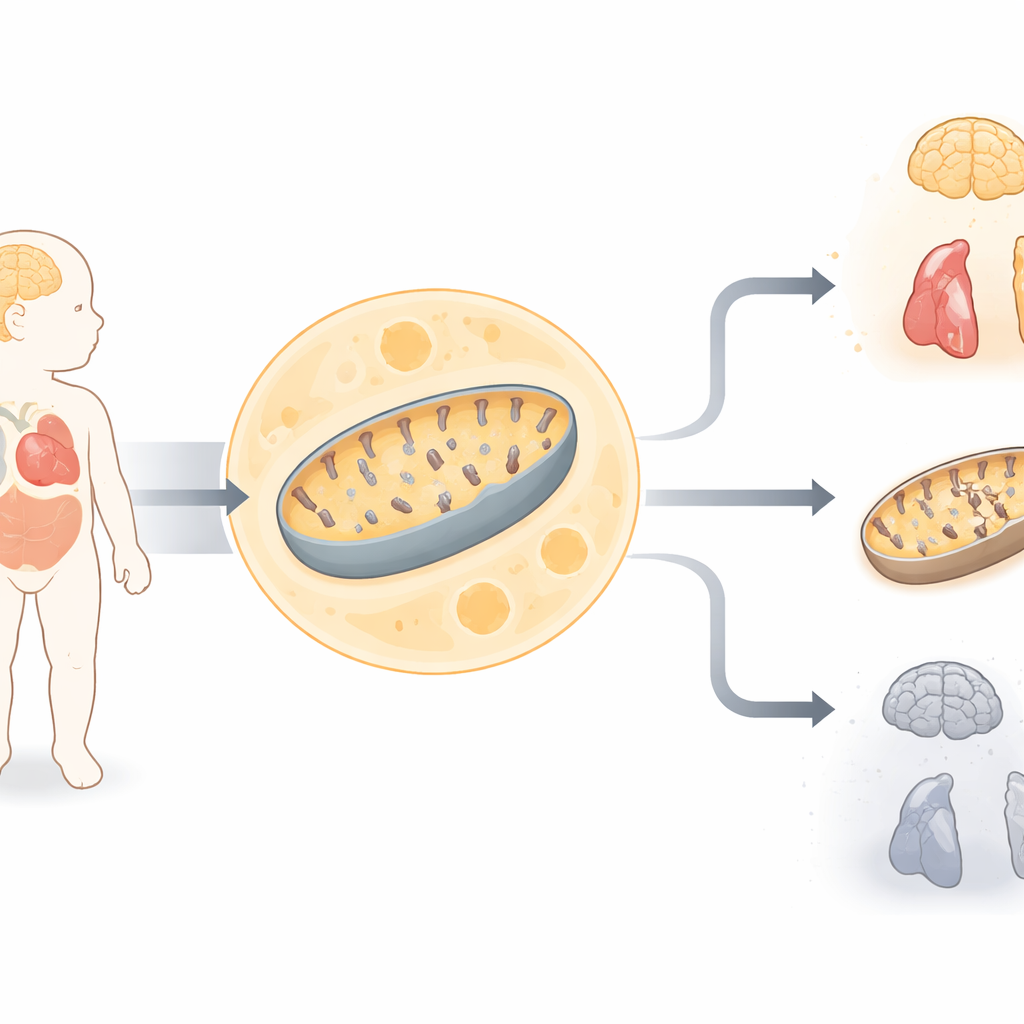
Un nouveau-né en grand danger
L’étude porte sur une petite fille née de parents apparentés qui, à première vue, semblait normale mais a rapidement développé des problèmes médicaux graves. Elle présentait une faiblesse musculaire, des difficultés respiratoires, des crises d’épilepsie, des troubles de l’audition, des anomalies cardiaques et des taux élevés d’acide lactique dans le sang — un signe révélateur que les cellules peinent à produire de l’énergie. Les scanners cérébraux ont montré une perte étendue de tissu cérébral, et des tests sur des cellules cutanées ont révélé que deux grands complexes enzymatiques producteurs d’énergie dans ses mitochondries fonctionnaient mal. Ces indices indiquaient un trouble sévère du métabolisme énergétique mitochondrial, mais les tests génétiques standard effectués avant la naissance n’avaient pas permis d’identifier une cause connue.
À la recherche d’une erreur génétique cachée
Pour aller au-delà des analyses routinières, l’équipe a utilisé une stratégie « multi-omique » — en lisant l’ADN, les messages ARN copiés de l’ADN et l’ensemble des protéines présentes dans les cellules de l’enfant. Le séquençage du génome entier a révélé une variante rare sur les deux copies d’un gène appelé MRPL42, qui code une petite pièce de la grande unité de fabrication des protéines (ribosome) à l’intérieur des mitochondries. Pris isolément, ce changement d’ADN était classé comme incertain car MRPL42 n’avait pas été associé auparavant à une maladie humaine. Toutefois, le séquençage de l’ARN a montré que le message génétique altéré était majoritairement mal épissé : une section critique était omise dans environ quatre molécules sur cinq, entraînant un décalage du cadre de lecture et un signal d’arrêt précoce. Seule une petite fraction de message normal, et donc un peu de protéine normale, était encore produite.
Comment une pièce manquante affaiblit la centrale
Des études protéiques et d’imagerie réalisées sur les cellules cutanées du patient ont révélé ce que ce message défectueux signifiait en pratique. Les niveaux de protéine MRPL42 étaient réduits à environ un quart de la normale, et le réseau mitochondrial paraissait plus fragmenté que dans des cellules saines. Des analyses protéiques détaillées ont montré que de nombreux éléments constitutifs du ribosome mitochondrial — tant de sa grande que de sa petite sous-unité — étaient diminués, suggérant que la structure entière était moins stable. Parallèlement, de nombreux composants des complexes producteurs d’énergie I et IV, et dans une moindre mesure du complexe III, étaient réduits, tandis que le complexe II restait inchangé. Des mesures de consommation d’oxygène ont confirmé que la capacité des cellules à respirer et à produire de l’ATP, la monnaie énergétique cellulaire, était fortement altérée.
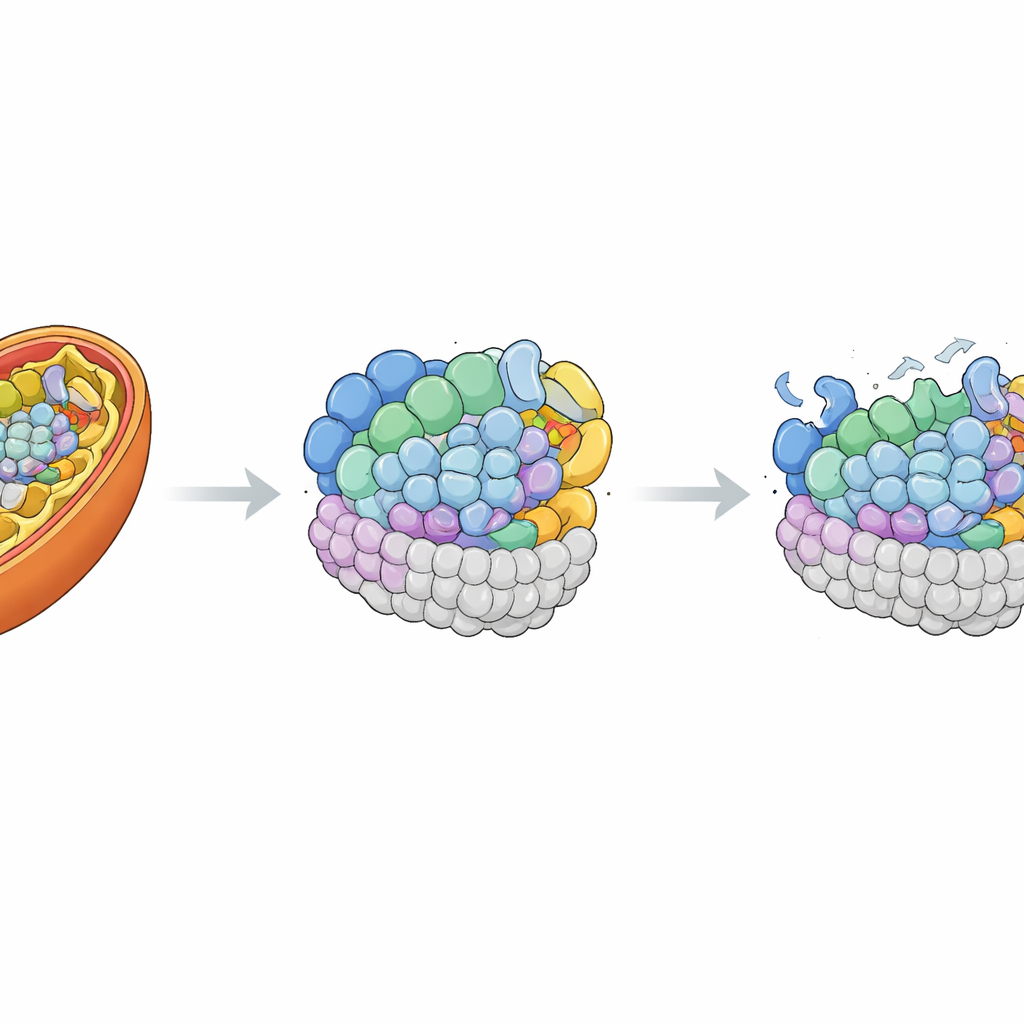
Remettre la pièce manquante
Pour démontrer que le défaut de MRPL42 était bien responsable, les chercheurs ont réintroduit une copie normale du gène dans les cellules du patient à l’aide d’un vecteur viral inoffensif. Cela a augmenté les niveaux de MRPL42 au-delà de ceux des cellules témoins et a partiellement restauré la forme tubulaire normale du réseau mitochondrial. Il est important de noter que de nombreux composants protéiques perdus du ribosome mitochondrial et des complexes I et IV sont remontés vers des quantités proches de la normale. Lorsque l’équipe a mesuré à nouveau la respiration mitochondriale, elle a constaté que la capacité respiratoire maximale et la réserve ont presque normalisé, et que le turnover énergétique de base s’était aussi amélioré. Ces expériences de restauration ont fortement lié les défauts cellulaires de l’enfant au manque de MRPL42 fonctionnel.
Ce que cela signifie pour les patients et la science
Au total, l’étude montre qu’une variante biallélique (deux copies) entraînant une perte de fonction de MRPL42 peut causer un trouble sévère, souvent fatal, dans lequel plusieurs complexes énergétiques mitochondriaux échouent. Le gène ne semble pas absolument indispensable — une certaine protéine se forme encore, permettant le développement jusqu’à la naissance — mais il est crucial pour maintenir le ribosome mitochondrial suffisamment stable afin de soutenir une production d’énergie normale. Pour les familles, ce travail apporte une explication moléculaire à une maladie dévastatrice et ouvre la voie à un conseil génétique précis. Plus largement, il souligne à quel point le séquençage de l’ADN, l’analyse de l’ARN et le profilage protéique, intégrés ensemble, peuvent révéler de nouveaux gènes de maladie et clarifier comment de petites défaillances de la machinerie cellulaire se propagent jusqu’à affecter des organes entiers et, finalement, l’ensemble du corps.
Citation: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Mots-clés: maladie mitochondriale, phosphorylation oxydative, protéine ribosomique, multi-omique, variant génétique