Clear Sky Science · nl
Een bialleel MRPL42‑variant veroorzaakt een gecombineerd oxidatieve fosforyleringsdeficiëntiesyndroom aan het licht gebracht door multi‑omics
Wanneer de energiecentrales van de cel falen
Mitochondriën worden vaak de energiecentrales van onze cellen genoemd; ze zetten stilletjes brandstof om in de energie die harten laat kloppen en hersenen laat functioneren. Dit artikel volgt het verhaal van een pasgeborene wiens ernstige ziekte wetenschappers ertoe bracht een klein defect in de eiwitproductie‑machine binnen de mitochondriën te ontdekken. Door meerdere geavanceerde laboratoriumtechnieken te combineren, laten de onderzoekers zien hoe één erfelijke wijziging in een gen de cellulaire energieproductie kan destabiliseren en een fatale multi‑orgaanziekte kan veroorzaken.
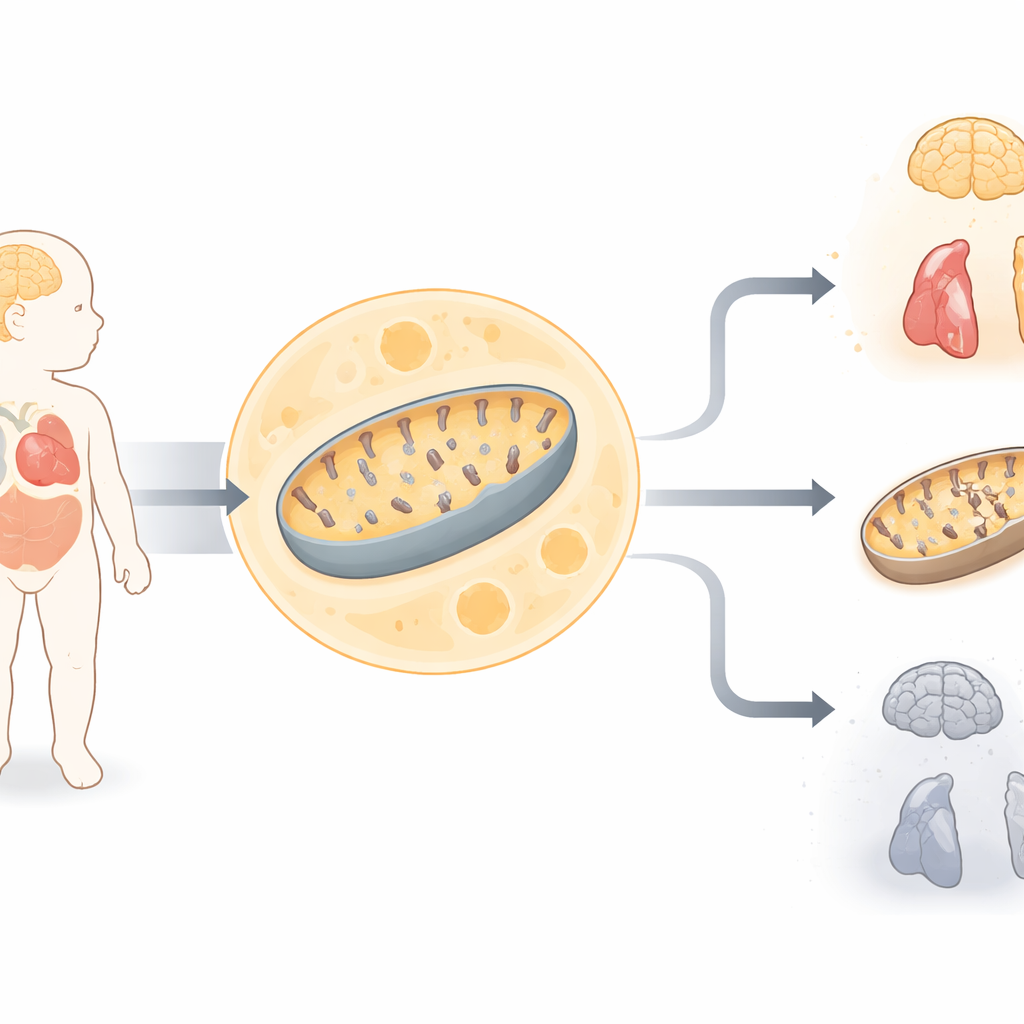
Een pasgeborene in ernstig gevaar
De studie concentreert zich op een meisje geboren uit verwante ouders die, op het eerste gezicht, normaal leek maar al snel ernstige medische problemen ontwikkelde. Ze had spierzwakte, ademhalingsproblemen, epileptische aanvallen, gehoorproblemen, hartafwijkingen en hoge lactaatwaarden in het bloed — een kenmerkend teken dat cellen moeite hebben om energie te produceren. Hersenbeelden lieten wijdverspreid verlies van hersenweefsel zien, en onderzoeken van huidcellen toonden aan dat twee belangrijke energieproducerende enzymcomplexen in haar mitochondriën ondermaats functioneerden. Deze aanwijzingen wezen op een ernstige stoornis van het mitochondriële energiemetabolisme, maar standaard genetische tests vóór de geboorte hadden geen bekende oorzaak gevonden.
Op zoek naar een verborgen genfout
Om verder te gaan dan routinetests gebruikte het team een “multi‑omics” strategie — het lezen van het DNA, de RNA‑boodschappen die van DNA worden gekopieerd, en de volledige set eiwitten in de cellen van het kind. Whole‑genome sequencing toonde een zeldzame wijziging in beide kopieën van een gen genaamd MRPL42, dat codeert voor een klein onderdeel van de grote eiwitproducerende eenheid (ribosoom) binnen de mitochondriën. Op zichzelf werd deze DNA‑verandering geclassificeerd als onzeker omdat MRPL42 eerder niet aan menselijke ziekten was gekoppeld. RNA‑sequencing liet echter zien dat het veranderde genboodschap grotendeels verkeerd gespliced was: een kritieke sectie werd in ongeveer vier van de vijf moleculen overgeslagen, wat een verschuiving in het leesraam en een vroeg stopsein veroorzaakte. Slechts een klein deel van de normale boodschap, en daarmee enig normaal eiwit, werd nog geproduceerd.
Hoe een ontbrekend onderdeel de energiecentrale verzwakt
Eiwit‑ en beeldvormingsstudies in de huidcellen van de patiënt lieten zien wat deze foutieve boodschap in de praktijk betekende. De hoeveelheden MRPL42‑eiwit waren gereduceerd tot ongeveer een kwart van normaal, en het mitochondriale netwerk leek meer gefragmenteerd dan in gezonde cellen. Gedetailleerde eiwitanalyses toonden dat veel bouwstenen van het mitochondriale ribosoom — zowel van de grote als de kleine subeenheid — verminderd waren, wat suggereert dat de hele structuur minder stabiel was. Parallel daaraan waren talrijke componenten van de energieproducerende complexen I en IV, en in mindere mate complex III, verlaagd, terwijl complex II onveranderd bleef. Metingen van zuurstofgebruik bevestigden dat het vermogen van de cellen om te ‘ademen’ en ATP te maken, de energievaluta van de cel, duidelijk was aangetast.
Het ontbrekende onderdeel terugplaatsen
Om te bewijzen dat het MRPL42‑defect daadwerkelijk de oorzaak was, introduceerden de onderzoekers een normale kopie van het gen in de cellen van de patiënt met behulp van een onschadelijke virale drager. Dit verhoogde de MRPL42‑niveaus boven die in controlecellen en herstelde gedeeltelijk de normale buisvormige structuur van het mitochondriale netwerk. Belangrijker nog, veel van de verloren eiwitcomponenten van het mitochondriale ribosoom en van complexen I en IV namen weer toe richting normale hoeveelheden. Toen het team de mitochondriale respiratie opnieuw mat, bleek dat de maximale ademcapaciteit en de spare capacity bijna normaliseerden, en ook de basale energiedoorvoer verbeterde. Deze rescue‑experimenten verbonden de cellulaire defecten van het kind sterk met het tekort aan functioneel MRPL42.
Wat dit betekent voor patiënten en wetenschap
Alles bij elkaar toont de studie aan dat een bialleel (twee‑kopieën) verlies‑van‑functie wijziging in MRPL42 een ernstige, vaak dodelijke aandoening kan veroorzaken waarbij meerdere mitochondriale energiecomplexen falen. Het gen lijkt niet absoluut essentieel te zijn — er vormt zich nog enig eiwit, waardoor de ontwikkeling tot de geboorte kan doorgaan — maar het is cruciaal om het mitochondriale ribosoom stabiel genoeg te houden om normale energieproductie te ondersteunen. Voor families biedt dit werk een moleculaire verklaring voor een verwoestende ziekte en een basis voor accurate genetische raadgeving. In bredere zin onderstreept het hoe diep geïntegreerd DNA‑sequencing, RNA‑analyse en eiwitprofilering nieuwe ziektegenen kunnen onthullen en kunnen verduidelijken hoe kleine defecten in de celmachinerie zich uitbreiden en hele organen en uiteindelijk het hele lichaam beïnvloeden.
Bronvermelding: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Trefwoorden: mitochondriale ziekte, oxidatieve fosforylering, ribosomaal eiwit, multi‑omics, genetische variant