Clear Sky Science · sv
En biallelic MRPL42-variant orsakar ett kombinerat oxidativt fosforyleringssyndrom avslöjat av multi-omik
När cellens kraftverk sviktar
Mitokondrier kallas ofta cellernas kraftverk—de omvandlar stillsamt bränsle till den energi som håller hjärtan slagande och hjärnor tänkande. Den här artikeln följer historien om en nyfödd vars svåra sjukdom ledde forskare till en liten felaktighet i cellens proteinproducerande maskineri inne i mitokondrierna. Genom att kombinera flera toppmoderna laboratoriemetoder visar forskarna hur en enda ärftlig förändring i en gen kan destabilisera cellernas energiproduktion och orsaka en dödlig multisystemsjukdom.
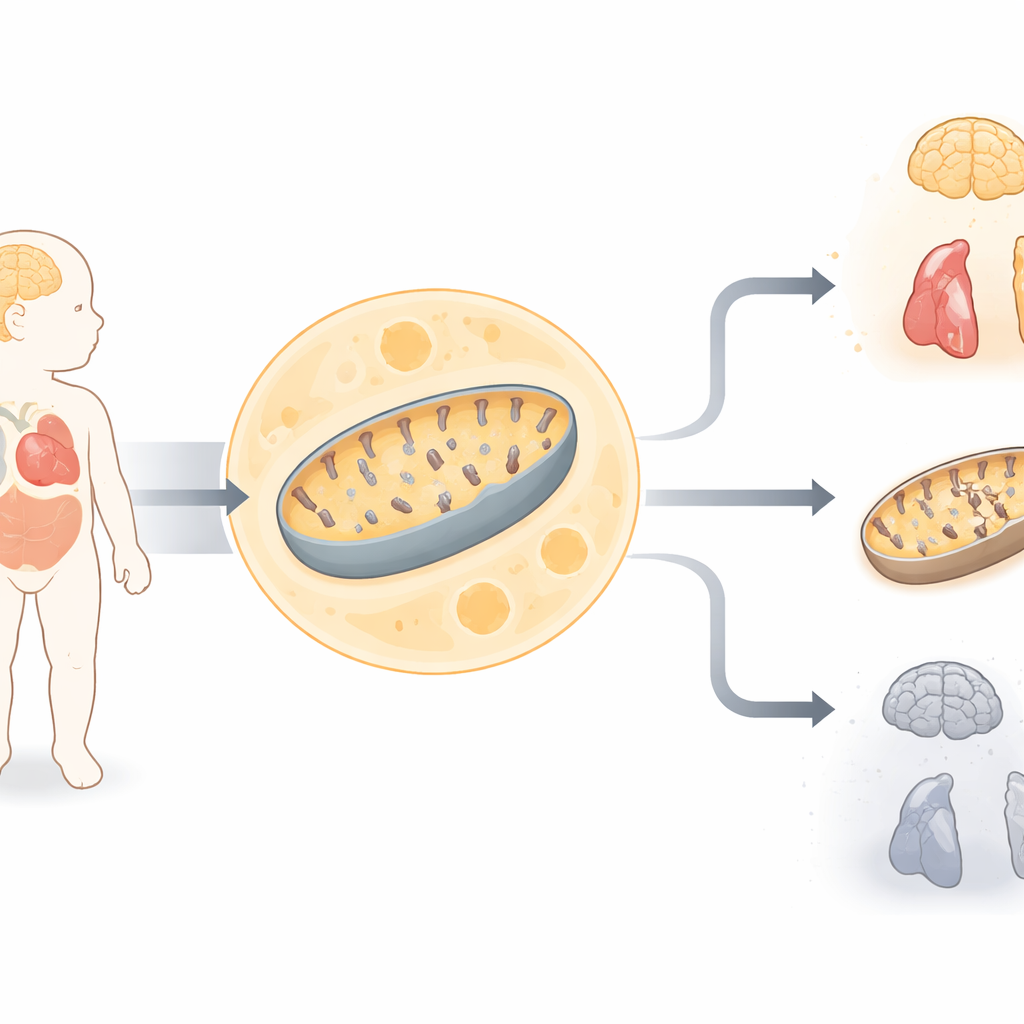
En nyfödd i allvarligt tillstånd
Studien kretsar kring en flicka född av närbesläktade föräldrar som vid första anblick verkade normal men snabbt utvecklade allvarliga medicinska problem. Hon hade svaga muskler, andningssvårigheter, anfall, hörselproblem, hjärtavvikelser och höga nivåer av mjölksyra i blodet—ett kännetecken på att cellerna har svårt att producera energi. Hjärnavbildningar visade omfattande förlust av hjärnvävnad, och tester på hudceller visade att två stora energiproducerande enzymkomplex i hennes mitokondrier fungerade dåligt. Dessa ledtrådar pekade mot en svår störning i mitokondriell energimetabolism, men rutinmässiga genetiska tester före födseln hade inte kunnat identifiera en känd orsak.
På jakt efter ett dolt gendefekt
För att gå bortom rutinanalys använde teamet en ”multi-omik”-strategi—man läste DNA, de RNA-meddelanden som kopieras från DNA, och hela uppsättningen proteiner i barnets celler. Helgenomsekvensering avslöjade en sällsynt förändring i båda kopiorna av en gen kallad MRPL42, som kodar för en liten del av den stora proteinproducerande enheten (ribosomen) inne i mitokondrierna. I sig själv klassificerades denna DNA-förändring som osäker eftersom MRPL42 tidigare inte kopplats till mänsklig sjukdom. Men RNA-sekvensering visade att det ändrade genbudskapet mestadels var felaktigt splitsat: en kritisk sektion utelämnades i ungefär fyra av fem molekyler, vilket orsakade ett läsramsskifte och en tidig stoppkodon. Endast en liten andel normalt meddelande, och därmed viss normal proteinmängd, fanns kvar.
Hur en saknad komponent försvagar kraftverket
Protein- och avbildningsstudier i patientens hudceller visade vad detta felaktiga budskap betydde i praktiken. Nivåerna av MRPL42-protein var reducerade till cirka en fjärdedel av det normala, och det mitokondriella nätverket såg mer fragmenterat ut än i friska celler. Detaljerade proteinstudier visade att många byggstenar i den mitokondriella ribosomen—både dess stora och små delar—var reducerade, vilket tyder på att hela strukturen var mindre stabil. Parallellt minskade många komponenter i de energi‑producerande komplexen I och IV, och i mindre grad komplex III, medan komplex II var oförändrat. Mätningar av syreförbrukning bekräftade att cellernas förmåga att andas och tillverka ATP, cellens energivaluta, var kraftigt nedsatt.
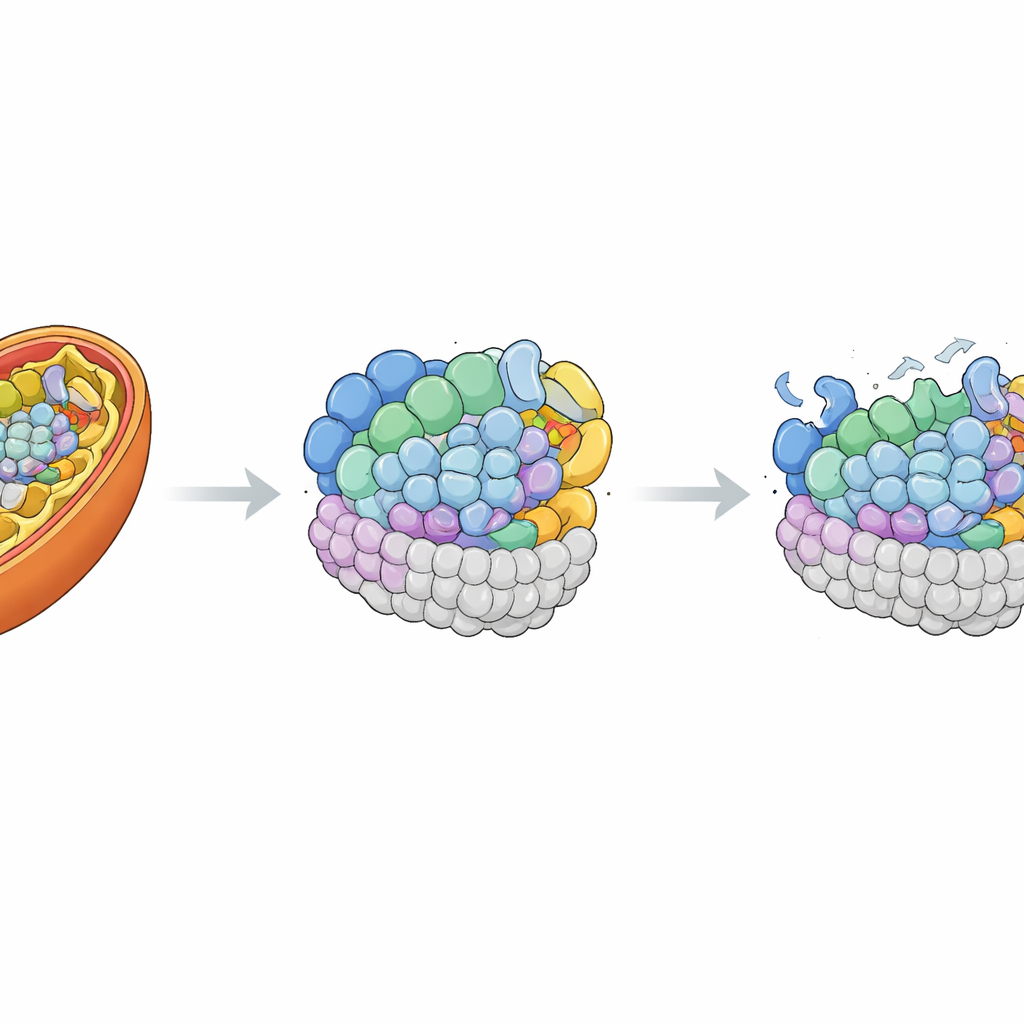
Sätta tillbaka den saknade biten
För att bevisa att MRPL42-felet verkligen var ansvarigt återinförde forskarna en normal kopia av genen i patientens celler med hjälp av en ofarlig viral bärare. Detta ökade MRPL42-nivåerna över dem i kontrollceller och återställde delvis den normala tubulära formen hos det mitokondriella nätverket. Viktigt är att många av de förlorade proteinkomponenterna i den mitokondriella ribosomen och i komplex I och IV återhämtade sig mot normala mängder. När teamet mätte mitokondriell andning igen fann de att maximal andningskapacitet och reservkapacitet nästan normaliserades, och även grundläggande energiförbrukning förbättrades. Dessa räddningsexperiment knöt starkt barnets cellulära fel till bristen på funktionellt MRPL42.
Vad detta betyder för patienter och vetenskap
Sammantaget visar studien att en biallel (tvåkopiors) funktionstörande förändring i MRPL42 kan orsaka en svår, ofta dödlig sjukdom där flera mitokondriella energikomplex fallerar. Genen tycks inte vara absolut nödvändig—viss proteinbildning kvarstår, vilket möjliggör utveckling fram till födseln—men den är avgörande för att hålla den mitokondriella ribosomen tillräckligt stabil för att stödja normal energiproduktion. För familjer ger detta arbete en molekylär förklaring till en förödande sjukdom och en väg till korrekt genetisk rådgivning. Mer generellt understryker det hur djupt integrerat DNA-sekvensering, RNA-analys och proteomprofilering kan avtäcka nya sjukdomsgenrer och klargöra hur små fel i cellens maskineri sprider sig för att påverka hela organ och, i slutändan, hela kroppen.
Citering: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Nyckelord: mitokondriesjukdom, oxidativ fosforylering, ribosomalt protein, multi-omik, genetisk variant