Clear Sky Science · ar
متغيّر ثنائي الأليل في MRPL42 يسبب متلازمة نقص الفسفرة التأكسدية المركبة تكشّفها نهج متعدد الأومكس
عندما تتعطل محطات طاقة الخلية
تُسمى الميتوكوندريا غالبًا بمحطات توليد الطاقة في خلايانا، حيث تحول الوقود بهدوء إلى طاقة تبقي القلوب تخفق والأدمغة تفكر. تتبع هذه المقالة قصة مولودة حديثًا أدت حالتها الصحية الحرجة إلى كشف العلماء لخلل صغير في آلية صناعة البروتين داخل الميتوكوندريا. من خلال دمج عدة تقنيات مخبرية متقدمة، يوضح الباحثون كيف يمكن لتغيير وراثي واحد موروث في جين واحد أن يزعزع إنتاج الخلايا للطاقة ويتسبب في مرض متعدد الأجهزة قد يكون قاتلاً.
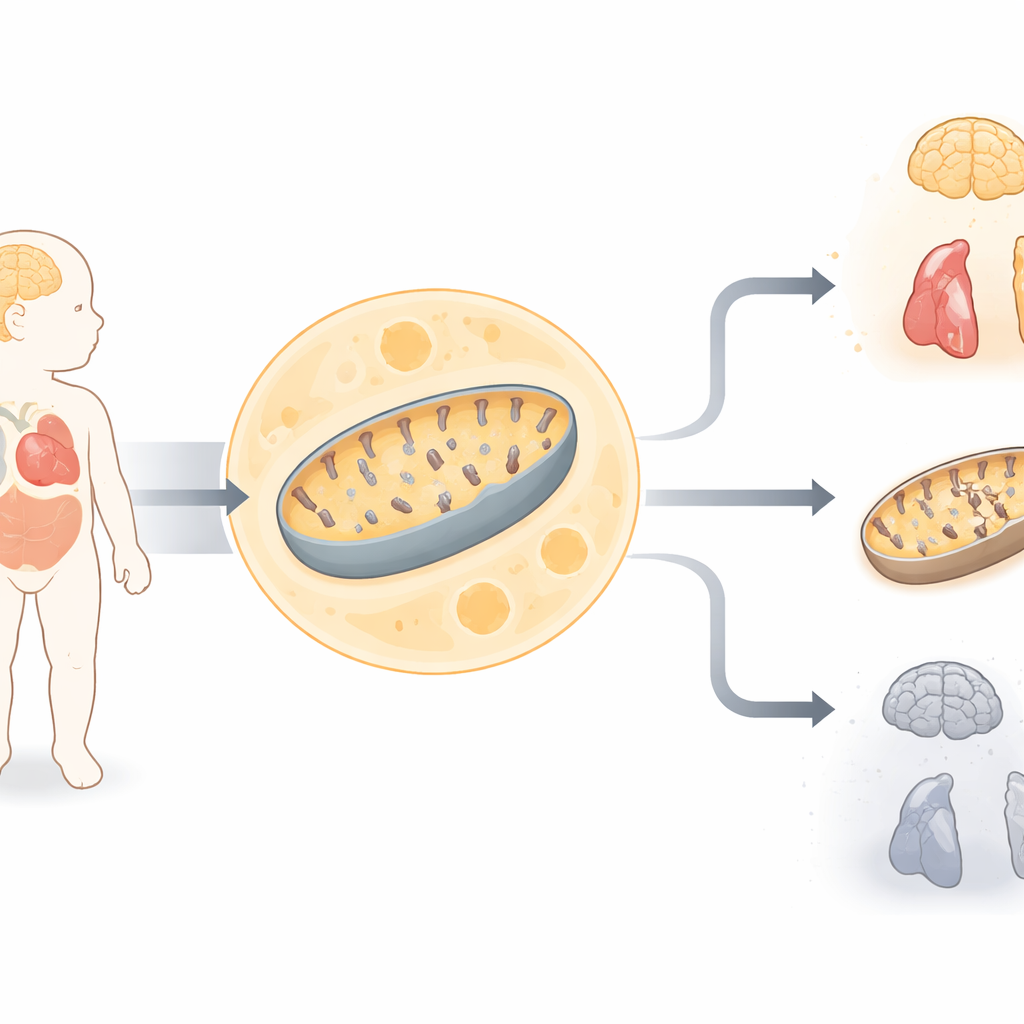
مولودة في مأزق خطير
تركز الدراسة على رضيعَة وُلدت لأبوين مرتبطين قرابياً وبدا في البداية أنها طبيعية لكنها سرعان ما طورت مشاكل طبية خطيرة. كانت لديها عضلات ضعيفة، وصعوبات في التنفس، ونوبات صرع، ومشكلات سمعية، وتغيرات في القلب، ومستويات مرتفعة من حمض اللاكتيك في الدم — وهي علامة دالة على أن الخلايا تكافح لإنتاج الطاقة. كشفت صور الدماغ عن فقدان واسع للنسيج الدماغي، وأظهرت اختبارات على خلايا الجلد أن اثنين من المعقّدات الرئيسية المولدة للطاقة في ميتوكوندرياتها كانت تعمل دون المستوى الطبيعي. أشارت هذه الدلائل إلى اضطراب شديد في أيض طاقة الميتوكوندريا، لكن الفحوصات الجينية القياسية قبل الولادة فشلت في العثور على سبب معروف.
البحث عن خطأ جيني مخفي
لتجاوز الاختبارات الروتينية، استخدم الفريق استراتيجية «متعدد الأومكس» — قراءة الحمض النووي، والرسائل الريبونية المنسوخة من الحمض النووي، والمجموعة الكاملة للبروتينات في خلايا الطفل. كشف التسلسل الجينومي الكامل عن تغيير نادر في النسختين من جين يُدعى MRPL42، الذي يشفر جزءًا صغيرًا من الوحدة الكبيرة لصناعة البروتين (الريبوزوم) داخل الميتوكوندريا. بمفرده، صُنّف هذا التغيير في الحمض النووي على أنه غير مؤكد لأن MRPL42 لم يُرتبط سابقًا بمرض بشري. ومع ذلك، أظهر تسلسل الرنا أن رسالة الجين المتغيرة كانت متشابكة بشكل خاطئ في الغالب: تم تجاهل مقطع حاسم في حوالي أربعة من كل خمسة جزيئات، مما تسبب في تحوّل إطار القراءة وإشارة توقف مبكرة. لم تُنتَج سوى نسبة صغيرة من الرسائل الطبيعية، ومن ثم بعض البروتين الطبيعي.
كيف يضعف جزء مفقود محطة الطاقة
كشفت دراسات البروتين والتصوير في خلايا جلد المريضة ما يعنيه هذا الخطأ عمليًا. انخفضت مستويات بروتين MRPL42 إلى حوالي ربع المستوى الطبيعي، وبدت شبكة الميتوكوندريا أكثر تجزؤًا مقارنة بالخلايا السليمة. أظهرت مسوحات البروتين التفصيلية أن العديد من مكوّنات بناء الريبوزوم الميتوكوندري — سواء الجزء الكبير أو الصغير — كانت منخفضة، مما يوحي بأن الهيكل بأكمله أقل استقرارًا. وبالتوازي، انخفضت العديد من مكوّنات المعقّدات المولدة للطاقة I وIV، وبدرجة أقل المعقّد III، بينما بقي المعقّد II دون تغيير. أكدت قياسات استهلاك الأكسجين أن قدرة الخلايا على التنفس وإنتاج ATP، عملة الطاقة في الخلية، كانت متضررة بشكل ملحوظ.
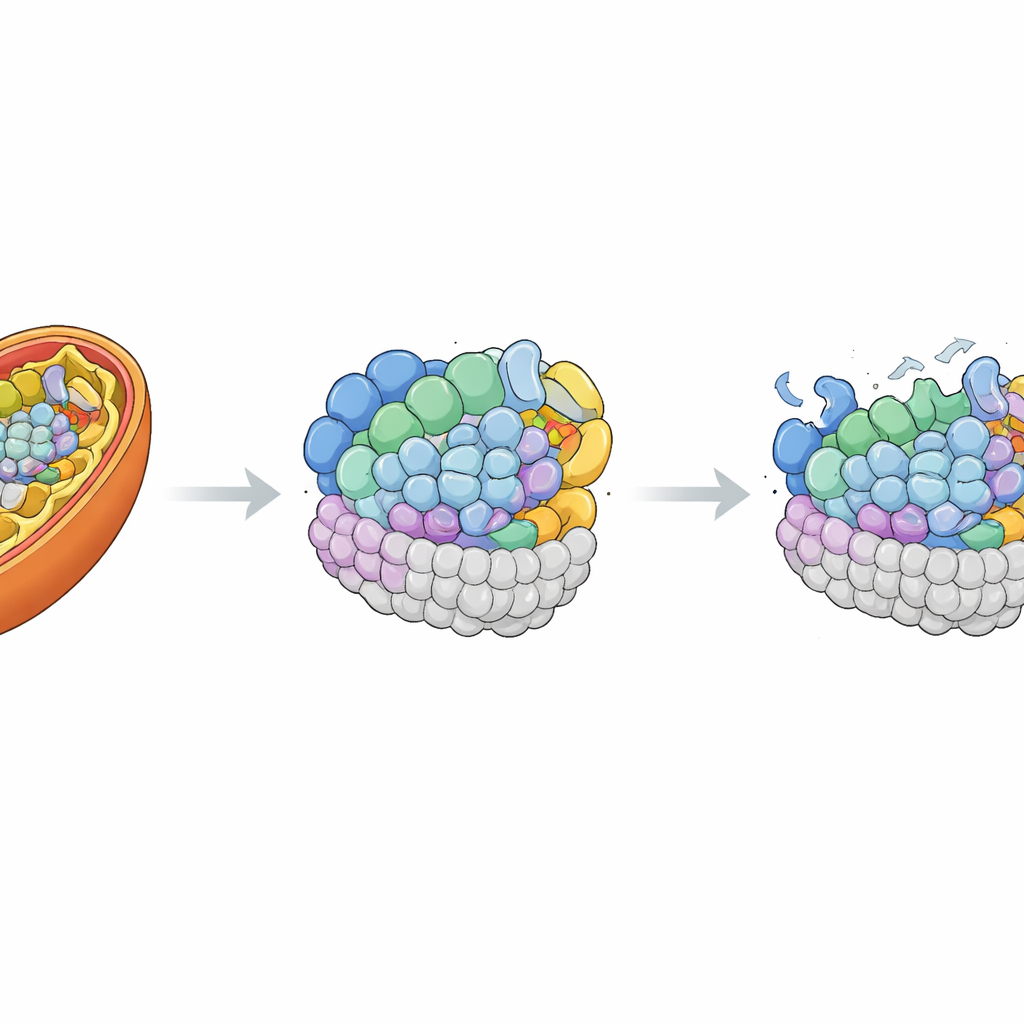
إرجاع القطعة المفقودة
لإثبات أن خلل MRPL42 كان بالفعل السبب، أعاد الباحثون إدخال نسخة طبيعية من الجين إلى خلايا المريضة باستخدام ناقل فيروسي غير مؤذٍ. رفع هذا الإجراء مستويات MRPL42 إلى ما فوق تلك في خلايا التحكم وأعاد جزئيًا الشكل الأنبوبي الطبيعي لشبكة الميتوكوندريا. والأهم أن العديد من مكوّنات بروتين الريبوزوم الميتوكوندري ومعقّدات I وIV التي فقدت استعادت كمياتها باتجاه الطبيعي. عند إعادة قياس تنفّس الميتوكوندريا، وجد الفريق أن القدرة التنفسية القصوى والسعة الاحتياطية كادتا أن تصبح طبيعيتين، وتحسّن معدل دوران الطاقة الأساسي أيضًا. ربطت تجارب الإنقاذ هذه بقوة عيوب الخلايا لدى الطفل بنقص MRPL42 الوظيفي.
ما الذي يعنيه هذا للمرضى والعلم
بشكل إجمالي، تُظهر الدراسة أن تغيير فقدان الوظيفة ثنائي الأليل في MRPL42 يمكن أن يسبب اضطرابًا شديدًا وغالبًا مميتًا تتعطل فيه عدة معقّدات طاقة ميتوكوندرية. يبدو أن الجين ليس ضروريًا بالكامل — فبعض البروتين لا يزال يتكوّن، مما يسمح بالتطور حتى الولادة — لكنه حاسم للحفاظ على استقرار الريبوزوم الميتوكوندري بما يكفي لدعم إنتاج الطاقة الطبيعي. بالنسبة للعائلات، يوفر هذا العمل تفسيرًا جزيئيًا لمرض مدمر وطريقًا للاستشارة الجينية الدقيقة. وعلى نطاق أوسع، يبرز كيف أن دمج تسلسل الحمض النووي وتحليل الرنا وتوصيف البروتين يمكن أن يكشف عن جينات مرضية جديدة ويوضح كيف تؤثر أعطال صغيرة في آلية الخلية امتدادًا على أعضاء كاملة وفي نهاية المطاف على الجسم بأكمله.
الاستشهاد: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
الكلمات المفتاحية: مرض ميتوكوندري, الفسفرة التأكسدية, بروتين ريبوزومي, متعدد الأومكس, متغيّر جيني