Clear Sky Science · pt
Uma variante bialélica de MRPL42 causa uma síndrome de deficiência combinada da fosforilação oxidativa revelada por multi-ômicas
Quando as usinas de energia da célula falham
As mitocôndrias são frequentemente chamadas de usinas de energia de nossas células, convertendo silenciosamente combustível na energia que mantém corações batendo e cérebros funcionando. Este artigo acompanha a história de um recém-nascido cuja doença grave levou cientistas a descobrir uma falha minúscula na maquinaria de produção de proteínas dentro das mitocôndrias. Ao combinar várias técnicas laboratoriais de ponta, os pesquisadores mostram como uma única alteração herdada em um gene pode desestabilizar a produção de energia celular e causar uma doença multisistêmica fatal.
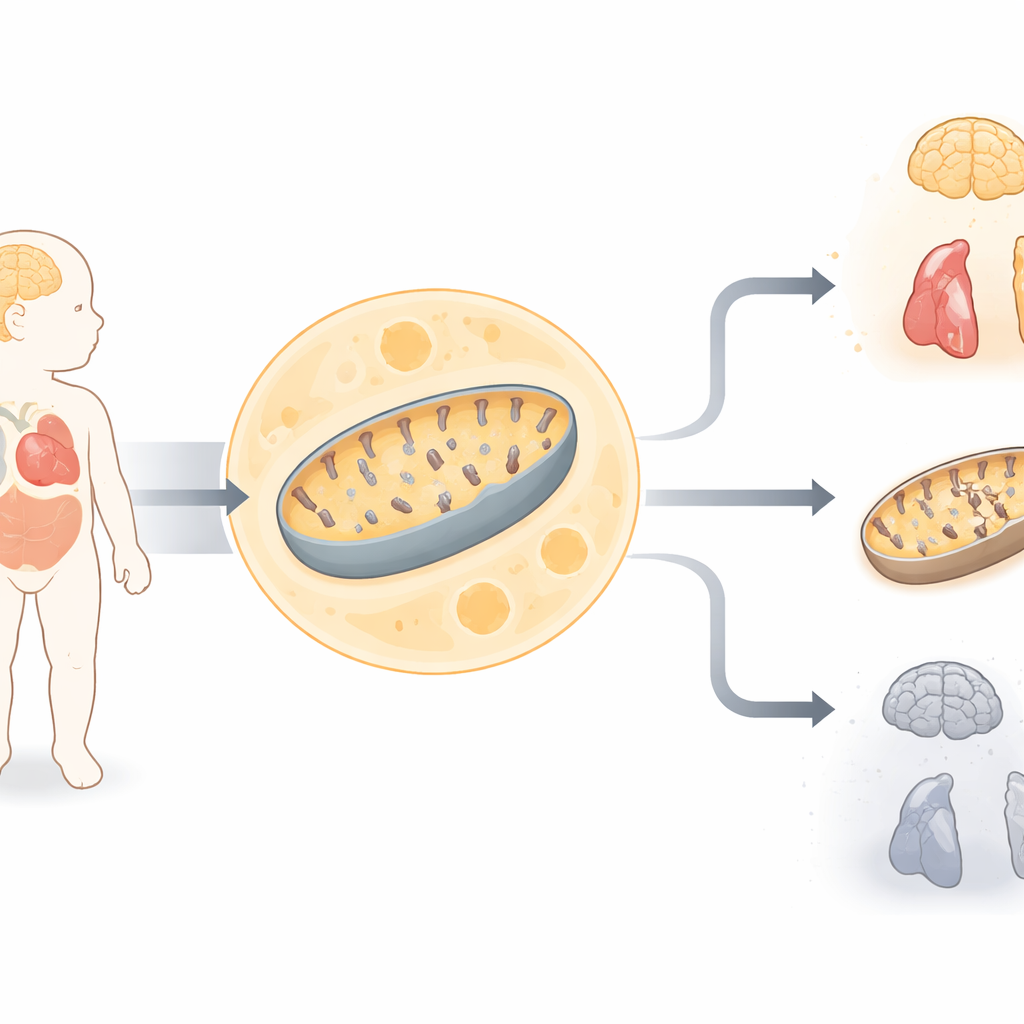
Um recém-nascido em grave perigo
O estudo centra-se em uma menina nascida de pais consanguíneos que, à primeira vista, parecia normal, mas rapidamente desenvolveu problemas médicos graves. Ela apresentava fraqueza muscular, dificuldades respiratórias, convulsões, alterações na audição, alterações cardíacas e níveis elevados de ácido lático no sangue — um sinal claro de que as células estavam com dificuldade para produzir energia. Exames cerebrais revelaram perda extensa de tecido cerebral, e testes em células da pele mostraram que dois grandes complexos enzimáticos produtores de energia nas mitocôndrias estavam com desempenho reduzido. Essas pistas apontavam para um distúrbio severo do metabolismo energético mitocondrial, mas os testes genéticos padrão antes do nascimento não haviam identificado uma causa conhecida.
Procurando um erro genético oculto
Para ir além dos testes de rotina, a equipe usou uma estratégia “multi-ômicas” — lendo o DNA, as mensagens de RNA copiadas do DNA e o conjunto completo de proteínas nas células da criança. O sequenciamento do genoma completo revelou uma alteração rara em ambas as cópias de um gene chamado MRPL42, que codifica uma pequena parte da grande unidade de produção de proteínas (ribossomo) dentro das mitocôndrias. Isoladamente, essa alteração no DNA foi classificada como de significado incerto porque MRPL42 não havia sido previamente associada a doenças humanas. Entretanto, o sequenciamento de RNA mostrou que a mensagem gênica alterada era majoritariamente mal emparelhada (misspliced): uma seção crítica foi omitida em cerca de quatro em cada cinco moléculas, causando uma mudança no quadro de leitura e um sinal de parada precoce. Apenas uma pequena fração de mensagem normal, e portanto alguma proteína normal, ainda era produzida.
Como uma peça ausente enfraquece a usina de energia
Estudos de proteínas e imagens nas células da pele da paciente revelaram o que essa mensagem defeituosa significava na prática. Os níveis da proteína MRPL42 estavam reduzidos para cerca de um quarto do normal, e a rede mitocondrial parecia mais fragmentada do que em células saudáveis. Levantamentos proteicos detalhados mostraram que muitos blocos de construção do ribossomo mitocondrial — tanto de sua parte grande quanto da pequena — estavam reduzidos, sugerindo que toda a estrutura estava menos estável. Em paralelo, numerosos componentes dos complexos produtores de energia I e IV, e em menor grau do complexo III, estavam diminuídos, enquanto o complexo II permaneceu inalterado. Medições do consumo de oxigênio confirmaram que a capacidade das células de respirar e produzir ATP, a moeda energética celular, estava marcadamente prejudicada.
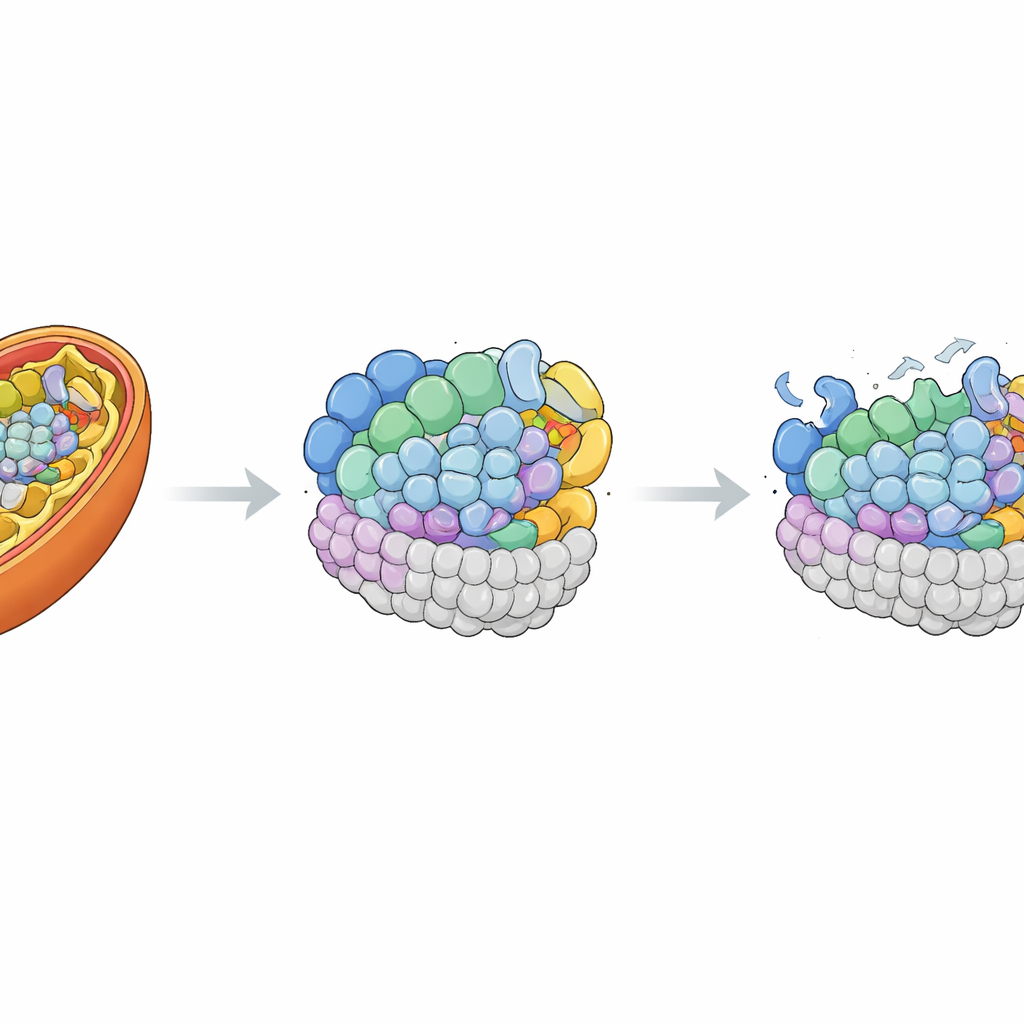
Recolocando a peça ausente
Para provar que o defeito em MRPL42 era de fato responsável, os pesquisadores reintroduziram uma cópia normal do gene nas células da paciente usando um vetor viral inofensivo. Isso elevou os níveis de MRPL42 acima dos observados em células controle e restaurou parcialmente a forma tubular normal da rede mitocondrial. Importante, muitos dos componentes proteicos perdidos do ribossomo mitocondrial e dos complexos I e IV retornaram em direção a quantidades normais. Quando a equipe reavaliou a respiração mitocondrial, constatou que a capacidade máxima de respiração e a capacidade de reserva quase se normalizaram, e o consumo energético básico também melhorou. Esses experimentos de resgate ligaram fortemente os defeitos celulares da criança à escassez de MRPL42 funcional.
O que isso significa para pacientes e para a ciência
No conjunto, o estudo mostra que uma alteração de perda de função bialélica (duas cópias) em MRPL42 pode causar uma doença severa, frequentemente fatal, na qual múltiplos complexos energéticos mitocondriais falham. O gene parece não ser absolutamente essencial — alguma proteína ainda é formada, permitindo que o desenvolvimento alcance o nascimento —, mas é crucial para manter o ribossomo mitocondrial estável o suficiente para sustentar a produção normal de energia. Para as famílias, este trabalho fornece uma explicação molecular para uma doença devastadora e um caminho para aconselhamento genético preciso. Mais amplamente, destaca como a integração profunda de sequenciamento de DNA, análise de RNA e perfil proteico pode revelar novos genes de doença e esclarecer como falhas minúsculas na maquinaria celular repercutem para afetar órgãos inteiros e, em última instância, todo o corpo.
Citação: Boschann, F., Kopp, J., Römer, S. et al. A biallelic MRPL42 variant causes a combined oxidative phosphorylation deficiency syndrome revealed by multi-omics. npj Genom. Med. 11, 20 (2026). https://doi.org/10.1038/s41525-026-00564-1
Palavras-chave: doença mitocondrial, fosforilação oxidativa, proteína ribossomal, multi-ômicas, variante genética