Clear Sky Science · tr
KIMMDY: bir biyomoleküler reaksiyon öykünücüsü
Moleküllerin Bağ Yapmasını ve Kırmasını İzlemek
Yaşam, hücrelerimizde gerçekleşen sayısız küçük kimyasal reaksiyona bağlıdır, ancak bu reaksiyonların ayrıntılı olarak açığa çıkışını gerçekten gözlemek neredeyse imkansızdır. Deneyler yalnızca bulanık ortalamaları görür ve bilgisayar modelleri hem büyük biyomoleküllerin hareketini hem de kimyasal bağların oluşup kırılmasını uzun zaman ölçeklerinde izlemekte zorlanır. Bu makale, reaksiyonun her kuantum ayrıntısını takip etmeye çalışmayan, onun yerine reaksiyonların karmaşık biyolojik ortamlarda nasıl seyredeceğini taklit eden yeni bir simülatör türü olan KIMMDY’yi tanıtıyor. Bu yaklaşım, dokuların stres altında nasıl yaşlandığını, DNA’nın ışık tarafından nasıl hasar gördüğünü ve birbirleriyle yarışan reaksiyon yollarının biyolojiyi nasıl şekillendirdiğini gözlemlemeye olanak tanıyor.
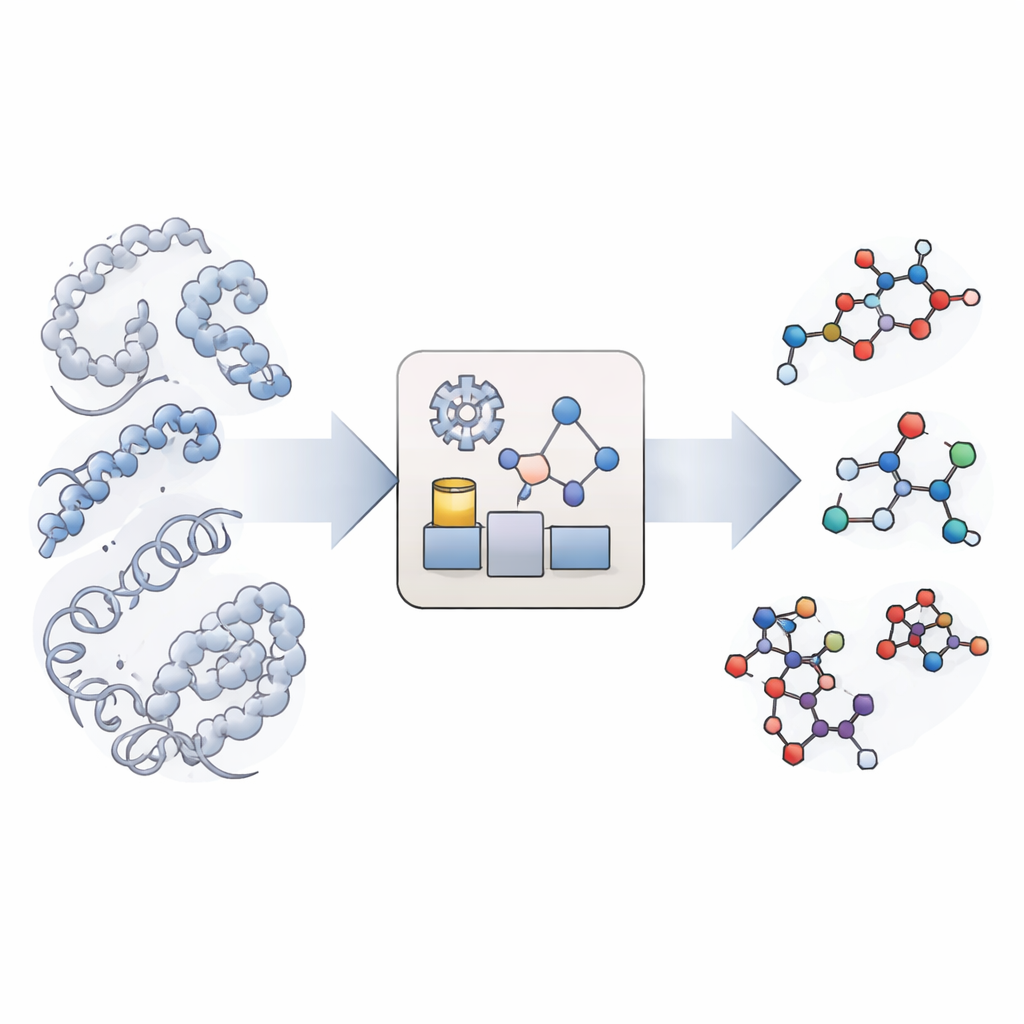
Kimyasal Reaksiyonları Taklit Etmenin Yeni Bir Yolu
Geleneksel moleküler simülasyonlar, proteinler ve DNA gibi büyük biyomoleküllerin nasıl hareket ettiğini ve katlandığını göstermek konusunda mükemmeldir, ancak kimyasal bağları kırılmaz olarak ele alırlar. Gerçekten reaktif simülasyonlar vardır, fakat o kadar hesaplama yoğunlardır ki biyoloji için önemli olan uzun zaman ölçeklerine nadiren ulaşabilirler; özellikle birçok farklı reaksiyon tipi ve bölgesi söz konusuysa. KIMMDY (Kinetic Monte Carlo Molecular Dynamics kısaltması) farklı bir yol izler. Geleneksel simülasyonların moleküler hareketi ele almasına izin verir, ardından reaksiyonların meydana gelebileceği yerleri aramak, bunların ne kadar hızlı gerçekleşeceğini tahmin etmek ve hangi reaksiyonun sırada gerçekleşeceğini rastgele seçmek için ek bir modül kullanır. Hareket, reaksiyon araması ve reaksiyon seçimi döngüsünü tekrar tekrar uygulayarak KIMMDY, tam bir kuantum düzeyinde reaksiyon yolunu hesaplamadan, saniyenin kesirlerinden çok daha uzun zamanlara dek karmaşık reaksiyon kaskadlarını izleyebilir.
Reaksiyon Öykünücüsü Nasıl Çalışır
KIMMDY’nin kalbinde, moleküllerin anlık biçimlerinden reaksiyon hızlarını tahmin eden bir "reaksiyon öykünücüsü" bulunur. Bir moleküler dinamik çalışmasından alınan her anlık görüntü için KIMMDY olası reaksiyon ortaklarını belirler ve her reaksiyon için bariyerin ne kadar yüksek olacağını tahmin etmek üzere farklı modeller kullanır. Birçok durumda, atomları düğümler ve bağları bağlantılar olarak ele alan grafik sinir ağları—önceki yüksek düzey kuantum hesaplamalarına dayalı bariyer yüksekliklerini tahmin eden makine öğrenmesi modelleri—kullanılır. Diğer durumlarda, daha basit fizik temelli formüllere veya deneylerden türetilmiş sezgisel kurallara başvurulur. Bu bariyerlerden hızlar hesaplanır ve bunlar, bir sonraki reaksiyonu rastgele seçen, simüle edilmiş saati ilerleten ve sonraki moleküler hareket turu öncesinde moleküler yapıyı ve kuvvet alanını güncelleyen bir kinetik Monte Carlo adımına beslenir.
Protein İskeletlerinde Radikal Hasarını İzlemek
KIMMDY’nin amaçladığı gibi çalıştığını kontrol etmek için yazarlar önce deneysel verilerin mevcut olduğu küçük organik radikallerdeki basit bir reaksiyon sınıfına uyguladılar. Öykünücü, mutlak hızlarını az tahmin etse bile hangi hidrojen kayma reaksiyonlarının en olası olduğunu yeniden üretti. Ardından çok daha karmaşık bir vaka olan kollajene geçtiler; bağ dokulara güç veren lifli protein. Mekanik gerilim altında kollajendeki bağlar homolitik olarak ayrılabilir ve birbirinden yüksek reaktiviteye sahip radikaller oluşturarak bir zincir boyunca hidrojen atomları aktararak sıçrayabilirler. 2,6 milyon atomlu bir kollajen fibrilinde KIMMDY yüzlerce bu sıçramayı izledi ve radikallerin kökenlerinden birçok nanometre uzağa göç edebildiğini gösterdi. Simülasyonlar, sıra dışı bir çapraz bağın (PYD olarak adlandırılan) ve değiştirilmiş bir amino asidin (DOPA) her ikisinin de son derece etkili radikal tuzakları olarak davrandığını ortaya koydu; bu sonuç, termodinamik hesaplamalar ve önceki elektron spin rezonans spektrumlarının yeniden yorumlanmasıyla desteklendi.
Farklı Reaksiyonlar Yarıştığında
Birçok biyolojik sistem aynı bağı birden fazla şekilde kırabilir; bu ya radikal oluşumuna ya da daha geleneksel "kapalı kabuk" ürünlere yol açar. Örneğin kollajende bir peptid bağı ya iki radikale simetrik olarak ayrılabilir (homoliz) ya da su ile reaksiyona girip dengesiz biçimde ayrılabilir (hidroliz). Gerçekçi bir ortamda her iki seçeneğin doğrudan kuantum simülasyonları uygulamak imkansız olurdu. KIMMDY ile yazarlar, kuvvet destekli homoliz için fiziksel bir modeli ve hidroliz için deney temelli bir sezgi modelini birleştirip bu iki reaksiyonun hem izole bir peptid içinde hem de yoğun bir kollajen fibrilinde birbirleriyle yarışmasına izin verdiler. İzole bir zincirin çekilmesi altında hidrolizin açıkça hakim olduğunu buldular. Ancak kalabalık, çapraz bağlı bir fibrilde mekanik gerilim belirli bölgelerde o kadar yoğunlaşır ki homoliz rekabetçi veya hatta daha hızlı hale gelir; bu da gerçek dokularda radikal oluşumunun neden gözlendiğini açıklar.
Işıkla Tetiklenen Hasar ve DNA’daki Çapraz Bağlar
KIMMDY ayrıca ultraviyole ışığın DNA’yı nasıl değiştirdiğini aydınlatıyor. İki bitişik timin bazı UV fotonlarını absorbe ettiğinde, cilt kanseriyle güçlü şekilde ilişkili bir lezyon olan siklobütan dimerine dönüşebilirler; bu aynı zamanda DNA nanoteknolojisinde zincirleri çapraz bağlamak için de kullanılır. Reaktif bağlar arasındaki mesafe ve açıyı reaksiyon olasılığına bağlayan, küçük molekül deneylerine uyan basit bir geometrik kural kullanarak yazarlar KIMMDY ile çeşitli DNA motifleri için "kuantum verimlerini"—emilen bir foton başına ne sıklıkta bir dimer oluştuğunu—tahmin ettiler. Öykünücü, DNA origamilerde yaygın olarak kullanılan bazı düzenlemelerin, örneğin sarkan diziler ve çapraz geçişlerin, standart çift sarmal veya kesilmiş DNA’ya kıyasla aslında şaşırtıcı derecede düşük verimlere sahip olduğunu tahmin etti. Ayrıca bir dimer oluşmasının yakınında başka bir dimer oluşma olasılığını dramatik biçimde değiştirmediğini öne sürerek, önceki hasarın DNA’yı daha fazla dimer için mutlaka hazırlamadığını ima etti.
Biyoloji ve Tasarım İçin Neden Önemli
Basitçe söylemek gerekirse, KIMMDY canlı maddede kimya için "ya şu olsaydı" senaryolarını hızla ve esnek biçimde oynatmanın bir yolunu sunuyor. Reaksiyonları tam olarak simüle etmek yerine öykünerek, moleküllerin sürekli değişen biçimlerinin hangi reaksiyonların nerede ve ne zaman gerçekleştiğini nasıl etkilediğini hesaba katarken devasa sistemleri ve uzun zaman ölçeklerini ele alabilir. Yöntem, kollajende daha önce gözden kaçmış bir radikal-stabilize edici bölgeyi ortaya çıkarmaya, mekanik kuvvetlerin bağ kırılma yollarının dengesini nasıl kaydırdığını açıklamaya ve ışık altında DNA çapraz bağlarının nasıl ve nerede oluştuğuna dair yeni sorular ortaya koymaya yardımcı oldu. Öykünücü daha fazla reaksiyon türüne ve daha doğru hız modellerine genişledikçe, biyomoleküllerin nasıl yaşlandığını, işlevsizleştiğini veya tıp ve nanoteknoloji için nasıl tasarlanabileceğini anlamada güçlü bir araç olma sözü veriyor.
Atıf: Hartmann, E., Buhr, J., Riedmiller, K. et al. KIMMDY: a biomolecular reaction emulator. Nat Commun 17, 3500 (2026). https://doi.org/10.1038/s41467-026-71955-2
Anahtar kelimeler: biyomoleküler simülasyonlar, reaksiyon kinetiği, moleküler modelleme, DNA hasarı, mekanokimya