Clear Sky Science · nl
KIMMDY: een emulatie van biomoleculaire reacties
Moleculen Zien Bindingen Maken en Breken
Het leven berust op talloze kleine chemische reacties in onze cellen, maar die reacties daadwerkelijk in detail volgen is vrijwel onmogelijk. Experimentele waarnemingen geven alleen vaag gemiddelde beelden, en computermodellen hebben moeite om zowel de beweging van grote biologische moleculen als het maken en breken van chemische bindingen over lange tijden te volgen. Dit artikel introduceert KIMMDY, een nieuw type simulator die niet probeert elk kwantumdetail van een reactie te volgen, maar in plaats daarvan emuleert hoe reacties zich zouden voltrekken in complexe biologische omgevingen. Het biedt een venster op hoe weefsels verouderen onder stress, hoe DNA door licht beschadigd raakt, en hoe concurrerende reactiepaden de biologie vormen.
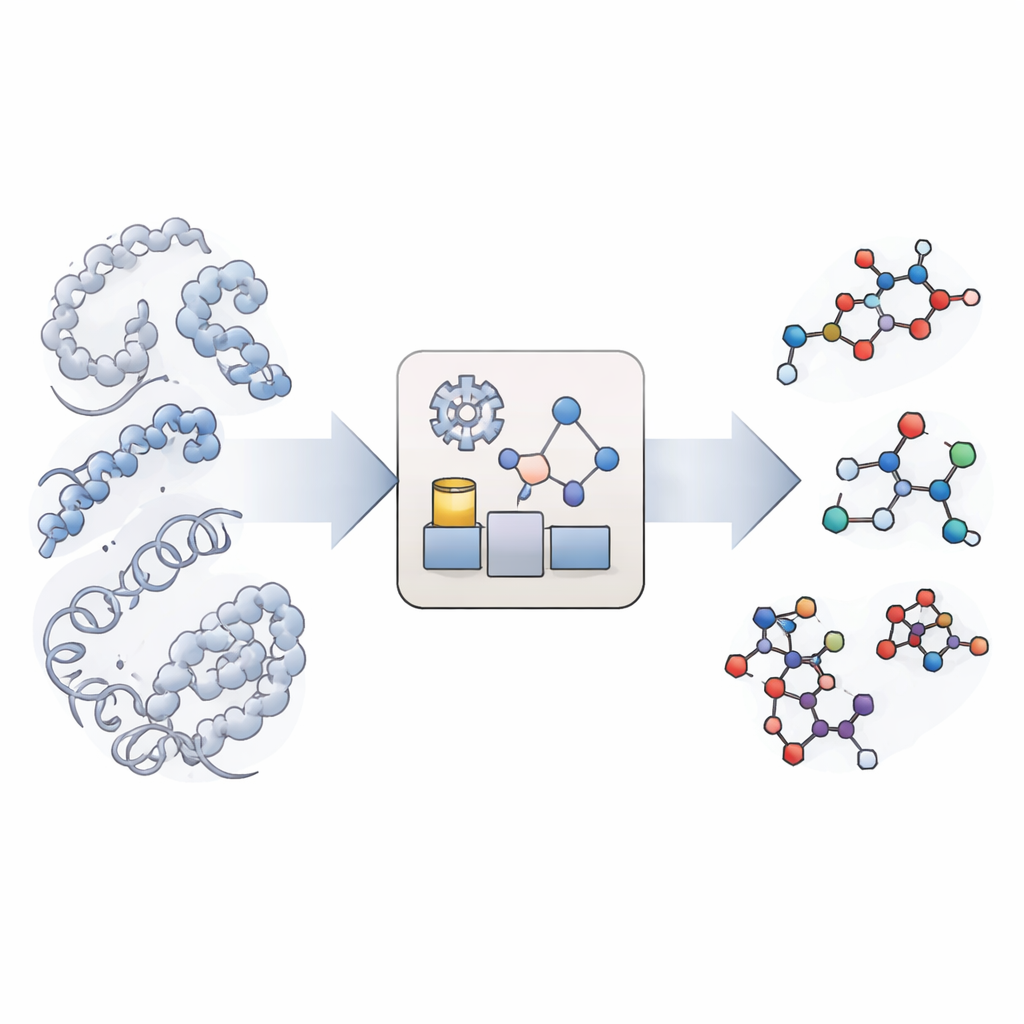
Een Nieuwe Manier om Chemische Reacties na te Bootsen
Traditionele moleculaire simulaties zijn uitstekend in het laten zien hoe grote biomoleculen zoals eiwitten en DNA bewegen en vouwen, maar ze behandelen chemische bindingen als onbreekbaar. Echt reactieve simulaties bestaan wel, maar ze zijn zo rekenkundig intensief dat ze zelden de lange tijdschalen bereiken die relevant zijn voor biologie, vooral wanneer veel verschillende reactietypen en -plaatsen betrokken zijn. KIMMDY (afkorting van Kinetic Monte Carlo Molecular Dynamics) kiest een andere aanpak. Het laat conventionele simulaties de moleculaire beweging afhandelen en gebruikt vervolgens een extra module om plekken te zoeken waar reacties zouden kunnen optreden, te schatten hoe snel ze zouden verlopen, en willekeurig te kiezen welke reactie als volgende plaatsvindt. Door herhaaldelijk cycli van beweging, reactiezorg en reactiekeuze te doorlopen, kan KIMMDY complexe reactiekaskades volgen over tijden van fracties van een seconde tot veel langer, zonder ooit een volledige kwantumniveau-reactieweg uit te rekenen.
Hoe de Reactie-Emulator Werkt
In het hart van KIMMDY staat een "reactie-emulator" die reactietempo's voorspelt op basis van de onmiddellijke vormen van moleculen. Voor elke snapshot uit een moleculaire-dynamica-run identificeert KIMMDY mogelijke reagerende partners en gebruikt het verschillende modellen om te schatten hoe groot de barrière voor elke reactie is. In veel gevallen worden graph neural networks toegepast—machine-learningmodellen die atomen als knopen en bindingen als verbindingen behandelen—om de barrièrehogtes te raden op basis van eerdere hoog-niveau kwantumberekeningen. In andere gevallen valt het terug op eenvoudigere, op de fysica gebaseerde formules of heuristische regels afgeleid van experimenten. Vanuit die barrières berekent het snelheden en voert die in een kinetische Monte Carlo-stap die willekeurig de volgende reactie kiest, de gesimuleerde klok vooruitzet en vervolgens de moleculaire structuur en het krachtveld bijwerkt voordat de volgende ronde van moleculaire beweging begint.
Het Volgen van Radicaalschade in Proteïneschachten
Om te controleren of KIMMDY werkt zoals bedoeld, pasten de auteurs het eerst toe op een eenvoudige klasse van reacties in kleine organische radicalen waarvoor experimentele gegevens beschikbaar zijn. De emulator reproduceerde welke waterstofverschuivingsreacties het meest waarschijnlijk zijn, ook al onderschatte hij hun absolute snelheden. Daarna gingen ze over naar een veel complexer geval: collageen, het fibrillaire eiwit dat bindweefsels hun stevigheid geeft. Onder mechanische stress kunnen bindingen in collageen homolytisch splitsen, waardoor zeer reactieve radicalen ontstaan die van de ene plaats naar de andere hoppen door waterstofatomen langs een keten door te geven. In een collageenfibril van 2,6 miljoen atomen volgde KIMMDY honderden van deze hops en toonde aan dat radicalen vele nanometers van hun oorsprong kunnen migreren. De simulaties onthulden dat een ongebruikelijke crosslink (genoemd PYD) en een gemodificeerd aminozuur (DOPA) beide uitzonderlijk goede radicalenvallen vormen, een conclusie ondersteund door thermodynamische berekeningen en door het herinterpreteren van eerdere elektronen-spinresonantiespectra.
Wanneer Verschillende Reacties Concurrent Zijn
Veel biologische systemen kunnen dezelfde binding op meer dan één manier breken, wat leidt tot ofwel radicaalvorming of tot meer conventionele "gesloten-schil" producten. In collageen bijvoorbeeld kan een peptidebinding symmetrisch in twee radicalen splitsen (homolyse) of met water reageren en ongelijk splitsen (hydrolyse). Directe kwantumsimulaties van beide opties in een realistische omgeving zouden onbetaalbaar zijn. Met KIMMDY combineerden de auteurs een fysisch model voor kracht-ondersteunde homolyse met een heuristisch, op experimenten gebaseerd model voor hydrolyse en lieten de twee reacties concurreren binnen zowel een enkel peptide als een dicht vernet werkend collageenfibril. Ze vonden dat in een geïsoleerde keten onder trekken hydrolyse duidelijk domineert. In een druk, gecrosslinkt fibril concentreert mechanische stress zich echter zo sterk in bepaalde regio's dat homolyse concurrerend of zelfs sneller wordt, wat verklaart waarom radicaalvorming in echte weefsels wordt waargenomen.
Door Licht Aangedreven Schade en Crosslinks in DNA
KIMMDY maakt ook duidelijk hoe ultraviolet licht DNA verandert. Wanneer twee aangrenzende thyminebasen UV absorberen, kunnen ze versmelten tot een cyclobutaan-dimeer, een letsel dat sterk verbonden is met huidkanker maar ook wordt benut om strengen in DNA-nanotechnologie te crosslinken. Met een eenvoudige geometrische regel die afstand en hoek tussen reactieve bindingen relateert aan reactiekans, afgestemd op experimenten met kleine moleculen, gebruikten de auteurs KIMMDY om "quantumyields" te schatten—hoe vaak een dimeer vormt per geabsorbeerd foton—voor verschillende DNA-motieven. De emulator voorspelde dat sommige rangschikkingen die vaak in DNA-origami worden gebruikt, zoals overhangen en kruisingen, eigenlijk verrassend lage yields hebben vergeleken met standaard dubbelstrengs of genikte DNA. Hij suggereerde ook dat het vormen van één dimeer de kans op het vormen van een andere in de buurt niet dramatisch verandert, wat impliceert dat eerdere schade DNA niet per definitie voorbereidt op verdere dimeervorming.
Waarom Dit Belangrijk is voor Biologie en Ontwerp
Simpel gezegd biedt KIMMDY een snelle, flexibele manier om "wat-als" scenario's voor chemie binnen levende materie uit te spelen. Door reacties te emuleren in plaats van volledig te simuleren, kan het enorme systemen en lange tijdschalen aan terwijl het toch rekening houdt met hoe de voortdurend veranderende vormen van moleculen beïnvloeden welke reacties waar en wanneer plaatsvinden. De methode hielp een eerder over het hoofd geziene radicaal-stabiliserende plek in collageen aan het licht te brengen, verduidelijkte hoe mechanische krachten het evenwicht tussen bond-breekpaden verschuiven, en riep nieuwe vragen op over hoe en waar DNA-crosslinks onder licht ontstaan. Naarmate de emulator wordt uitgebreid naar meer reactietypen en nauwkeurigere snelheidsmodellen, belooft hij een krachtig instrument te worden om te begrijpen hoe biomoleculen verouderen, verkeerd functioneren of kunnen worden ontworpen voor geneeskunde en nanotechnologie.
Bronvermelding: Hartmann, E., Buhr, J., Riedmiller, K. et al. KIMMDY: a biomolecular reaction emulator. Nat Commun 17, 3500 (2026). https://doi.org/10.1038/s41467-026-71955-2
Trefwoorden: biomoleculaire simulaties, reactiekinetiek, moleculair modelleren, DNA-schade, mechanochemie