Clear Sky Science · tr
Hücresel komşu tercih yöntemlerinin nicel doku analizi için karşılaştırılması ve optimizasyonu
Hücre komşuları neden önemli
Vücudumuz rastgele dağılmış hücrelerden değil, hareketli hücre mahallelerinden oluşur. Hangi hücrelerin hangi hücrelerin yanında olduğu, bir tümörün nasıl büyüdüğünü, bir yaranın nasıl iyileştiğini veya bir kalbin kalp krizi sonrası nasıl toparlandığını etkileyebilir. Bu makale, aldatıcı derecede basit bir soruyu gündeme getiriyor: bilim insanları doku görüntülerinde hangi hücre tiplerinin birbirine yakın olma eğiliminde olduğunu ölçtüklerinde, kullandıkları farklı yöntemler ne kadar güvenilir ve daha iyi yapabilir miyiz?
Bilim insanları hücresel şehir haritasını nasıl okuyor
Modern görüntüleme ve uzamsal genomik teknolojileri, bir doku kesitindeki binlerce hücrenin tam konumunu ve kimliğini kaydedebilir. Bu verileri analiz etmenin yaygın bir yolu “komşu tercihleri” hesaplamaktır: belirli bir hücre tipi A için, rastgele beklenene kıyasla ne sıklıkla hücre tipi B yakın komşu olarak bulunuyor? Bu görev için halihazırda birçok yazılım aracı var, ancak bunlar ince farklı adımlara dayanır. Yazarlar bunları üç temel seçeneğe ayırıyor: her hücrenin etrafındaki mahalleyi nasıl tanımlamak (örneğin, yakındaki hücreler arasında kenar çizmek veya sabit bir mesafe kullanmak), komşuları nasıl saymak (A–B çiftini B–A ile aynı mı saymak veya A’dan B’ye yönü B’den A’ya ayırmak), ve bu sayımları nihai bir puana nasıl dönüştürmek (basit normalleştirilmiş sayımlar, permutasyon temelli istatistikler veya makine öğrenimi ölçüleri). Bu ortak çerçeve, yöntemlerin adil bir şekilde yan yana karşılaştırılmasını sağlar.
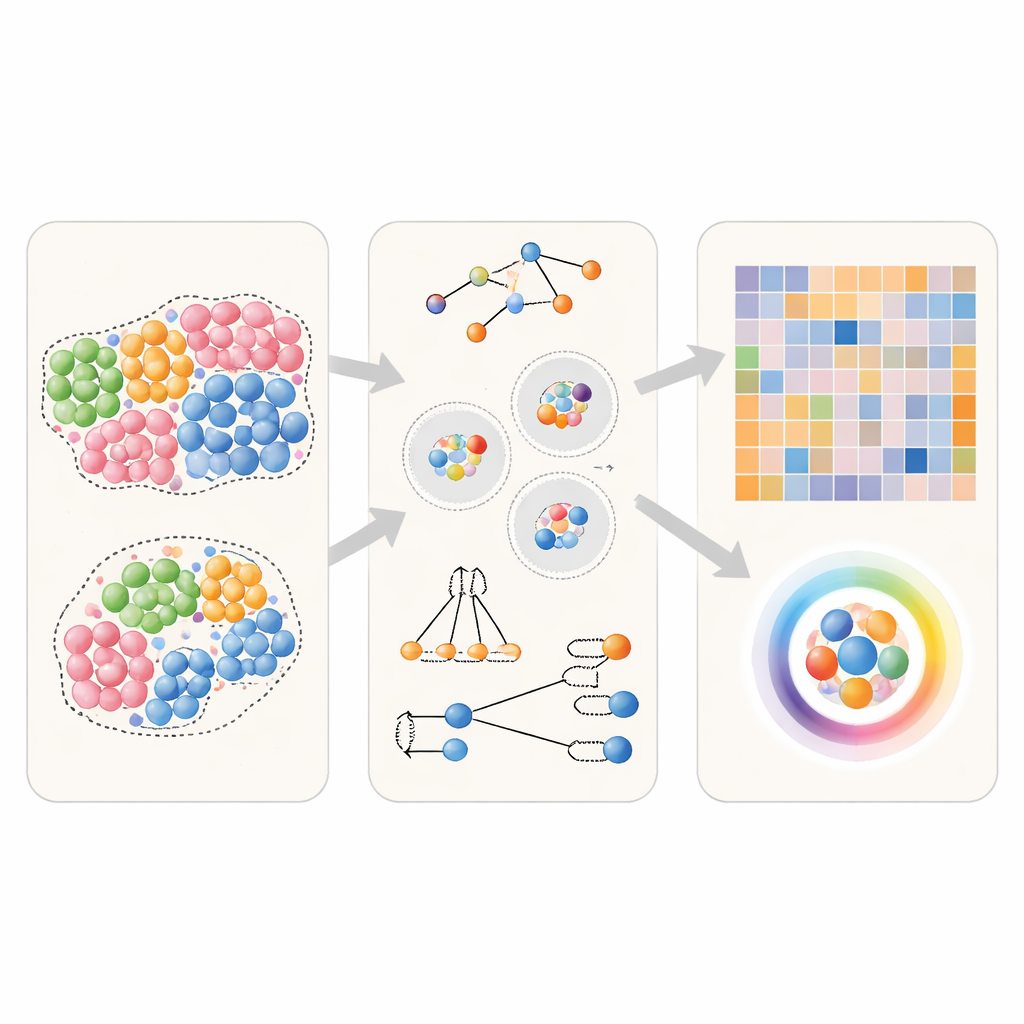
Sanal dokularda komşu yöntemlerinin test edilmesi
Farklı yaklaşımların ne kadar iyi performans gösterdiğini görmek için ekip önce gerçek komşuluk ilişkilerinin önceden bilindiği bilgisayar tarafından üretilmiş dokular kullandı. Belirli bir hücre tipinin ya hiçbir özel tercihi olmadığı, kendi türünü hafifçe tercih ettiği ya da güçlü şekilde kümeleştiği basit senaryolar yarattılar. Ayrıca bir hücre tipinin diğerine tercihli olarak yaklaştığı, ancak tersine olmadığını gösteren yönlü durumları da simüle ettiler. Bu sanal dokuları kullanarak, yazarlar aynı verileri birkaç yaygın araçla besledi ve sonra sordular: her yöntem bu senaryoları güvenilir şekilde ayırabiliyor mu ve hangi hücre tipinin hangi komşuyu aradığını doğru şekilde yeniden çıkarabiliyor mu?
Yön ve inceliği yakalamak neden zor
Karşılaştırma, neredeyse tüm yöntemlerin dokudaki büyük, açık farkları tespit edebildiğini gösterdi. Ancak iki önemli zayıflık ortaya çıktı. Birincisi, bazı araçlar çıktılarını kaba, üç seviyeli puanlara sıkıştırıyor (örneğin “rastgelein altında”, “fark yok” veya “rastgelein üzerinde”), bu da zayıf bir komşu tercihini güçlü olandan ayırmayı zorlaştırıyor. İkincisi, birçok yöntem belirli bir hücrenin diğer tip ile hiç karşılaşıp karşılaşmadığına bakmaksızın, verilen bir türdeki tüm hücreler üzerinde komşu sayımlarını ortalıyor. Bu “toplam ortalama” yönselliği bulanıklaştırma eğiliminde olup, A’dan B’ye olan ilişkiyi B’den A’ya benzeyecek şekilde gösteriyor; oysa yalnızca tek yönde gerçekten bir tercih olabilir. Sonuç olarak, mevcut araçlar özellikle bir hücre tipi nadir ve diğeri yaygın olduğunda hücresel infiltrasyonun görünür yönünü olduğundan az gösterebilir veya tersine çevirebilir.
Yönlü komşuları puanlamak için yeni bir yol
Bu sorunları ele almak için yazarlar koşullu z-puanı veya COZI adını verdikleri yeni bir puanlama şeması tanıtıyor. COZI, gözlenen komşu sayımlarını dokunun birçok rastgeleleştirilmiş versiyonuyla karşılaştırma fikrini koruyor, ancak sayımların nasıl ortalandığını değiştiriyor: yalnızca en az bir B hücresiyle gerçekten temas eden A tipi hücreleri dikkate alıyor. Bu “koşullu” odaklanma, yönselliği geri kazanmak için hayati önemde oluyor. COZI sonra sonucu, gözlenen desenin rastgele beklentiden ne kadar saptığını yansıtan sürekli bir z-puanına dönüştürüyor. Puanları yorumlamayı kolaylaştırmak için yazarlar eşlik eden bir ölçü, koşullu hücre oranını (CCR) ekliyor; bu, A tipi hücrelerin hangi oranının A–B mahallesine katıldığını basitçe rapor ediyor. Z-puanı ve CCR birlikte yalnızca mekansal ilişkinin ne kadar güçlü olduğunu değil, aynı zamanda bunun birkaç özelleşmiş hücre tarafından mı yoksa doku organizasyonunda geniş bir kayma ile mi yönlendirildiğini de ortaya koyuyor.
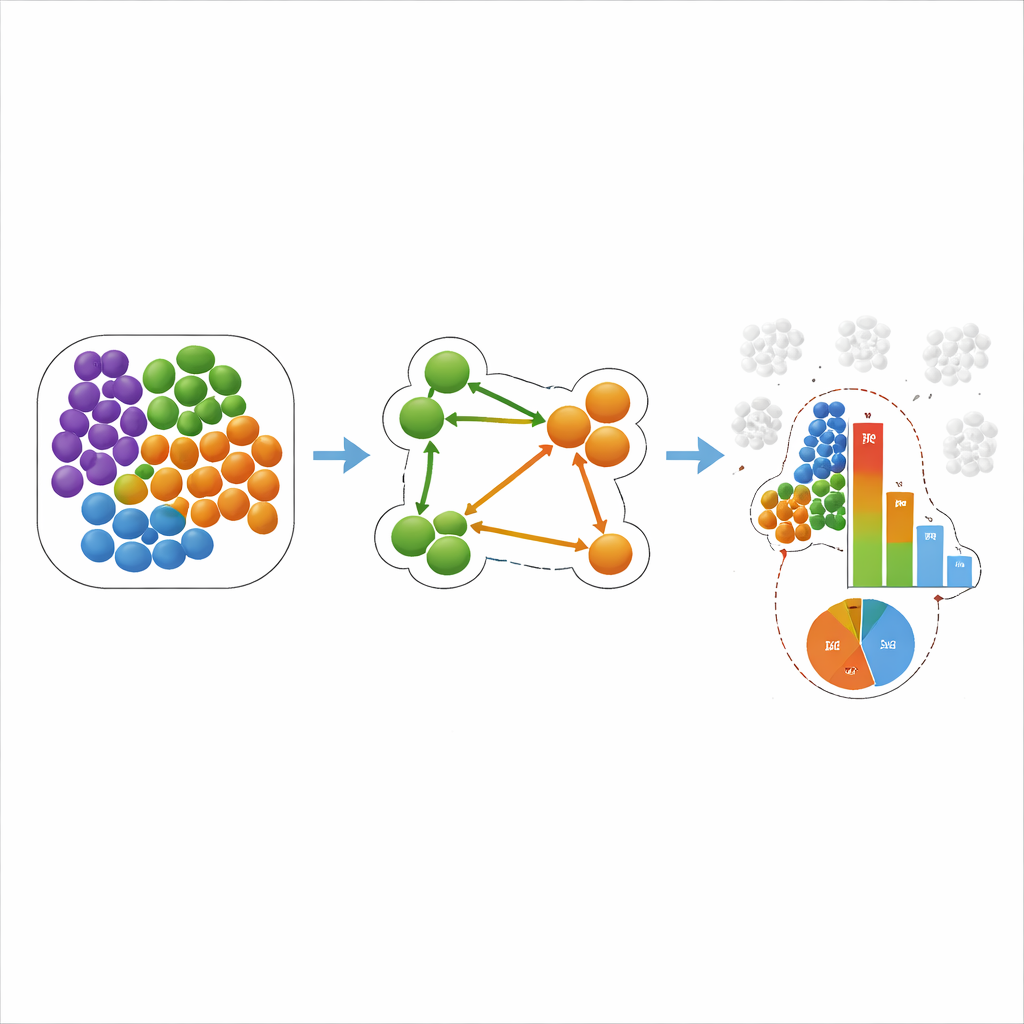
Bu, kanser ve kalp hastalığı için ne anlama geliyor
Ekip daha sonra COZI ve diğer yöntemleri iki gerçek dünya veri setine uyguladı. Üçlü-negatif meme kanseri çalışmasında, önceki çalışmalar immün hücrelerin ve tümör hücrelerinin karışma biçimlerine göre tümörleri “soğuk”, “karışık” ve “kompartımanlı” olarak gruplandırmıştı. COZI bu gruplamaları yalnızca yeniden üretmekle kalmadı, aynı zamanda yönlü desenleri de ortaya çıkardı: örneğin bazı tümörlerde bağışıklık hücreleri kendi aralarında kümelenme eğilimindeyken, bir alt küme tümör hücresi bu ceplere uzanıyordu; diğerlerinde ise immün hücreler tümör bölgelerine sızan taraf oluyordu. Bir fare kalp krizi modelinde COZI, nötrofillerin ve monositlerin önce ventrikülün iç yüzeyi aracılığıyla, ardından yaralı bölgenin daha derinlerine nasıl ilerlediğini izledi. Önemli olarak, hücre sayılarına dair küresel değişimleri, kimin kimin komşusu olduğunu ve hangi yönde olduğunu gösteren gerçek değişimlerden ayırdı.
Alınacak ders
Bu çalışma, hücre mahallelerini okuyan tüm araçların eşit yaratılmadığını ve küçük algoritmik tercihlerin biyolojik sonuçları güçlü şekilde şekillendirebileceğini gösteriyor. Mevcut yöntemlerin nasıl çalıştığını açıklığa kavuşturarak ve COZI ile koşullu hücre oranını tanıtarak yazarlar, uzamsal doku verilerinde komşu analizlerini seçme ve yorumlama için bir yol haritası sunuyor. Uzman olmayanlar için ana fikir şudur: dokudaki “şehir”de kimin kimin yanında yaşadığını — ve kimin kimin bölgesine doğru ilerlediğini — doğru araçlarla ölçüldüğü sürece hastalığın erken işaretlerini, terapiye yanıtları ve hedefe yönelik tedavi yollarını ortaya çıkarabilir.
Atıf: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Anahtar kelimeler: uzamsal omikler, hücre mahalleleri, tümör mikroçevresi, immün hücre infiltrasyonu, hesaplamalı patoloji