Clear Sky Science · sv
Jämförelse och optimering av metoder för cellnära preferenser vid kvantitativ vävnadsanalys
Varför cellgrannar spelar roll
Våra kroppar består av livliga cellgrannskap, inte av slumpmässigt utspridda celler. Vilka celler som ligger intill varandra kan påverka hur en tumör växer, hur ett sår läker eller hur hjärtat återhämtar sig efter en hjärtinfarkt. Denna artikel ställer en bedrägligt enkel fråga: när forskare mäter vilka celltyper som tenderar att befinna sig nära varandra i vävnadsbilder, hur tillförlitliga är de olika metoderna de använder, och kan vi göra det bättre?
Hur forskare läser den cellulära stadskartan
Moderna avbildnings- och spatiala genomikmetoder kan registrera exakt position och identitet för tusentals celler i en vävnadsskiva. Ett vanligt sätt att analysera dessa data är att beräkna ”grannpreferenser”: för en given celltyp A, hur ofta har den celltyp B som närmaste granne jämfört med vad som skulle förväntas av en slump? Många mjukvaruverktyg finns redan för denna uppgift, men de bygger på subtilt olika steg. Författarna bryter ner dessa i tre kärnval: hur ett grannskap runt varje cell definieras (till exempel genom att dra kanter mellan närliggande celler eller använda ett fast avstånd), hur grannar räknas (behandla ett par A–B som samma som B–A, eller skilja riktningen från A till B respektive B till A), och hur dessa räkningar omvandlas till ett slutligt mått (enkla normaliserade räkningar, permutationsbaserad statistik eller maskininlärningsmått). Detta gemensamma ramverk möjliggör en rättvis, sida‑vid‑sida‑jämförelse av metoder.
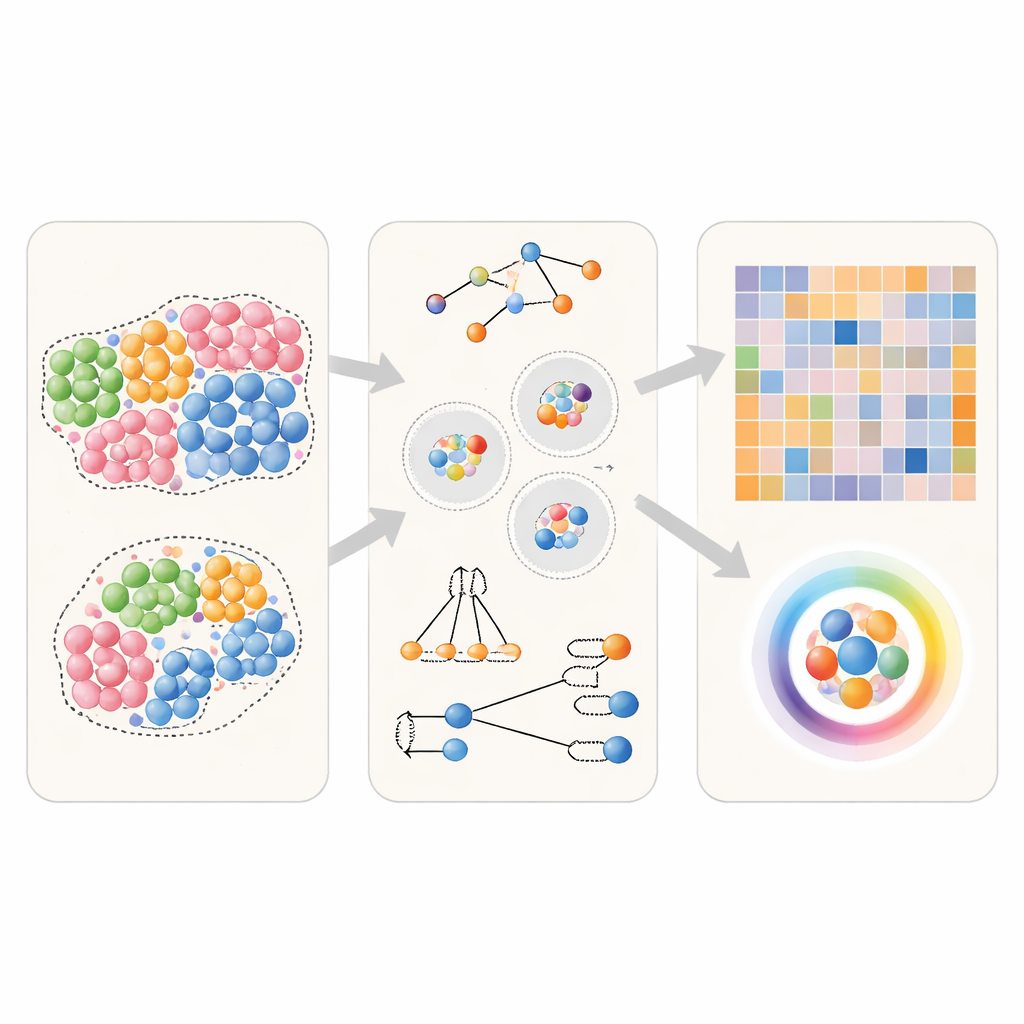
Test av grannmetoder i virtuella vävnader
För att se hur väl olika tillvägagångssätt presterar använde teamet först datorgenererade vävnader där de sanna grannskapsrelationerna är kända i förväg. De skapade enkla scenarier där en viss celltyp antingen inte hade någon särskild preferens, svagt föredrog sin egen typ eller starkt klustrade med sig själv. De simulerade också riktade situationer där en celltyp föredrar att ligga intill en annan, men inte tvärtom. Med dessa virtuella vävnader matade författarna identiska data till flera allmänt använda verktyg och ställde sedan frågan: kan varje metod pålitligt särskilja dessa scenarier, och kan den korrekt återfinna vilken celltyp som söker vilken granne?
Varför riktning och subtilitet är svåra att fånga
Jämförelsen visade att nästan alla metoder kan upptäcka stora, uppenbara skillnader i vävnadsorganisation. Dock framträdde två viktiga svagheter. För det första komprimerar vissa verktyg sitt output till grova, tregradiga poäng (till exempel ”under slump”, ”ingen skillnad” eller ”över slump”), vilket gör det svårt att skilja en svag grannpreferens från en stark. För det andra medelvärdesbildar många metoder grannräkningar över alla celler av en viss typ, oavsett om en viss cell någonsin möter den andra typen eller inte. Denna ”totala medelvärdesbildning” tenderar att sudda ut riktning, vilket gör relationen från A till B liknande den från B till A, även när endast en riktning faktiskt visar en preferens. Som ett resultat kan befintliga verktyg underskatta eller till och med vända den uppenbara riktningen för cellinfiltration, särskilt när en celltyp är sällsynt och den andra är riklig.
Ett nytt sätt att poängsätta riktade grannar
För att hantera dessa problem introducerar författarna ett nytt poängsystem kallat det villkorade z‑poänget, eller COZI. COZI behåller idén att jämföra observerade grannräkningar med många slumpade versioner av vävnaden, men ändrar hur räkningarna medelvärdesbildas: den betraktar endast celler av typ A som faktiskt vidrör minst en cell av typ B. Detta ”villkorade” fokus visar sig vara avgörande för att återfinna riktningen. COZI omvandlar sedan resultatet till ett kontinuerligt z‑poäng, vilket speglar hur starkt det observerade mönstret avviker från slumpförväntan. För att göra poängen lättare att tolka lägger författarna till ett komplementärt mått, det villkorade cellförhållandet (CCR), som helt enkelt rapporterar vilken andel av cellerna av typ A som alls deltar i A–B‑grannskapet. Tillsammans avslöjar z‑poänget och CCR inte bara hur stark en rumslig relation är, utan också om den drivs av ett fåtal specialiserade celler eller av en bred förändring i vävnadsorganisation.
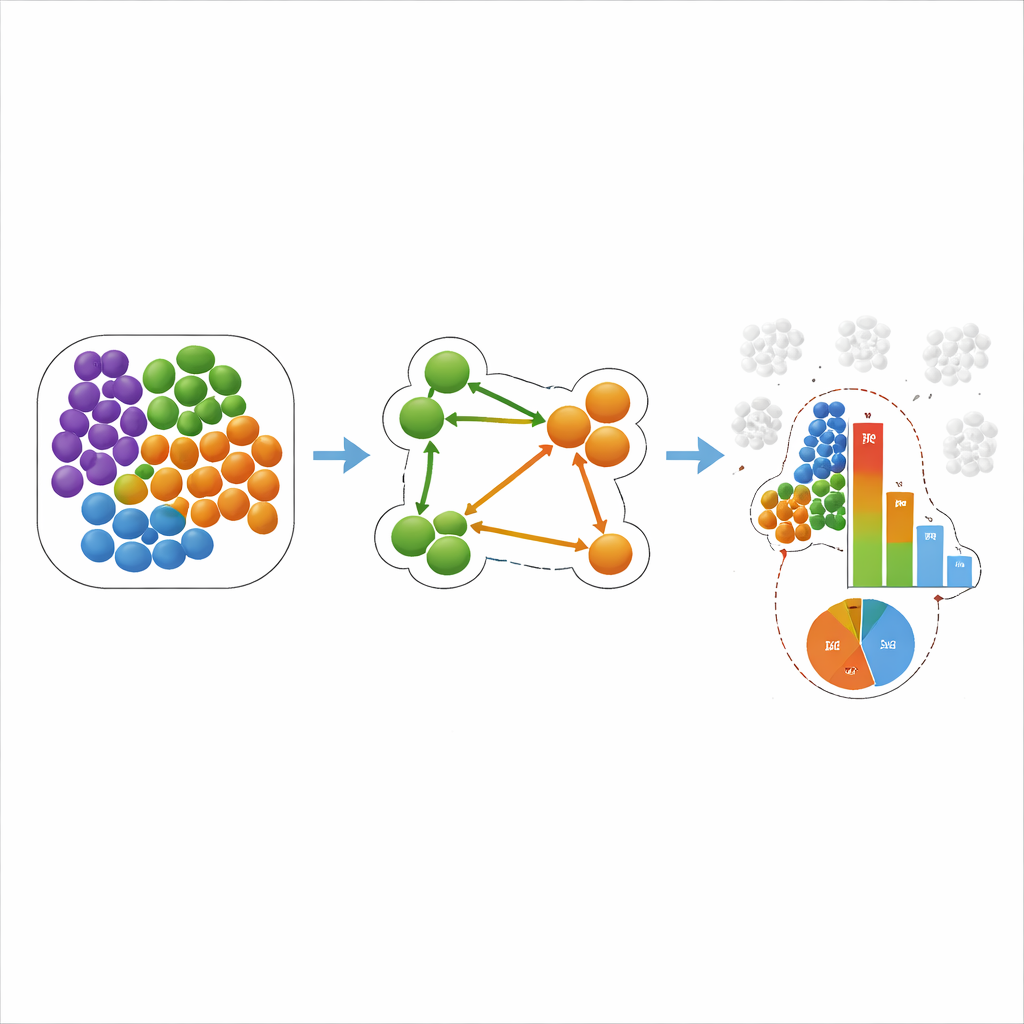
Vad detta betyder för cancer och hjärtsjukdom
Teamet tillämpade sedan COZI och andra metoder på två verkliga dataset. I en studie av trippelnegativ bröstcancer hade tidigare arbete grupperat tumörer i ”kalla”, ”blandade” och ”kompartmentaliserade” utifrån hur immunceller och tumörceller blandade sig. COZI återgav inte bara dessa grupperingar utan avslöjade också riktade mönster: till exempel i vissa tumörer tenderade immunceller att klustra bland sig medan en undergrupp av tumörceller sträckte sig in i dessa fickor, medan i andra var det immuncellerna som infiltrerade tumörområden. I en musmodell för hjärtinfarkt följde COZI hur neutrofiler och monocyter successivt trängde in i den skadade hjärtmuskeln, först genom kammarfodrets inre beklädnad och sedan djupare in i det skadade området. Viktigt är att metoden separerade globala förändringar i cellantal från verkliga förändringar i vem som är grannar med vem och i vilken riktning.
Sammanfattande budskap
Denna studie visar att inte alla verktyg för att läsa cellgrannskap är likvärdiga, och att små algoritmiska val kan starkt påverka biologiska slutsatser. Genom att klargöra hur befintliga metoder fungerar och introducera COZI tillsammans med det villkorade cellförhållandet erbjuder författarna en färdplan för att välja och tolka grannskapsanalyser i spatiala vävnadsdata. För icke‑specialister är huvudidén att förstå vem som bor granne med vem i vävnadens ”stad” — och vem som flyttar in på vems territorium — kan avslöja tidiga tecken på sjukdom, svar på behandling och vägar för riktad behandling, förutsatt att dessa mönster mäts med rätt verktyg.
Citering: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Nyckelord: spatiell omik, cellgrannskap, tumörmikromiljö, infiltration av immunceller, beräkningspatologi