Clear Sky Science · nl
Vergelijking en optimalisatie van methoden voor voorkeur van cellulaire buren voor kwantitatieve weefselanalyse
Waarom cellulaire buren ertoe doen
Ons lichaam bestaat uit levendige buurten van cellen, niet uit willekeurige verspreiding. Welke cellen naast elkaar liggen kan beïnvloeden hoe een tumor groeit, hoe een wond geneest of hoe een hart herstelt na een hartinfarct. Dit artikel stelt een schijnbaar eenvoudige vraag: wanneer wetenschappers meten welke celtypen de neiging hebben dicht bij elkaar te zitten in weefselbeelden, hoe betrouwbaar zijn de verschillende methoden die zij gebruiken, en kunnen we het beter doen?
Hoe wetenschappers de cellulaire stadskaart lezen
Moderne beeldvormings- en spatiale genomica-technologieën kunnen de exacte positie en identiteit van duizenden cellen in een weefselsnee vastleggen. Een veelgebruikte manier om deze gegevens te analyseren is het berekenen van “buurvoorkeuren”: voor een gegeven celtype A, hoe vaak heeft het celtype B als nabije buur vergeleken met wat je door toeval zou verwachten? Er bestaan al veel softwaretools voor deze taak, maar ze vertrouwen op subtiel verschillende stappen. De auteurs splitsen deze op in drie kernkeuzes: hoe een buurt rond elke cel te definiëren (bijvoorbeeld door randen te tekenen tussen nabijgelegen cellen of een vaste afstand te gebruiken), hoe buren te tellen (een paar A–B hetzelfde behandelen als B–A of richting van A naar B onderscheiden versus B naar A), en hoe deze tellingen om te zetten in een eindscoor (eenvoudig genormaliseerde tellingen, op permutaties gebaseerde statistieken of machine-learningmaatregelen). Dit gemeenschappelijke raamwerk maakt een eerlijke, naast elkaar staande vergelijking van methoden mogelijk.
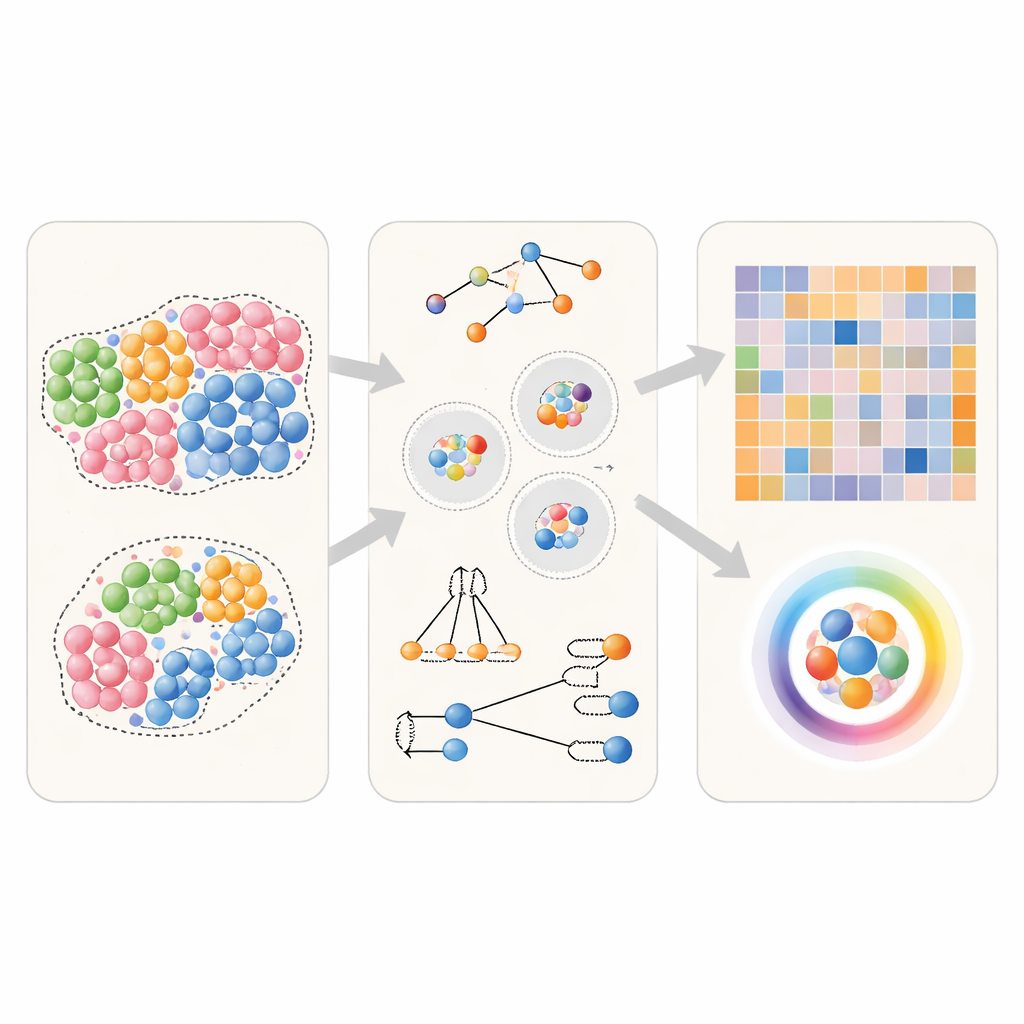
Het testen van buurmethoden in virtuele weefsels
Om te zien hoe goed verschillende benaderingen presteren, gebruikte het team eerst computergestuurde weefsels waarbij de werkelijke buurrelaties van tevoren bekend zijn. Ze creëerden eenvoudige scenario’s waarin een bepaald celtype geen speciale voorkeur heeft, lichtjes de eigen soort prefereert, of sterk in clusters met zichzelf voorkomt. Ook simuleerden ze directionele situaties waarin het ene celtype zich bij voorkeur dicht tegen een ander aanschuift, maar niet andersom. Met deze virtuele weefsels voeden de auteurs identieke gegevens aan meerdere veelgebruikte tools en stelden dan de vraag: kan elke methode deze scenario’s betrouwbaar onderscheiden, en kan ze correct achterhalen welk celtype welke buur zoekt?
Waarom richting en subtiliteit lastig vast te leggen zijn
De vergelijking toonde aan dat bijna alle methoden grote, duidelijke verschillen in weefselorganisatie kunnen detecteren. Er kwamen echter twee belangrijke zwakheden naar voren. Ten eerste comprimeren sommige tools hun output tot grove, driedelige scores (bijvoorbeeld “onder random”, “geen verschil” of “boven random”), wat het moeilijk maakt een zwakke buurvoorkeur te onderscheiden van een sterke. Ten tweede middelen veel methoden buurentellingen over alle cellen van een gegeven type, ongeacht of een specifieke cel ooit het andere type ontmoet. Dit “totale middelen” heeft de neiging richting te vervagen, waardoor de relatie van A naar B lijkt op die van B naar A, zelfs wanneer slechts één richting daadwerkelijk een voorkeur toont. Hierdoor kunnen bestaande tools de schijnbare richting van celinfiltratie onderschatten of zelfs omkeren, vooral wanneer het ene celtype zeldzaam is en het andere veel voorkomt.
Een nieuwe manier om directionele buren te scoren
Om deze problemen aan te pakken, introduceren de auteurs een nieuwe scoringsmethode genaamd de conditionele z-score, of COZI. COZI behoudt het idee om waargenomen buurentellingen te vergelijken met vele gerandomiseerde versies van het weefsel, maar verandert hoe de tellingen worden gemidddeld: het beschouwt alleen cellen van type A die daadwerkelijk ten minste één cel van type B aanraken. Deze “conditionele” focus blijkt cruciaal om richting te herstellen. COZI zet het resultaat vervolgens om in een continue z-score, die weergeeft hoe sterk het waargenomen patroon afwijkt van de verwachte random situatie. Om de scores makkelijker interpreteerbaar te maken, voegen de auteurs een aanvullende maat toe, de conditionele celratio (CCR), die eenvoudig rapporteert welk aandeel van cellen van type A überhaupt deelneemt aan de A–B-buurt. Samen onthullen de z-score en CCR niet alleen hoe sterk een ruimtelijke relatie is, maar ook of deze wordt gedreven door een paar gespecialiseerde cellen of door een brede verschuiving in weefselorganisatie.
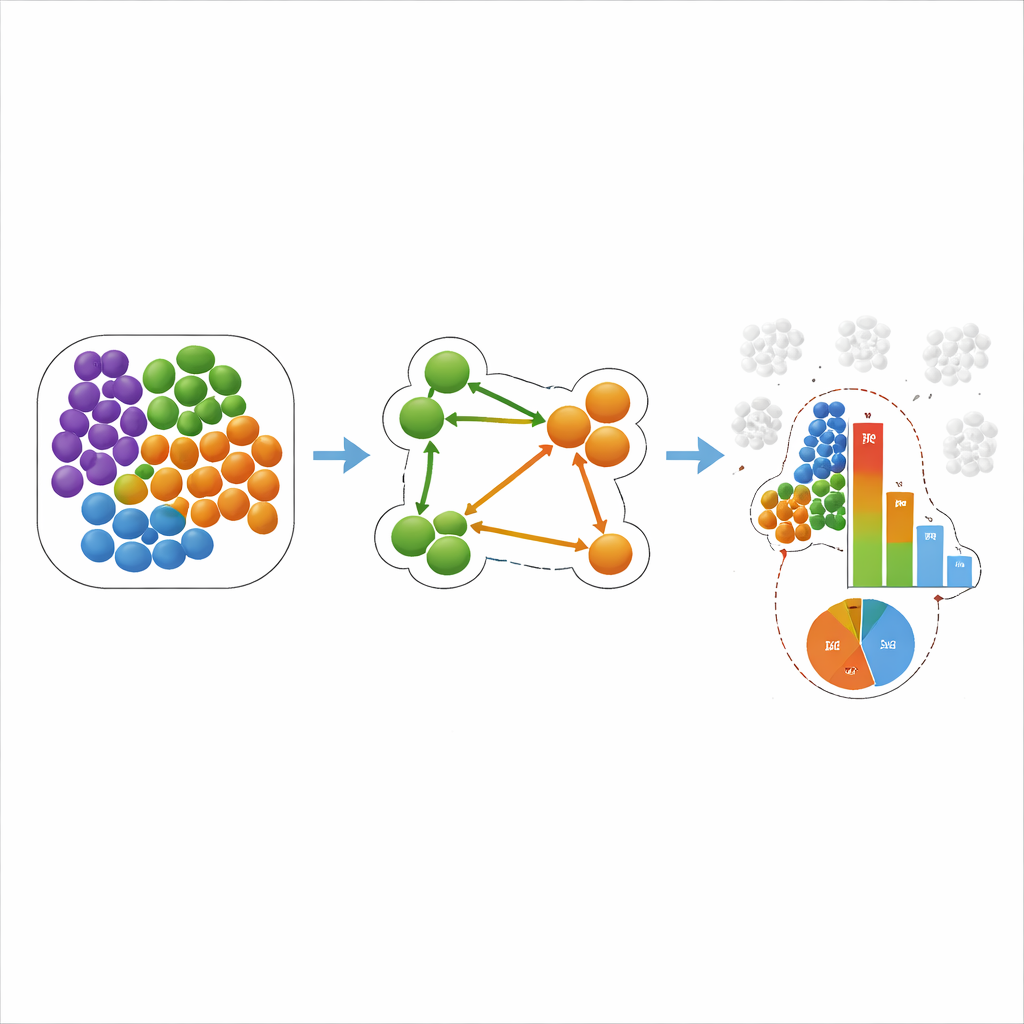
Wat dit betekent voor kanker en hartziekten
Het team paste vervolgens COZI en andere methoden toe op twee datasets uit de praktijk. In een studie naar triple-negatieve borstkanker hadden eerdere onderzoeken tumoren ingedeeld als “koud”, “gemengd” en “gecompartimenteerd” op basis van hoe immuuncellen en kankercellen door elkaar heen zaten. COZI reproduceerde niet alleen deze indelingen, maar bracht ook directionele patronen aan het licht: bijvoorbeeld, in sommige tumoren neigden immuuncellen ertoe onderling te clusteren terwijl een subset van kankercellen in deze pockets doordrong, terwijl in andere gevallen de immuuncellen juist de tumorgebieden infiltreerden. In een muismodel van een hartinfarct volgde COZI hoe neutrofielen en monocyten geleidelijk het beschadigde hartspierweefsel binnendrongen, eerst via de binnenbekleding van de hartkamer en daarna dieper in de aangetaste zone. Belangrijk is dat het globale verschuivingen in cel aantallen onderscheidde van echte veranderingen in wie wie als buur heeft en in welke richting.
Belangrijkste boodschap
Deze studie laat zien dat niet alle tools om celbuurten te lezen gelijk zijn, en dat kleine algoritmische keuzes biologische conclusies sterk kunnen vormen. Door te verduidelijken hoe bestaande methoden werken en COZI plus de conditionele celratio te introduceren, bieden de auteurs een stappenplan voor het kiezen en interpreteren van buuranalyses in ruimtelijke weefselgegevens. Voor niet-specialisten is het kernidee dat begrijpen wie naast wie woont in de weefsel-"stad" — en wie het territorium van wie betreedt — vroege tekenen van ziekte, reacties op therapie en routes voor gerichte behandeling kan onthullen, mits die patronen met de juiste tools worden gemeten.
Bronvermelding: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Trefwoorden: spatiële omica, celbuurten, tumormicro-omgeving, infiltratie van immuuncellen, computationale pathologie