Clear Sky Science · ru
Сравнение и оптимизация методов оценки предпочтений клеточных соседей для количественного анализа тканей
Почему важны клеточные соседи
Наши тела состоят не из случайно разбросанных клеток, а из оживлённых «районов». То, какие клетки находятся рядом друг с другом, может влиять на рост опухоли, заживление раны или восстановление сердца после инфаркта. В этой статье ставится кажущаяся простой задача: когда учёные измеряют, какие типы клеток склонны соседствовать в изображениях тканей, насколько надёжны разные применяемые методы и можно ли их улучшить?
Как учёные читают карту клеточного города
Современные методы визуализации и пространственной геномики фиксируют точное положение и тип тысяч клеток на срезе ткани. Популярный способ анализа таких данных — вычисление «предпочтений соседства»: для заданного типа клеток A как часто рядом оказывается тип B в сравнении с ожиданием случайного распределения? Существует много программных инструментов для этой задачи, но они опираются на слегка разные подходы. Авторы выделяют три ключевых выбора: как определить окрестность вокруг каждой клетки (например, связывая ближайшие клетки рёбрами или используя фиксированный радиус), как учитывать соседей (приравнивать пару A–B к B–A или различать направление от A к B и от B к A) и как переводить эти подсчёты в итоговую оценку (нормализованные счёты, статистика на основе перестановок или методы машинного обучения). Эта общая схема позволяет честно сравнить методы «бок о бок».
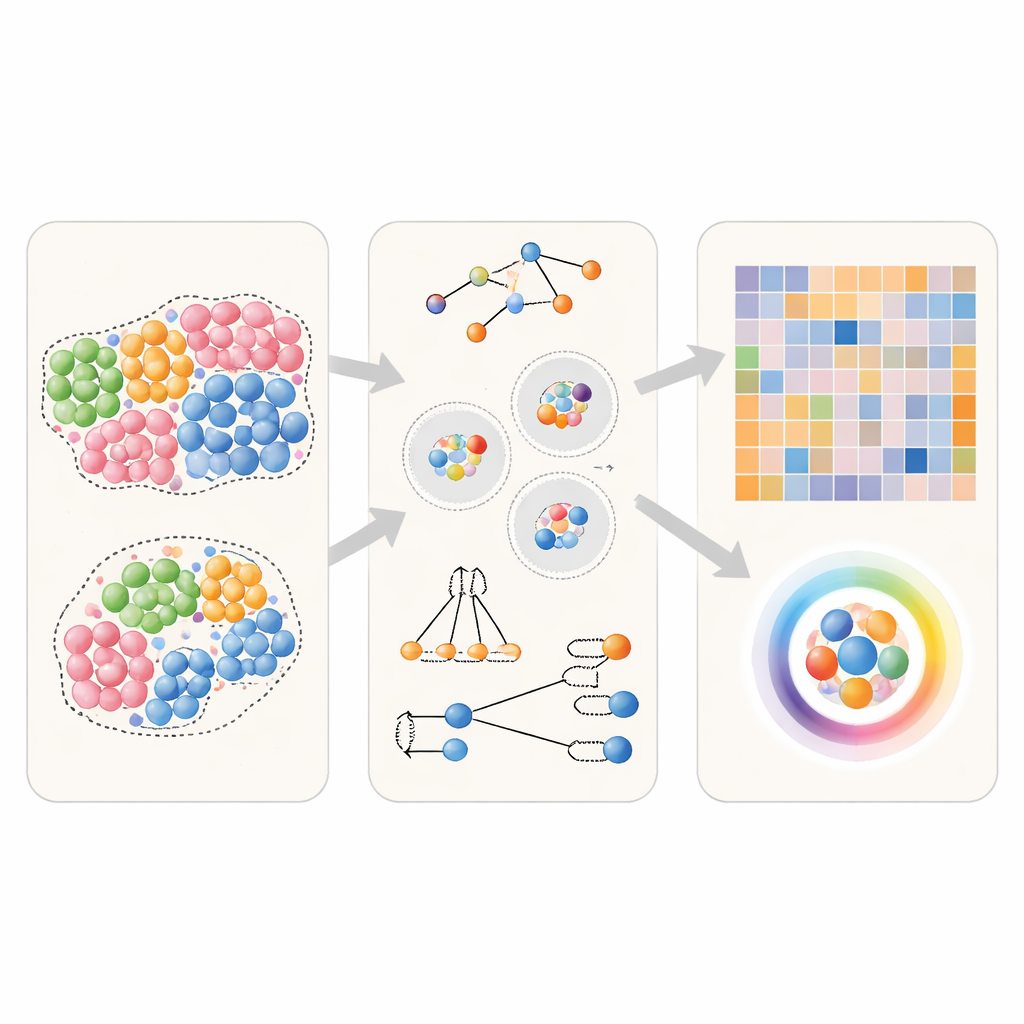
Тестирование методов соседства в виртуальных тканях
Чтобы проверить, как разные подходы работают, команда сначала использовала сгенерированные компьютером ткани, в которых истинные соседские отношения были известны заранее. Они создали простые сценарии, где определённый тип клеток либо не имеет особых предпочтений, либо слабо предпочитает своих сородичей, либо сильно кластеризуется. Также смоделировали направленные ситуации, в которых один тип клеток предпочитает подходить к другому, но не наоборот. Используя эти виртуальные ткани, авторы подали одинаковые данные в несколько широко используемых инструментов и спросили: может ли каждый метод надёжно отличать эти сценарии и правильно выявить, какой тип клеток стремится к какому соседу?
Почему сложно уловить направление и тонкие сигналы
Сравнение показало, что почти все методы способны обнаружить крупные, очевидные различия в организации ткани. Однако выявились два ключевых недостатка. Во‑первых, некоторые инструменты сводят результат к грубым трёхуровневым категориям (например, «ниже случайного», «без разницы» или «выше случайного»), что затрудняет различение слабого предпочтения от сильного. Во‑вторых, многие методы усредняют количество соседей по всем клеткам данного типа, независимо от того, встречается ли конкретная клетка с другим типом вообще. Такое «полное усреднение» размывает направленность, делая отношения от A к B похожими на отношения от B к A, даже когда предпочтение реально только в одном направлении. В результате существующие инструменты могут недооценивать или даже инвертировать кажущееся направление клеточной инфильтрации, особенно если один тип клеток редок, а другой — многочисленен.
Новый способ оценки направленных соседств
Чтобы устранить эти проблемы, авторы предлагают новую схему оценки, называемую условным z‑баллом, или COZI. COZI сохраняет идею сравнения наблюдаемых счётов соседства с множеством рандомизированных версий ткани, но меняет способ усреднения: учитываются только те клетки типа A, которые фактически контактируют как минимум с одной клеткой типа B. Такое «условное» внимание оказывается решающим для восстановления направленности. COZI затем переводит результат в непрерывный z‑балл, который отражает, насколько сильно наблюдаемая картина отличается от случайного ожидания. Чтобы упростить интерпретацию, авторы вводят вспомогательную меру — условное соотношение клеток (CCR), которое просто показывает, какую долю клеток типа A вообще вовлекают в соседство A–B. Вместе z‑балл и CCR показывают не только силу пространственной связи, но и то, вызвана ли она несколькими специализированными клетками или широким изменением в организации ткани.
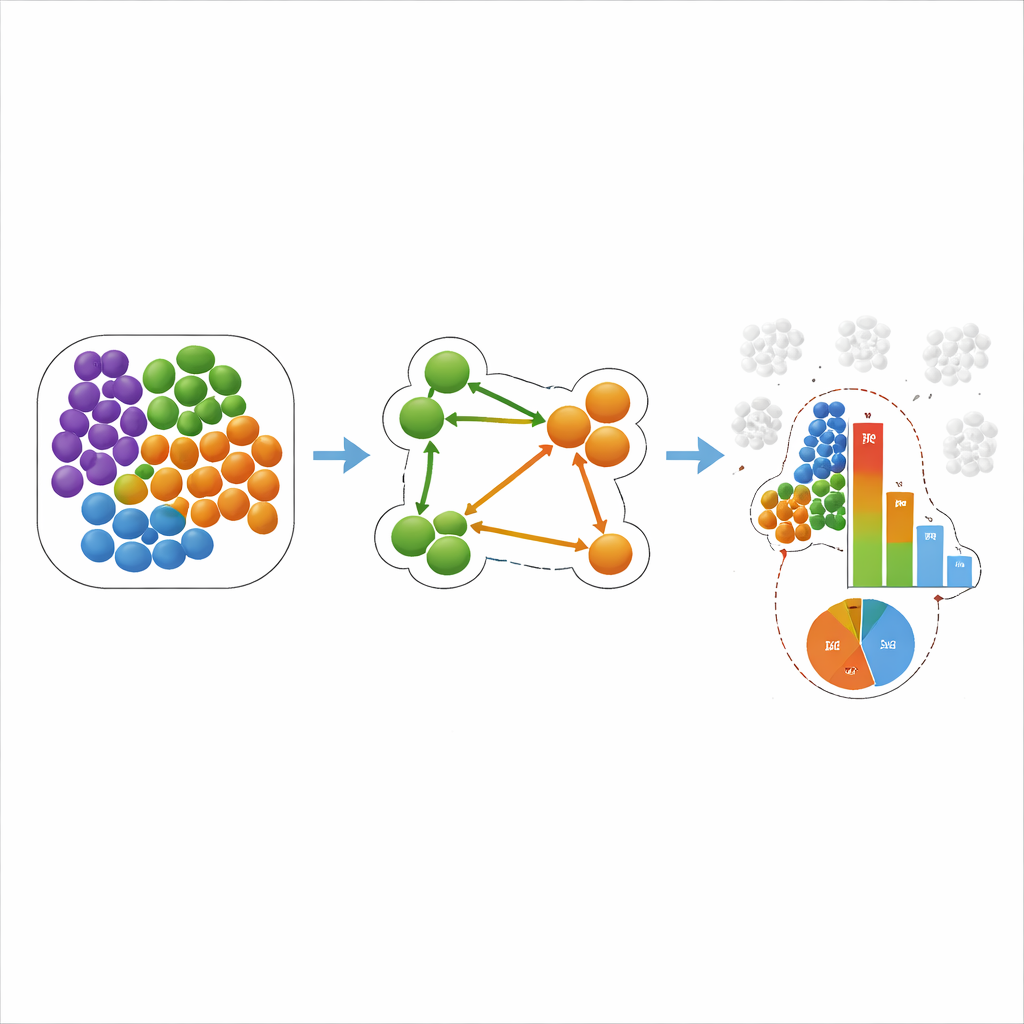
Что это значит для рака и сердечных болезней
Затем команда применила COZI и другие методы к двум реальным наборам данных. В исследовании трёхнегативного рака молочной железы предыдущие работы распределяли опухоли на «холодные», «смешанные» и «компартментализованные» в зависимости от того, как иммунные и опухолевые клетки переплетались. COZI не только воспроизвёл эти группы, но и выявил направленные паттерны: например, в одних опухолях иммунные клетки склонялись к кластеризации между собой, а часть опухолевых клеток проникала в эти «карманы», тогда как в других именно иммунные клетки инфильтрировали опухолевые области. В модели инфаркта у мышей COZI проследил, как нейтрофилы и моноциты постепенно входили в повреждённый сердечный мышечный слой — сначала через внутреннюю выстилку желудочка, затем глубже в зону повреждения. Важно, что метод отдельно выделял глобальные сдвиги в численности клеток и истинные изменения в том, кто соседствует с кем и в каком направлении.
Вывод
Это исследование показывает, что не все инструменты для чтения клеточных соседств одинаковы, и что мелкие алгоритмические решения могут существенно повлиять на биологические выводы. Прояснив работу существующих методов и представив COZI вместе с условным соотношением клеток, авторы предлагают дорожную карту для выбора и интерпретации анализов соседств в пространственных данных по тканям. Для неспециалистов ключевая мысль такова: понимание того, кто живёт рядом с кем в тканевом «городе» — и кто вторгается в чью территорию — может выявлять ранние признаки болезни, ответы на лечение и пути для таргетной терапии, но только если подобные паттерны измеряются с помощью подходящих инструментов.
Цитирование: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Ключевые слова: пространственная омics, клеточные соседства, микроокружение опухоли, инфильтрация иммунных клеток, вычислительная патология