Clear Sky Science · pl
Porównanie i optymalizacja metod określania preferencji sąsiedztwa komórek dla ilościowej analizy tkanek
Dlaczego sąsiedztwo komórek ma znaczenie
Nasze ciało składa się z tętniących życiem „dzielnic” komórek, a nie z przypadkowego rozsypania. To, które komórki siedzą obok których, może wpływać na to, jak rośnie guz, jak goi się rana lub jak serce regeneruje się po zawale. W artykule zadano na pozór proste pytanie: gdy naukowcy mierzą, które typy komórek mają tendencję do bycia blisko siebie na obrazach tkanek, na ile wiarygodne są stosowane metody i czy można je ulepszyć?
Jak naukowcy czytają mapę komórkowego miasta
Nowoczesne technologie obrazowania i genomiki przestrzennej potrafią zapisać dokładne położenie i tożsamość tysięcy komórek w przekroju tkanki. Popularnym sposobem analizy tych danych jest obliczanie „preferencji sąsiedztwa”: dla danego typu komórek A, jak często ma on typ komórek B jako bliskiego sąsiada w porównaniu z oczekiwaniem losowym? Istnieje już wiele narzędzi programowych do tego zadania, ale opierają się one na nieco różnych krokach. Autorzy rozbijają proces na trzy podstawowe wybory: jak zdefiniować sąsiedztwo wokół każdej komórki (na przykład przez rysowanie krawędzi między pobliskimi komórkami lub stosowanie stałego odcinka), jak zliczać sąsiadów (traktując parę A–B tak samo jak B–A, lub rozróżniając kierunek od A do B versus od B do A) oraz jak przekształcić te zliczenia w ostateczny wynik (proste znormalizowane zliczenia, statystyki oparte na permutacjach lub miary uczenia maszynowego). To wspólne ramowanie pozwala na uczciwe porównanie metod „jak obok siebie”.
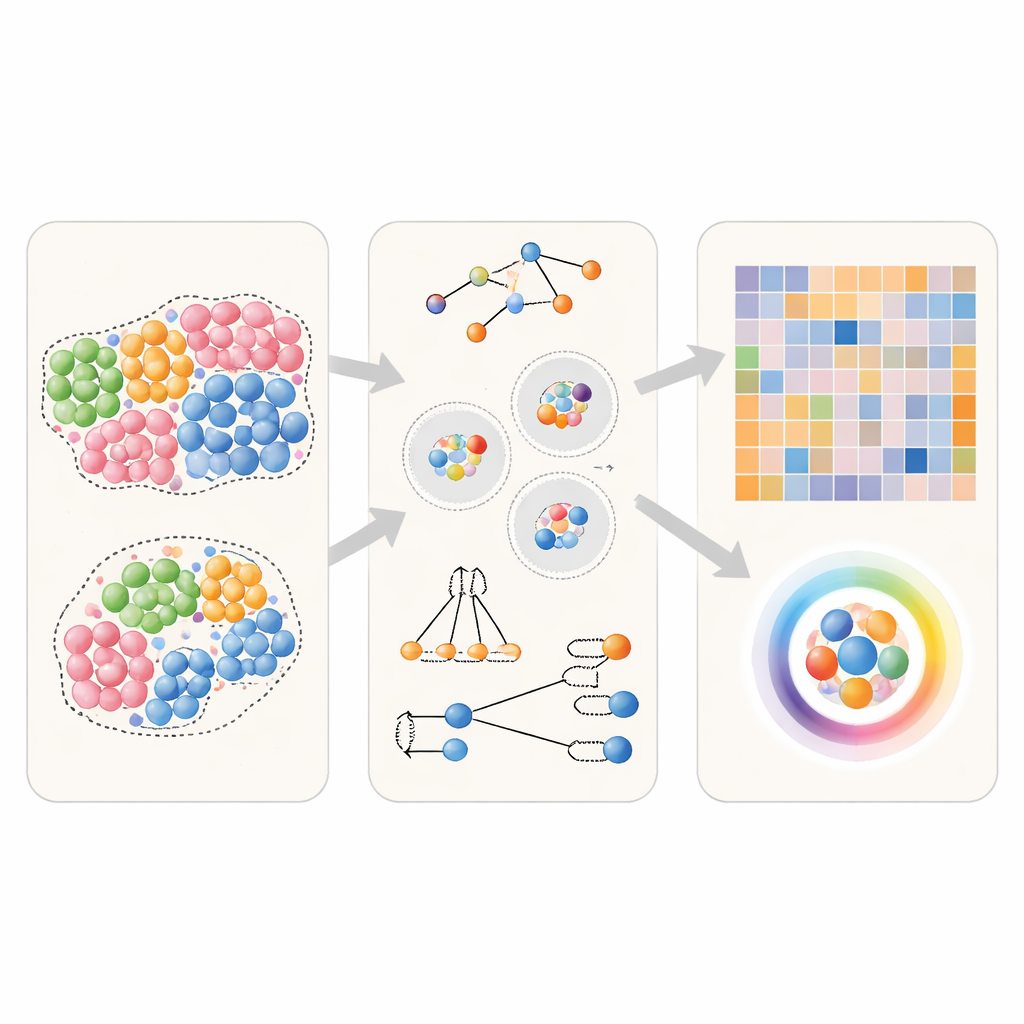
Testowanie metod sąsiedztwa w wirtualnych tkankach
Aby ocenić skuteczność różnych podejść, zespół najpierw użył komputerowo generowanych tkanek, gdzie prawdziwe relacje sąsiedztwa są znane z góry. Stworzono proste scenariusze, w których dany typ komórek albo nie ma specjalnych preferencji, lekko preferuje własny rodzaj, albo silnie zlepia się w skupiska. Symulowano też sytuacje kierunkowe, w których jeden typ komórek preferencyjnie przytula się do innego, ale nie odwrotnie. Korzystając z tych wirtualnych tkanek, autorzy wprowadzili identyczne dane do kilku powszechnie używanych narzędzi i sprawdzili: czy każda metoda potrafi wiarygodnie odróżnić te scenariusze i czy potrafi poprawnie odkryć, który typ komórki „szuka” którego sąsiada?
Dlaczego kierunkowość i subtelności trudno uchwycić
Porównanie wykazało, że prawie wszystkie metody potrafią wykryć duże, oczywiste różnice w organizacji tkanki. Jednak pojawiły się dwie kluczowe słabości. Po pierwsze, niektóre narzędzia kompresują wynik do grubych, trzystopniowych ocen (na przykład „poniżej losowego”, „brak różnicy” lub „powyżej losowego”), co utrudnia rozróżnienie słabej preferencji sąsiedztwa od silnej. Po drugie, wiele metod uśrednia zliczenia sąsiadów po wszystkich komórkach danego typu, niezależnie od tego, czy dana komórka w ogóle spotykała komórki innego typu. To „całkowite uśrednianie” ma tendencję do zamazywania kierunkowości, sprawiając, że relacja od A do B wygląda podobnie jak od B do A, nawet gdy tylko jeden kierunek faktycznie wykazuje preferencję. W efekcie istniejące narzędzia mogą zaniżać lub nawet odwracać pozorny kierunek naciekania komórek, zwłaszcza gdy jeden typ komórki jest rzadki, a drugi jest liczny.
Nowy sposób oceny kierunkowych sąsiadów
Aby rozwiązać te problemy, autorzy wprowadzają nową miarę nazwaną warunkowym z-score’em, czyli COZI. COZI zachowuje ideę porównywania obserwowanych zliczeń sąsiedztwa z wieloma losowymi wersjami tkanki, ale zmienia sposób uśredniania zliczeń: bierze pod uwagę tylko te komórki typu A, które faktycznie stykają się przynajmniej z jedną komórką typu B. To „warunkowe” skupienie się okazuje się kluczowe dla odtworzenia kierunkowości. COZI następnie przekształca wynik w ciągły z-score, który odzwierciedla, jak mocno obserwowany wzorzec odbiega od oczekiwania losowego. Aby ułatwić interpretację wyników, autorzy dodają miarę towarzyszącą, warunkowy stosunek komórek (CCR), który po prostu informuje, jaka część komórek typu A uczestniczy w ogóle w sąsiedztwie A–B. Razem z-score i CCR ujawniają nie tylko jak silna jest relacja przestrzenna, ale także czy jest ona napędzana przez kilka wyspecjalizowanych komórek, czy przez szeroki przemieszczenie w organizacji tkanki.
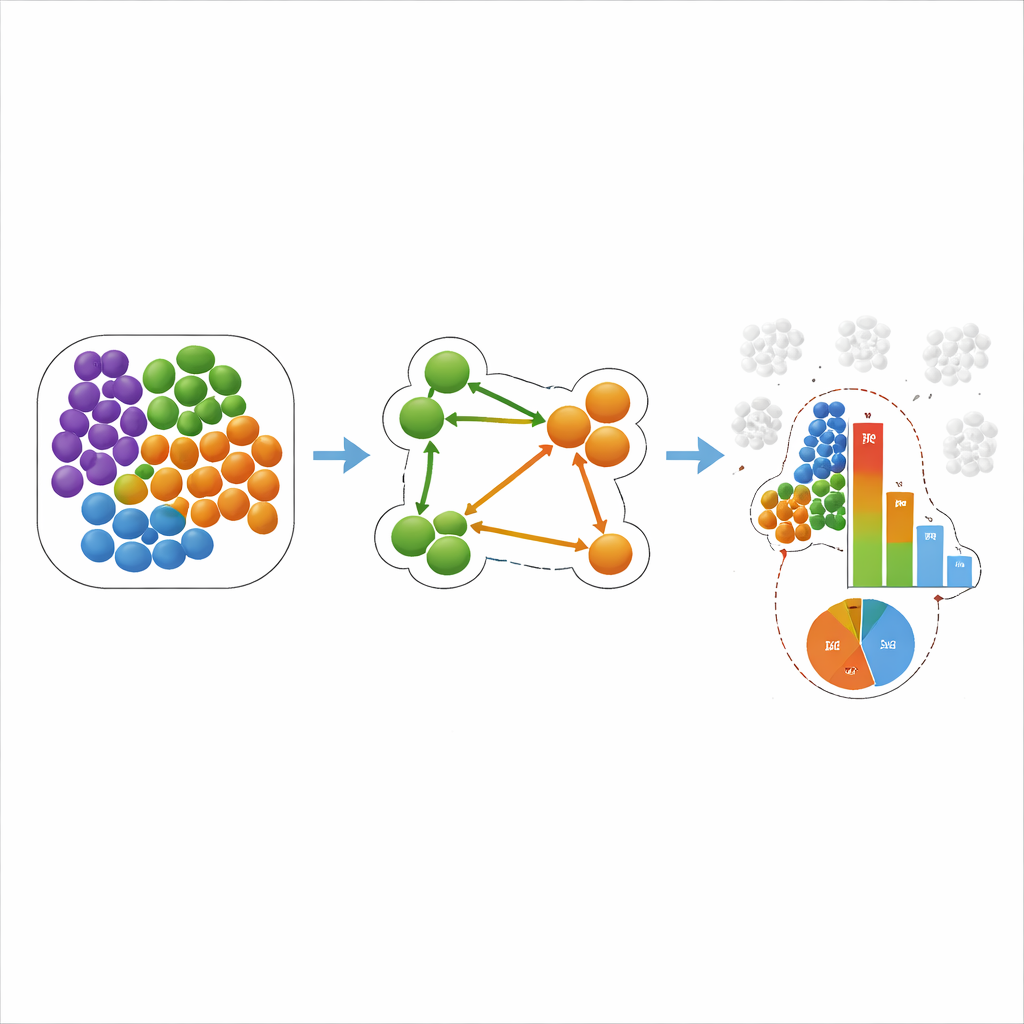
Co to znaczy dla raka i chorób serca
Zespół następnie zastosował COZI i inne metody do dwóch rzeczywistych zbiorów danych. W badaniu raka piersi potrójnie ujemnego wcześniejsze prace grupowały guzy na „zimne”, „mieszane” i „skompartamentalizowane” na podstawie tego, jak komórki odpornościowe i komórki nowotworowe się mieszały. COZI nie tylko odtworzył te grupowania, lecz także ujawnił wzorce kierunkowe: na przykład w niektórych guzach komórki odpornościowe miały tendencję do gromadzenia się wśród siebie, podczas gdy podzbiór komórek nowotworowych wdzierał się w te kieszenie, natomiast w innych to komórki odpornościowe nacierały na obszary guza. W modelu myszy po zawale serca COZI śledził, jak neutrofile i monocyty stopniowo wnikały w uszkodzoną tkankę serca, najpierw przez wewnętrzną wyściółkę komory, a potem głębiej w strefę urazu. Co ważne, rozdzielił globalne zmiany liczebności komórek od prawdziwych zmian w tym, kto jest czyim sąsiadem i w którym kierunku.
Wniosek
Badanie pokazuje, że nie wszystkie narzędzia do odczytywania sąsiedztw komórek są stworzone równo i że drobne decyzje algorytmiczne mogą silnie kształtować biologiczne wnioski. Poprzez wyjaśnienie, jak działają istniejące metody, oraz wprowadzenie COZI wraz z warunkowym stosunkiem komórek, autorzy dostarczają mapę drogową do wyboru i interpretacji analiz sąsiedztwa w danych przestrzennych tkanek. Dla laików kluczowa myśl jest taka, że zrozumienie, kto mieszka obok kogo w „miescie” tkanki — i kto wtargnął na czyje terytorium — może ujawnić wczesne oznaki choroby, odpowiedzi na leczenie i drogi do terapii celowanej, pod warunkiem że te wzorce mierzy się właściwymi narzędziami.
Cytowanie: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Słowa kluczowe: spatial omics, sąsiedztwa komórkowe, mikrootoczenie guza, naciekanie komórek odpornościowych, patologia obliczeniowa