Clear Sky Science · de
Vergleich und Optimierung von Methoden zur Bestimmung zellulärer Nachbarschaftspräferenzen für die quantitative Gewebeanalyse
Warum Zellnachbarn wichtig sind
Unser Körper besteht aus lebhaften Zellnachbarschaften, nicht aus willkürlichen Verteilungen. Welche Zellen nebeneinander sitzen, kann beeinflussen, wie ein Tumor wächst, wie eine Wunde heilt oder wie sich das Herz nach einem Infarkt erholt. Dieser Artikel stellt eine auf den ersten Blick einfache Frage: Wenn Forschende in Gewebebildern messen, welche Zelltypen typischerweise nahe beieinander vorkommen, wie zuverlässig sind die verschiedenen verwendeten Methoden und lässt sich das verbessern?
Wie Forschende die zelluläre Stadtkarte lesen
Moderne Bildgebung und räumliche Genomik-Technologien können die exakte Position und Identität von Tausenden Zellen in einem Gewebeschnitt erfassen. Eine verbreitete Analyse ist die Berechnung von „Nachbarschaftspräferenzen“: Für einen Zelltyp A, wie häufig hat er Zelltyp B als nahen Nachbarn im Vergleich zu dem, was zufällig zu erwarten wäre? Für diese Aufgabe existieren bereits viele Softwarewerkzeuge, die jedoch in feinen Details voneinander abweichen. Die Autorinnen und Autoren zerlegen diese Unterschiede in drei Kernentscheidungen: wie eine Nachbarschaft um jede Zelle definiert wird (beispielsweise durch Kanten zwischen nahe beieinanderliegenden Zellen oder über einen festen Abstand), wie Nachbarn gezählt werden (ein Paar A–B wie B–A behandeln oder die Richtung A→B gegenüber B→A unterscheiden) und wie diese Zählungen in einen Endscore überführt werden (einfache normalisierte Zählungen, permutationsbasierte Statistik oder maschinelle Lernmaße). Dieses gemeinsame Rahmenwerk ermöglicht einen fairen, nebeneinander gestellten Vergleich der Methoden.
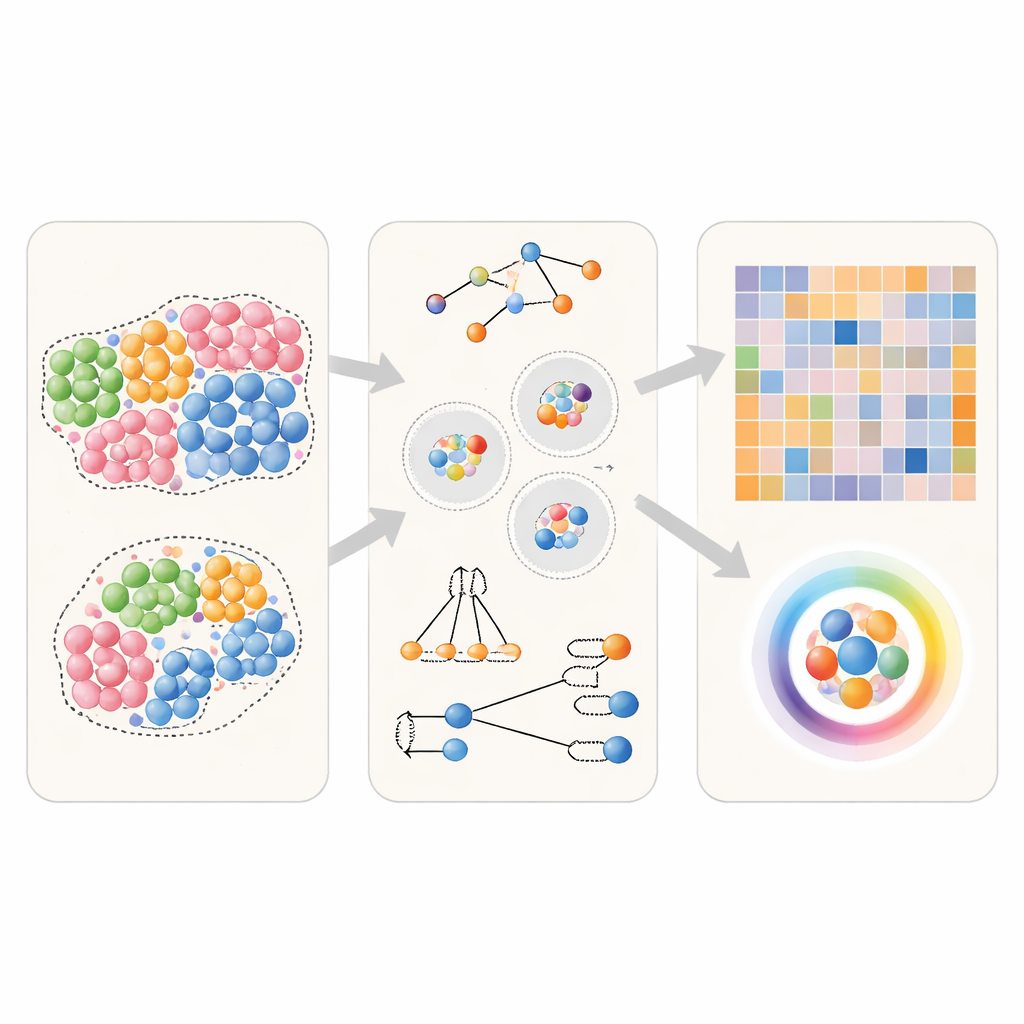
Testen der Nachbarschaftsmethoden in virtuellen Geweben
Um zu prüfen, wie gut die verschiedenen Ansätze funktionieren, nutzte das Team zunächst computergenerierte Gewebe, bei denen die wahren Nachbarschaftsbeziehungen im Voraus bekannt sind. Sie erzeugten einfache Szenarien, in denen ein bestimmter Zelltyp entweder keine besondere Präferenz hat, mild seine eigenen Art bevorzugt oder stark mit sich selbst klustert. Sie simulierten auch gerichtete Situationen, in denen sich ein Zelltyp bevorzugt an einen anderen anschmiegt, nicht jedoch umgekehrt. Mithilfe dieser virtuellen Gewebe fütterten die Autorinnen und Autoren identische Daten in mehrere weit verbreitete Werkzeuge und fragten dann: Kann jede Methode diese Szenarien zuverlässig auseinanderhalten und korrekt wiedergeben, welcher Zelltyp welchen Nachbarn sucht?
Warum Richtung und Feinheit schwer zu erfassen sind
Der Vergleich zeigte, dass fast alle Methoden große, offensichtliche Unterschiede in der Gewebeorganisation erkennen können. Zwei Schwachstellen traten jedoch deutlich zutage. Erstens komprimieren manche Werkzeuge ihre Ausgabe in grobe, dreistufige Scores (zum Beispiel „unter dem Zufallsniveau“, „kein Unterschied“ oder „über dem Zufallsniveau“), wodurch es schwierig wird, eine schwache von einer starken Nachbarschaftspräferenz zu unterscheiden. Zweitens mitteln viele Methoden Nachbarschaftszahlen über alle Zellen eines Typs, unabhängig davon, ob eine bestimmte Zelle überhaupt jemals auf den anderen Typ trifft. Dieses „Totale-Mittlung“-Vorgehen verwischt tendenziell die Richtung, sodass die Beziehung von A zu B ähnlich aussieht wie von B zu A, selbst wenn in Wahrheit nur eine Richtung eine Präferenz zeigt. Infolgedessen können bestehende Werkzeuge die scheinbare Richtung der Zellinfiltration unterschätzen oder sogar umkehren, besonders wenn ein Zelltyp selten und der andere häufig ist.
Eine neue Methode zur Bewertung gerichteter Nachbarn
Um diese Probleme anzugehen, führen die Autorinnen und Autoren ein neues Bewertungschema ein, genannt konditionaler z‑Score oder COZI. COZI behält die Idee bei, beobachtete Nachbarschaftszählungen mit vielen randomisierten Versionen des Gewebes zu vergleichen, ändert jedoch, wie die Zählungen gemittelt werden: Es berücksichtigt nur Zellen des Typs A, die tatsächlich mindestens eine Zelle des Typs B berühren. Dieser „konditionale“ Fokus ist entscheidend, um Richtungsinformationen wiederzugewinnen. COZI wandelt das Ergebnis anschließend in einen kontinuierlichen z‑Score um, der widerspiegelt, wie stark das beobachtete Muster von der zufälligen Erwartung abweicht. Um die Interpretation zu erleichtern, ergänzen die Autorinnen und Autoren ein Begleitmaß, das konditionale Zellverhältnis (CCR), das einfach angibt, welcher Anteil der Zellen vom Typ A überhaupt an der A–B‑Nachbarschaft teilnimmt. Zusammen zeigen z‑Score und CCR nicht nur, wie stark eine räumliche Beziehung ist, sondern auch, ob sie von wenigen spezialisierten Zellen oder von einer breiten Verschiebung in der Gewebeorganisation getragen wird.
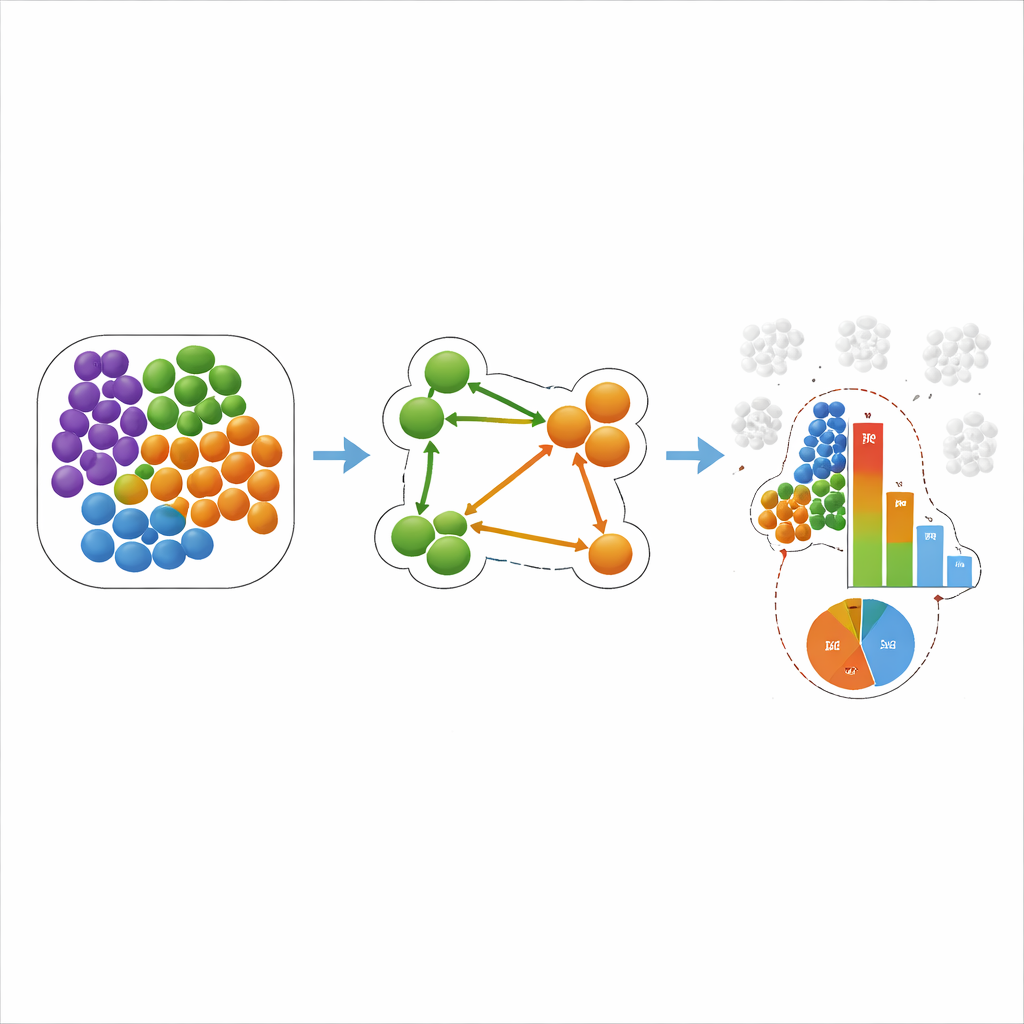
Was das für Krebs und Herzerkrankungen bedeutet
Das Team wandte COZI und andere Methoden anschließend auf zwei Datensätze aus der Praxis an. In einer Studie zu triple-negativem Brustkrebs hatten frühere Arbeiten Tumoren als „kalt“, „gemischt“ und „kompartimentiert“ eingeordnet, basierend darauf, wie Immun- und Tumorzellen sich vermischten. COZI reproduzierte diese Gruppierungen und deckte darüber hinaus gerichtete Muster auf: Beispielsweise neigten in manchen Tumoren Immunzellen dazu, unter sich zu clustern, während eine Untergruppe von Tumorzellen in diese Nischen hineinreichte, während in anderen Tumoren die Immunzellen die Tumorregionen infiltrierten. In einem Mausmodell des Herzinfarkts verfolgte COZI, wie Neutrophile und Monozyten schrittweise in den geschädigten Herzmuskel eindrangen, zuerst durch die Innenauskleidung der Herzkammer und dann tiefer in die verletzte Zone. Wichtig war dabei die Trennung globaler Verschiebungen in Zellzahlen von echten Veränderungen darin, wer wen als Nachbarn hat und in welche Richtung.
Kerngedanke
Diese Studie zeigt, dass nicht alle Werkzeuge zum Ablesen von Zellnachbarschaften gleichwertig sind und dass kleine algorithmische Entscheidungen biologische Schlussfolgerungen stark beeinflussen können. Indem die Autorinnen und Autoren klären, wie bestehende Methoden arbeiten, und COZI zusammen mit dem konditionalen Zellverhältnis einführen, liefern sie eine Roadmap zur Auswahl und Interpretation von Nachbarschaftsanalysen in räumlichen Gewebedaten. Für Nicht‑Spezialisten lautet die Kernbotschaft: Zu wissen, wer im Gewebe‑„Stadtbild“ neben wem lebt — und wer in wessen Gebiet eindringt — kann frühe Krankheitszeichen, Therapieantworten und Wege für gezielte Behandlungen offenbaren, vorausgesetzt, diese Muster werden mit den richtigen Werkzeugen gemessen.
Zitation: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Schlüsselwörter: räumliche Omik, Zellnachbarschaften, tumormikroumgebung, Infiltration von Immunzellen, computationale Pathologie