Clear Sky Science · it
Confronto e ottimizzazione dei metodi di preferenza dei vicini cellulari per l’analisi quantitativa dei tessuti
Perché i vicini cellulari contano
I nostri corpi sono composti da vivaci quartieri di cellule, non da sparpagliamenti casuali. Quali cellule si trovano accanto ad altre può influenzare come un tumore cresce, come guarisce una ferita o come il cuore si riprende dopo un infarto. Questo articolo pone una domanda apparentemente semplice: quando gli scienziati misurano quali tipi cellulari tendono a trovarsi vicini nelle immagini dei tessuti, quanto sono affidabili i diversi metodi che usano, e si può fare meglio?
Come gli scienziati leggono la mappa cittadina cellulare
Le tecnologie di imaging moderne e della genomica spaziale possono registrare la posizione esatta e l’identità di migliaia di cellule in una sezione di tessuto. Un modo popolare per analizzare questi dati è calcolare le “preferenze di vicinato”: per un dato tipo cellulare A, quanto spesso ha come vicino il tipo cellulare B rispetto a quanto ci si aspetterebbe per caso? Esistono già molti strumenti software per questo compito, ma si basano su passaggi leggermente diversi. Gli autori li scompongono in tre scelte fondamentali: come definire il vicinato intorno a ogni cellula (per esempio disegnando archi tra cellule vicine o usando una distanza fissa), come contare i vicini (trattando la coppia A–B allo stesso modo di B–A, oppure distinguendo la direzione da A verso B rispetto a B verso A), e come trasformare questi conteggi in un punteggio finale (conteggi normalizzati semplici, statistiche basate su permutazioni o misure di machine learning). Questo quadro comune permette un confronto equo, fianco a fianco, dei metodi.
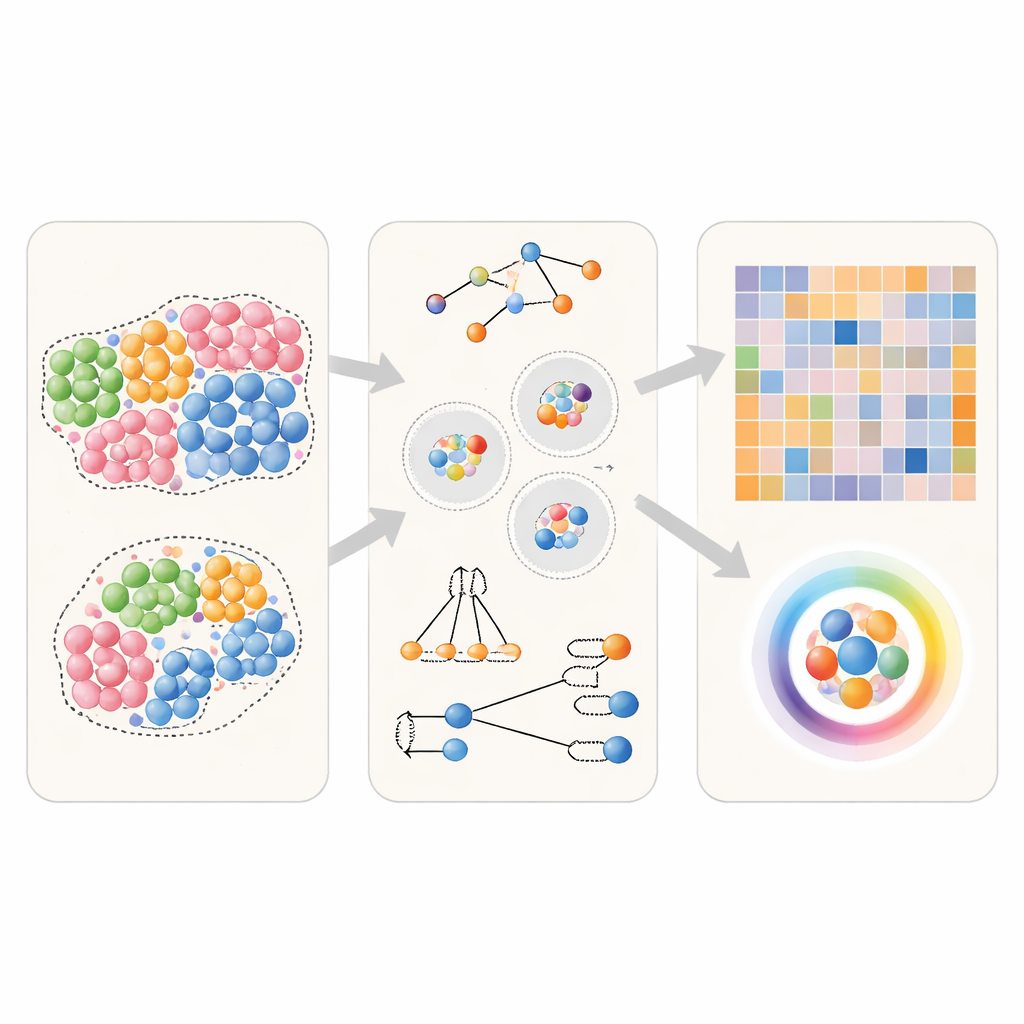
Testare i metodi di vicinato in tessuti virtuali
Per vedere quanto rendono i diversi approcci, il gruppo ha usato innanzitutto tessuti generati al computer dove le vere relazioni di vicinato sono note a priori. Hanno creato scenari semplici in cui un particolare tipo cellulare non mostra preferenze speciali, preferisce leggermente lo stesso tipo, o si raggruppa fortemente con sé stesso. Hanno anche simulato situazioni direzionali in cui un tipo cellulare tende a stare vicino a un altro, ma non viceversa. Usando questi tessuti virtuali, gli autori hanno fornito dati identici a diversi strumenti largamente utilizzati e poi hanno chiesto: ogni metodo riesce a distinguere in modo affidabile questi scenari, e può recuperare correttamente quale tipo cellulare cerca quale vicino?
Perché direzione e sottigliezza sono difficili da catturare
Il confronto ha rivelato che quasi tutti i metodi riescono a rilevare grandi differenze ovvie nell’organizzazione del tessuto. Tuttavia sono emerse due debolezze chiave. Primo, alcuni strumenti comprimono il loro output in punteggi grossolani a tre livelli (per esempio «sotto il caso», «nessuna differenza» o «sopra il caso»), il che rende difficile distinguere una preferenza di vicinato debole da una forte. Secondo, molti metodi fanno la media dei conteggi dei vicini su tutte le cellule di un dato tipo, indipendentemente dal fatto che una cellula particolare incontri effettivamente l’altro tipo. Questa «media totale» tende a offuscare la direzionalità, facendo apparire la relazione da A a B simile a quella da B a A, anche quando solo una direzione mostra realmente una preferenza. Di conseguenza, gli strumenti esistenti possono sottostimare o perfino invertire la direzione apparente dell’infiltrazione cellulare, specialmente quando un tipo cellulare è raro e l’altro è abbondante.
Un nuovo modo per valutare i vicini direzionali
Per affrontare questi problemi, gli autori introducono un nuovo schema di punteggio chiamato z-score condizionale, o COZI. COZI mantiene l’idea di confrontare i conteggi osservati di vicini con molte versioni randomizzate del tessuto, ma cambia il modo in cui i conteggi vengono mediati: considera solo le cellule di tipo A che toccano effettivamente almeno una cellula di tipo B. Questo focus «condizionale» si rivela cruciale per recuperare la direzionalità. COZI converte quindi il risultato in uno z-score continuo, che riflette quanto il pattern osservato si discosta dall’aspettativa casuale. Per rendere i punteggi più interpretabili, gli autori aggiungono una misura complementare, il rapporto cellulare condizionale (CCR), che riporta semplicemente quale frazione delle cellule di tipo A partecipa almeno a un vicinato A–B. Insieme, lo z-score e il CCR rivelano non solo quanto è forte una relazione spaziale, ma anche se è guidata da poche cellule specializzate o da uno spostamento ampio nell’organizzazione del tessuto.
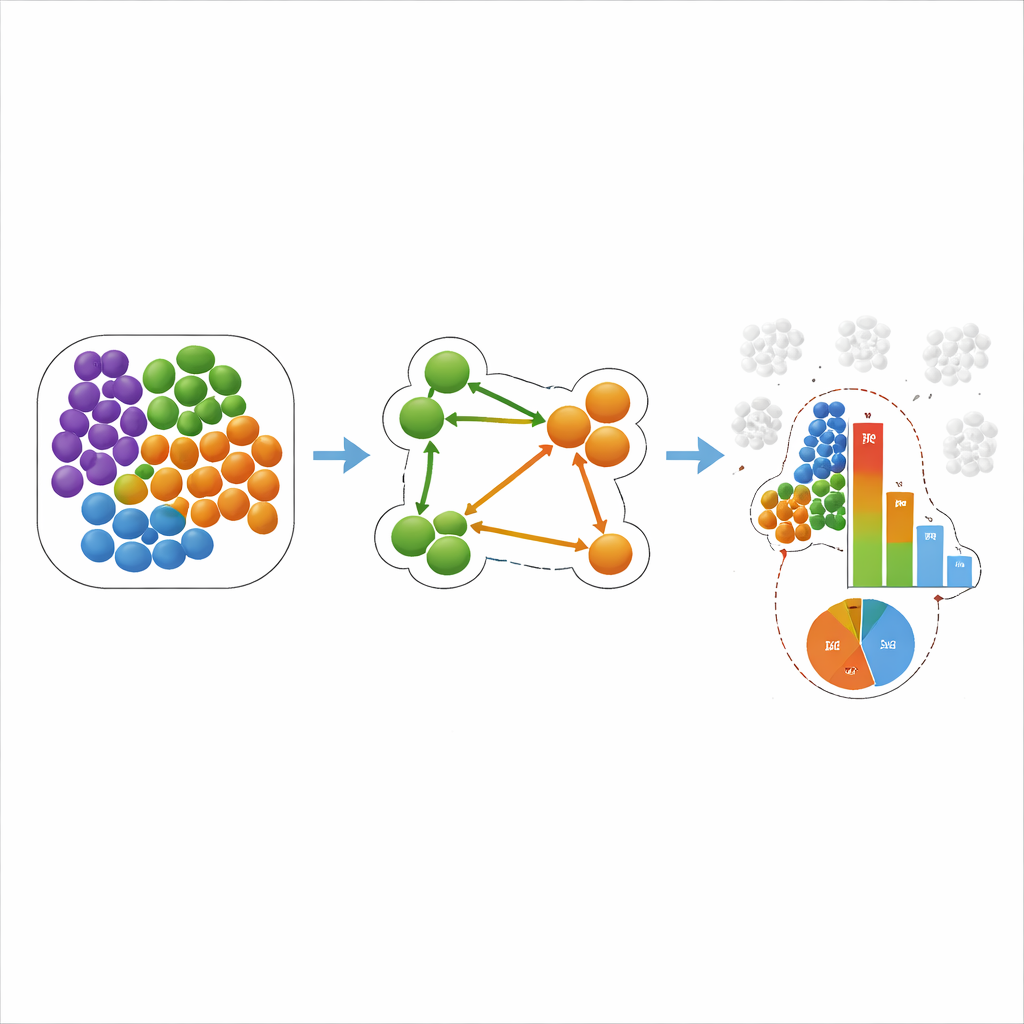
Cosa significa per cancro e malattie cardiache
Il gruppo ha poi applicato COZI e altri metodi a due dataset del mondo reale. In uno studio sul carcinoma mammario triplo-negativo, lavori precedenti avevano raggruppato i tumori in «freddi», «misti» e «compartimentati» in base a come le cellule immunitarie e le cellule tumorali si mescolavano. COZI non solo ha riprodotto questi raggruppamenti, ma ha anche scoperto pattern direzionali: per esempio, in alcuni tumori le cellule immunitarie tendevano a raggrupparsi tra loro mentre una sottopopolazione di cellule tumorali si insinuava in queste sacche, mentre in altri erano le cellule immunitarie a infiltrare le regioni tumorali. In un modello murino di infarto, COZI ha tracciato come neutrofili e monociti siano entrati progressivamente nel muscolo cardiaco danneggiato, prima attraverso il rivestimento interno del ventricolo e poi più in profondità nella zona lesionata. Importante, ha separato gli spostamenti globali nei numeri cellulari dai veri cambiamenti su chi sta vicino a chi e in quale direzione.
Messaggio principale
Questo studio mostra che non tutti gli strumenti per leggere i vicinati cellulari sono equivalenti e che piccole scelte algoritmiche possono plasmare fortemente le conclusioni biologiche. Chiarendo come funzionano i metodi esistenti e introducendo COZI insieme al rapporto cellulare condizionale, gli autori forniscono una mappa per scegliere e interpretare le analisi di vicinato nei dati spaziali dei tessuti. Per i non specialisti, l’idea chiave è che capire chi vive accanto a chi nella «città» tissutale — e chi sta entrando nel territorio di chi — può rivelare segnali precoci di malattia, risposte alla terapia e vie per trattamenti mirati, purché quei pattern siano misurati con gli strumenti giusti.
Citazione: Schiller, C., Ibarra-Arellano, M.A., Bestak, K. et al. Comparison and optimization of cellular neighbor preference methods for quantitative tissue analysis. Nat Commun 17, 3514 (2026). https://doi.org/10.1038/s41467-026-71699-z
Parole chiave: spatial omics, cell neighborhoods, tumor microenvironment, immune cell infiltration, computational pathology