Clear Sky Science · tr
Fazla-ayrışmış hücresel bölmelerde hedeflenmiş RNA düzenlemesi için ortogonal bir RNA aptameri
Hücresel Küçük Damlacıkların İçinde RNA’yı İzlemek ve Kontrol Etmek
Her hücrede RNA zincirleri sürekli üretilir, taşınır ve yok edilir. Bu RNA’ların birçoğu hücre içindeki küçük, sıvımsı damlacıklarda toplanır. Bu damlacıklar yaşamın kimyasını düzenlemeye yardımcı olur, ancak gerçek zamanlı olarak izlenmeleri zordur. Bu makale, bilim insanlarının bu damlacıkların içinde belirli RNA’ları hem aydınlatmasına hem de isteyerek yok etmesine olanak veren yeni bir moleküler araç setini tanımlıyor; böylece o RNA’ların canlı hücrelerde gerçekten ne yaptığını ortaya koyuyor.
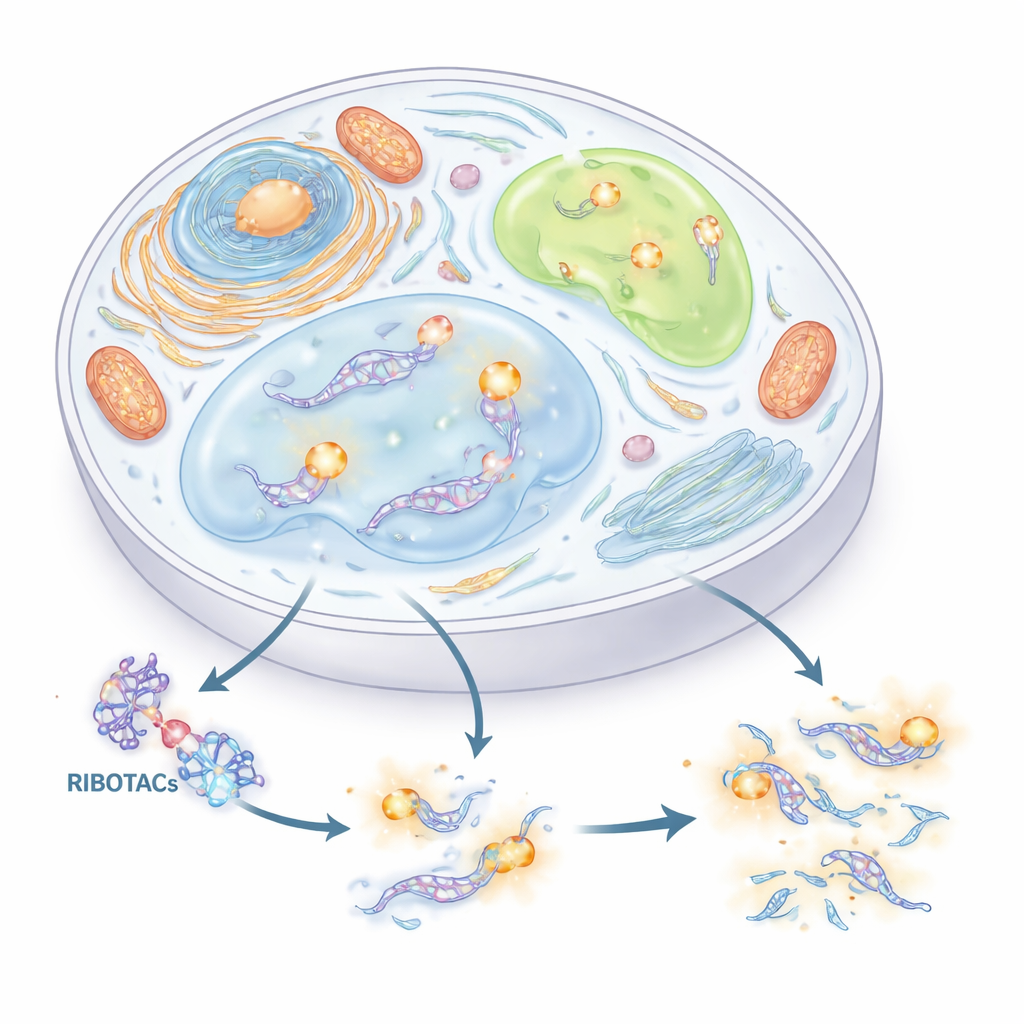
RNA’yı Bulmak ve Kesmek İçin Yeni Bir Tutamaç
Yazarlar, RNA’yı izlemek ve kontrol etmek için hassas, iki işlevli bir sistem oluşturmayı hedeflediler. İki fikri birleştirdiler. Birincisi, katlanarak belirli küçük bir molekülü yakalayabilen kısa bir RNA “etiketi” (aptamer). İkincisi ise seçili bir RNA’ya bağlanıp ardından doğal bir RNA kesici enzimi çekerek onu imha eden tasarımcı molekül sınıfı RIBOTAC’lar. Binlerce küçük molekülü ve yüzlerce RNA yapısını titizlikle tarayarak, ekip HIV-TAR adlı viral bir diziden türeyen kompakt bir RNA etiketi belirledi ve bunu HT adını verdikleri bir aptamer olarak optimize etti. Ardından HT’yi tanıyan ve hücrenin RNase L enzimini çeken RIBOTAC’lar inşa ettiler; böylece HT taşıyan herhangi bir RNA seçici olarak yok edilebilir bir hedef haline geldi.
Canlı Hücrelerde RNA’yı İzlemek İçin Parlak Bir Renk Eklemek
Etiketlenmiş bu RNA’ları görünür kılmak için araştırmacılar HT’yi, zararsız bir boyaya (NBSI) bağlandığında turuncu-kırmızı parlayan ayrı bir floresan aptamer olan Clivia ile birleştirdiler. Ortaya çıkan hibrit etiket Clivia-HT, işaretli her RNA’ya iki ayrı yetenek kazandırıyor: Clivia tarafı görüntüleme için ışıldayan boyayı çekerken, HT tarafı kontrollü kesim için RIBOTAC tarafından tanınıyor. Ekip, bu iki işlevin bağımsız olarak çalıştığını gösterdi: boya Clivia’yı ışıklandırırken bozunmayı etkilemiyor; RIBOTAC HT’ye bağlanıp kesimi tetiklerken floresan sinyali ancak RNA kendisi ortadan kalktığında sönüyor. Clivia-HT’yi bir RNA üzerine birkaç kez tekrarlayarak parlaklığı artırdılar ve böylece işaretli molekülleri canlı hücrelerde izleyebildiler.
Stres Damlacıklarındaki Gizli RNA Rolleri Üzerine Sondaj
Bu çift etiketle donanmış olarak yazarlar, zar olmadan oluşan damlacık benzeri faz-ayırtımlı hücresel bölmelerin içindeki RNA’ları incelediler. Önce U gövdelerini işaretleyen U1 küçük nükleer RNA’ya Clivia-HT yerleştirdiler. Hücreler strese girdiğinde bu U gövdeleri ışık saçtı; HT’ye hedeflenen RIBOTAC eklendiğinde sinyal kademeli olarak silindi ve U gövdelerinin sayısı azaldı, ancak bu yalnızca kesici enzim RNase L bulunduğunda gerçekleşti. Ardından stres granülleri içinde ATF4 haberci RNA’sını etiketlediler; bu granüller hücresel zorluk sırasında ortaya çıkar. ATF4 RNA’sı bu granüllerde açıkça birikti ve talep üzerine degradasyona uğratılabiliyordu, ancak onu kaldırmak granüllerin oluşum veya çözülme biçimini değiştirmedi. Bu, ATF4 RNA’sının orada bulunmasına rağmen stres granülü dinamiklerinin ana sürücüsü olmadığını gösteriyor.
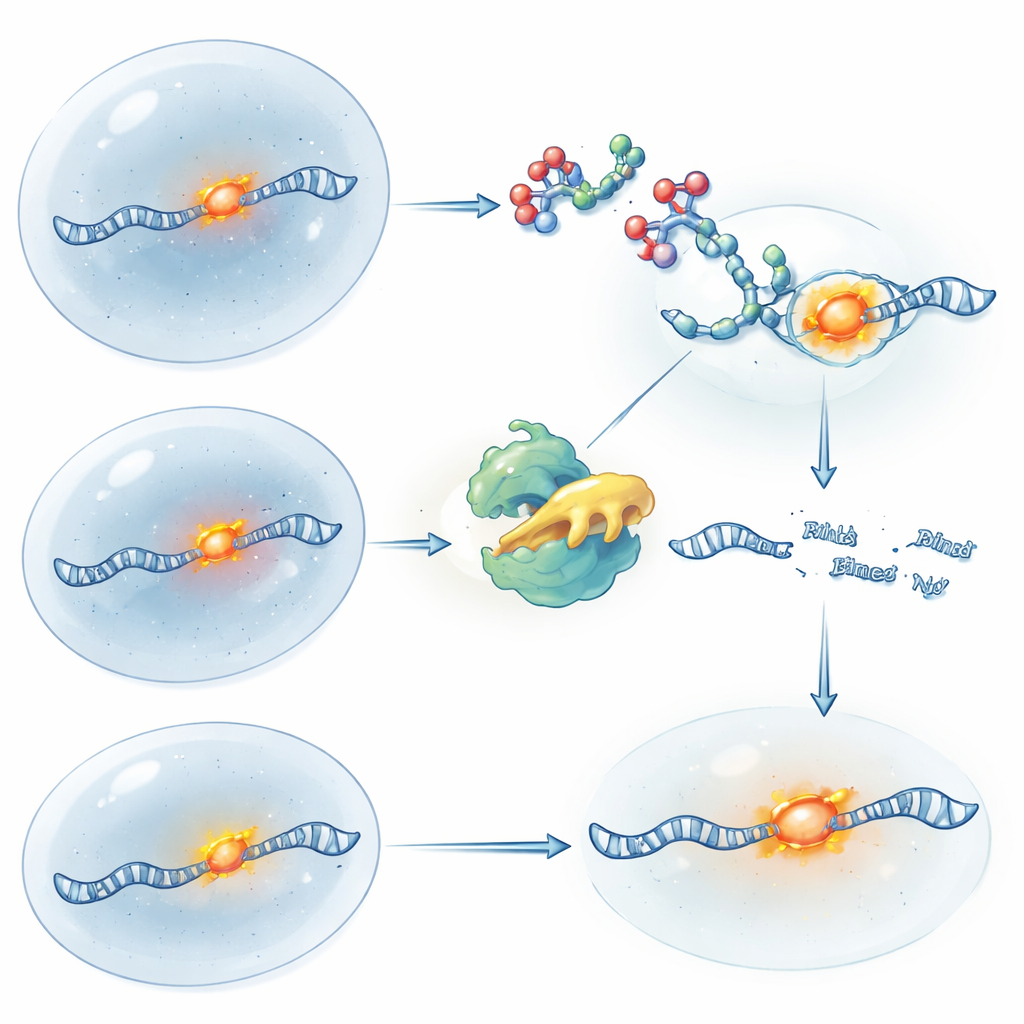
RNA Kontrolünü Işıkla Açıp Kapatmak
Zamanlama üzerinde daha ince kontrol sağlamak için ekip RIBOTAC’larının ışığa duyarlı sürümlerini oluşturdu. Bir tasarımda molekül başlangıçta aktiftir ve kısa bir ultraviyole ışık darbesi dahili güvenlik bağını kesince “kapalı” hale gelir; bu daha fazla kesimi durdurur ve taze RNA’nın yeniden birikmesine izin verir. Diğer bir tasarımda ise RIBOTAC kafeslenmiş ve bloke edilmiş konumdadır; ışık, engelleyici grubu uzaklaştırana kadar inaktif kalır ve aniden RNA kesme gücünü serbest bırakır. Bu araçları ATF4 RNA’sı üzerinde kullanarak, araştırmacılar gen kesme ve gen geri kazanma mantığını tamamen kimya ve ışıkla taklit edebildiler; tüm bunlar RNA’nın konumu floresans yoluyla izlenirken yapıldı. Bu yaklaşım, bir RNA’nın nerede olduğunu sormanın ötesine geçerek, o RNA belirli anlarda kaldırıldığında veya geri getirildiğinde hücrede neler olduğunu sorma olanağı sağlıyor.
Uzun Bir RNA’nın Genomu Nasıl Koruduğunu Ortaya Koymak
Yazarlar daha sonra kromozom bütünlüğünü korumaya yardımcı olduğu bilinen uzun bir RNA olan NORAD’a yöneldiler. NORAD, Pumilio proteinleriyle birlikte sitoplazmada NP gövdeleri adı verilen belirgin damlacıklarda toplanır. NORAD ve minimal bir NORAD fragmanı (circPRE8) Clivia-HT ile etiketlendiğinde bu oluşumlar görselleştirilebildi ve RNA seçici olarak yok edilebildi. NORAD veya circPRE8 bulunduğunda Pumilio proteinleri parlak noktacıklar oluşturdu ve hücrelerde kromozom ayrım hataları daha az oldu. Etiketli RNA RIBOTAC ile degradasyona uğratıldığında damlacıklar kayboldu, Pumilio proteinleri dağıldı ve kromozom hataları arttı. Bu deneyler, belirli NORAD bölgelerinin genomu koruyan protein–RNA damlacıklarının oluşması için gerekli olduğunu gösteriyor.
Gelecek Hücre Biyolojisi İçin Anlamı
Özetle, bu çalışma herhangi bir seçilen RNA’nın hücre içinde, hatta hassas sıvımsı bölmelerde bile hem görülebilmesini hem de hassas şekilde yok edilebilmesini sağlayan çok yönlü bir “tak-çıkar” RNA etiketi sunuyor. Parlak görüntülemeyi hedeflenmiş yok etme ile birleştirip ışık tabanlı açık–kapalı anahtarlar ekleyerek Clivia-HT sistemi, bir RNA’nın bir yapıda bulunmasının hücre davranışı açısından gerçekten önemli olup olmadığını test etmeyi mümkün kılıyor. Bu araç seti, araştırmacıların RNA konumunun statik görüntülerinin ötesine geçip belirli RNA’ların stres yanıtlarını, damlacık oluşumunu ve genoma kararlılığı nasıl şekillendirdiğini ortaya çıkaran nedensel deneyler yapmasına yardımcı olacak.
Atıf: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Anahtar kelimeler: RNA görüntüleme, fazla-ayrışmış kondensatlar, RNA bozunumu, ışık kontrollü kimya, uzun kodlamayan RNA