Clear Sky Science · fr
Un aptamère ARN orthogonal pour la régulation ciblée de l’ARN dans des compartiments subcellulaires séparés par phase
Observer et contrôler l’ARN à l’intérieur de minuscules gouttelettes cellulaires
À l’intérieur de chaque cellule, des brins d’ARN sont en permanence synthétisés, déplacés et détruits. Beaucoup de ces ARN se rassemblent dans de petites gouttes à l’aspect liquide qui flottent dans le cytoplasme. Ces gouttelettes contribuent à organiser la chimie de la vie, mais elles sont difficiles à étudier en temps réel. Cet article décrit un nouvel ensemble d’outils moléculaires qui permet aux scientifiques d’illuminer des ARN spécifiques et de les effacer intentionnellement à l’intérieur de ces gouttelettes, révélant ainsi ce que ces ARN font réellement dans des cellules vivantes.
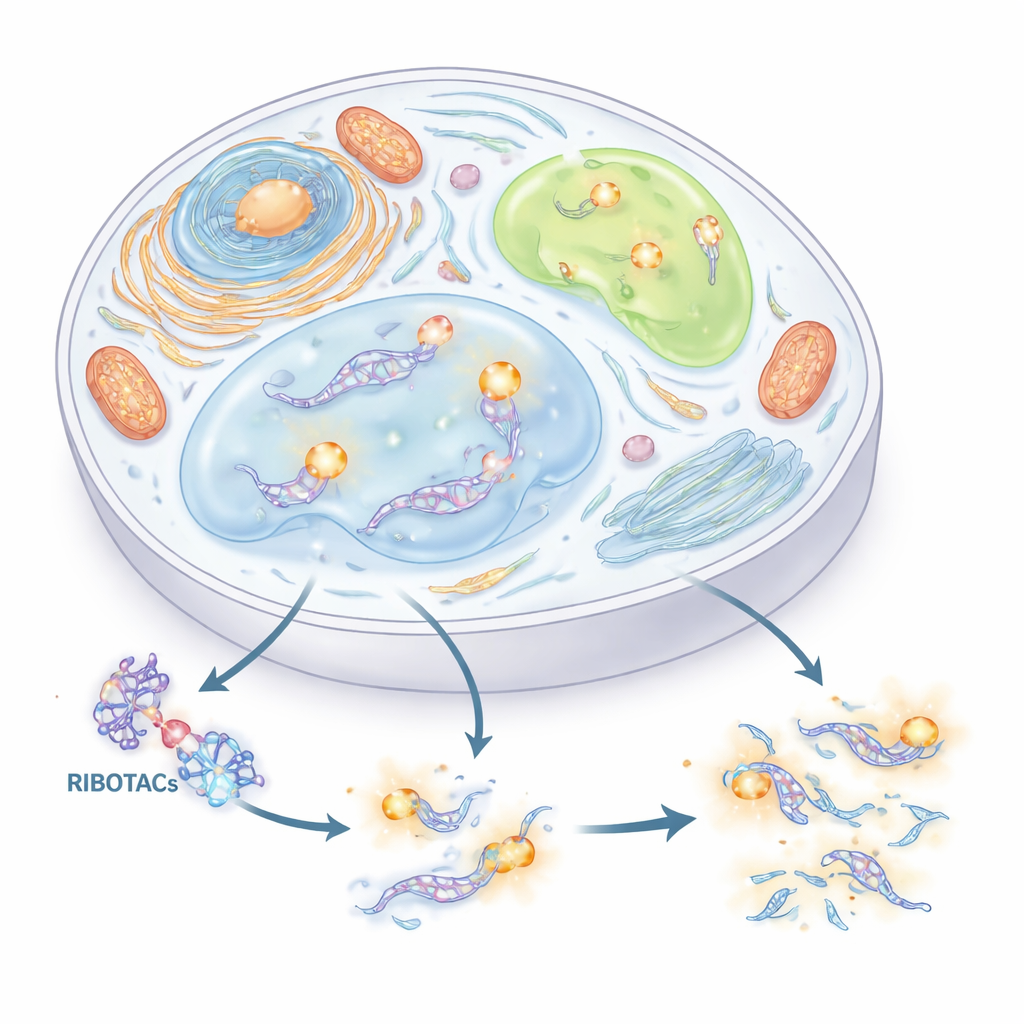
Une nouvelle poignée pour repérer et couper l’ARN
Les auteurs ont cherché à construire un système précis et double usage pour suivre et contrôler l’ARN. Ils ont combiné deux idées. La première est une courte « étiquette » ARN (un aptamère) capable de se replier et de capturer une petite molécule complémentaire. La seconde est une classe de molécules conçues appelées RIBOTACs, qui se lient à un ARN choisi puis recrutent une enzyme cellulaire de clivage de l’ARN pour le détruire. En criblant soigneusement des milliers de petites molécules et des centaines de structures d’ARN, l’équipe a identifié une étiquette ARN compacte, dérivée d’une séquence virale appelée HIV‑TAR, et l’a optimisée en un aptamère qu’ils nomment HT. Ils ont ensuite conçu des RIBOTACs qui reconnaissent HT et recrutent l’enzyme RNase L de la cellule, transformant tout ARN portant HT en une cible destructible de manière sélective.
Ajouter une couleur vive pour suivre l’ARN dans des cellules vivantes
Pour rendre ces ARN marqués visibles, les chercheurs ont fusionné HT à un aptamère fluorescent distinct nommé Clivia, qui émet une fluorescence orange‑rouge lorsqu’il se lie à un colorant inoffensif (NBSI). L’étiquette hybride résultante, Clivia‑HT, confère à chaque ARN marqué deux capacités distinctes : le côté Clivia attire le colorant lumineux pour l’imagerie, tandis que le côté HT est reconnu par le RIBOTAC pour la découpe contrôlée. L’équipe a montré que ces deux fonctions opèrent indépendamment : le colorant illumine Clivia sans affecter la dégradation, et le RIBOTAC se fixe sur HT et déclenche la découpe sans atténuer le signal fluorescent tant que l’ARN n’a pas été éliminé. En répétant Clivia‑HT plusieurs fois sur un même ARN, ils ont augmenté la luminosité suffisamment pour suivre les molécules marquées dans des cellules vivantes.
Explorer les rôles cachés de l’ARN dans les gouttelettes de stress
Armés de cette double étiquette, les auteurs ont exploré les ARN à l’intérieur de compartiments subcellulaires séparés par phase — des structures en forme de gouttelettes qui se forment sans membrane. Ils ont d’abord inséré Clivia‑HT dans l’ARN nucléaire petit U1, qui marque les corps U, un type de granule riche en ARN. Lorsque les cellules étaient stressées, ces corps U s’illuminaient ; l’ajout du RIBOTAC ciblant HT effaçait ensuite progressivement le signal et diminuait le nombre de corps U, mais seulement en présence de l’enzyme RNase L. Ensuite, ils ont marqué l’ARN messager ATF4 à l’intérieur des granules de stress, des gouttelettes qui apparaissent lors de difficultés cellulaires. Bien que l’ARN ATF4 s’accumulât clairement dans ces granules et pût être dégradé à la demande, son élimination n’a pas modifié la façon dont les granules se formaient ou se dissipaient. Cela indique que, malgré sa présence, l’ARN ATF4 n’est pas un élément moteur des dynamiques des granules de stress.
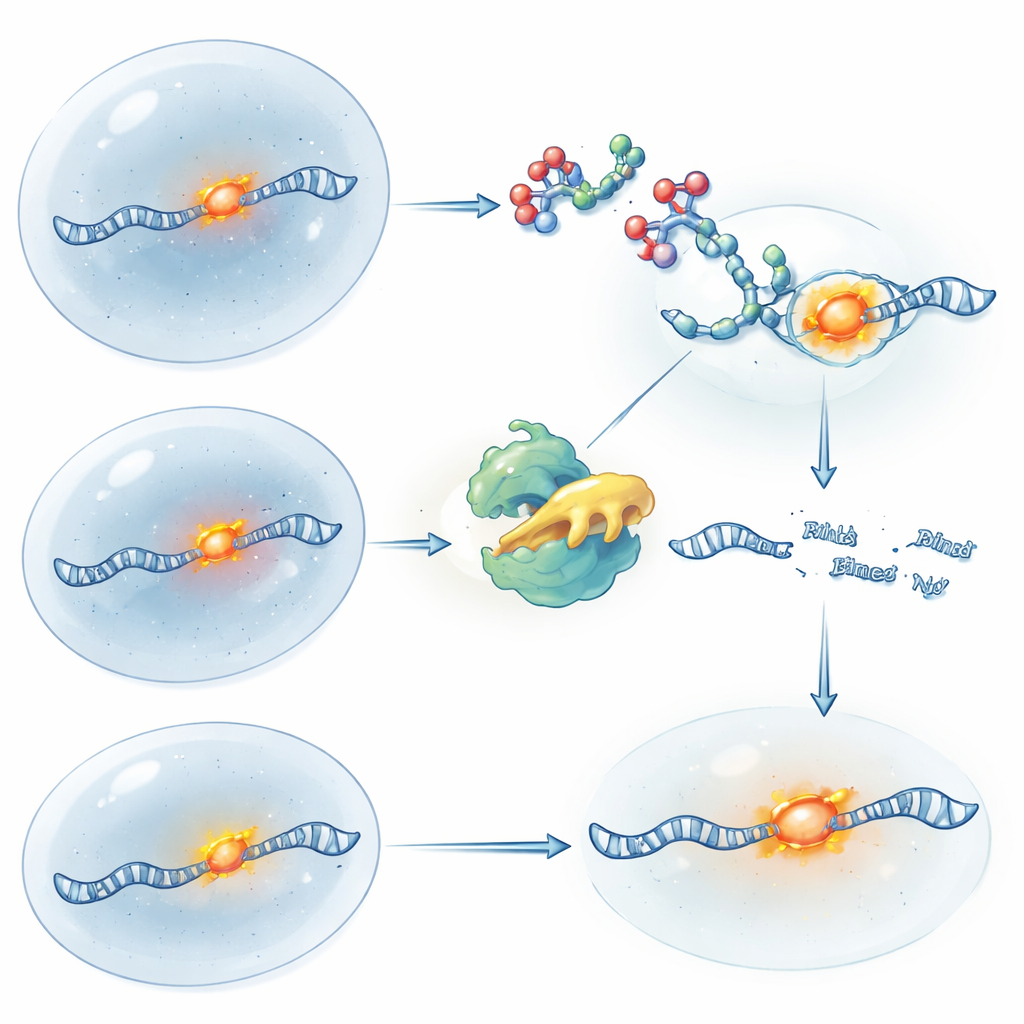
Activer et désactiver le contrôle de l’ARN par la lumière
Pour obtenir un contrôle temporel encore plus fin, l’équipe a conçu des versions photosensibles de leurs RIBOTACs. Dans une conception, la molécule commence active et est « désactivée » lorsqu’une brève impulsion de lumière ultraviolette clive un lien de sécurité intégré, arrêtant la découpe et permettant à de nouveaux ARN de se reconstituer. Dans l’autre conception, le RIBOTAC est cagé et inactif jusqu’à ce que la lumière retire le groupe bloquant, libérant soudainement son pouvoir de cliver l’ARN. En utilisant ces outils sur l’ARN ATF4, les chercheurs ont pu imiter la logique d’une suppression génique puis d’une restauration uniquement par la chimie et la lumière, tout en suivant l’emplacement de l’ARN par fluorescence. Cette approche permet d’étudier non seulement où se trouve un ARN, mais aussi ce qui arrive à la cellule lorsque cet ARN est retiré ou restauré à des moments précis.
Révéler comment un ARN long protège le génome
Les auteurs se sont ensuite intéressés à un long ARN appelé NORAD, connu pour aider à préserver l’intégrité des chromosomes. NORAD se rassemble avec les protéines Pumilio en gouttelettes distinctes appelées corps NP dans le cytoplasme. En marquant NORAD et un fragment minimal de NORAD (circPRE8) avec Clivia‑HT, ils ont pu visualiser ces assemblages et effacer sélectivement l’ARN. Lorsque NORAD ou circPRE8 était présent, les protéines Pumilio formaient des poncta brillants et les cellules présentaient moins d’erreurs de ségrégation chromosomique. Lorsque l’ARN marqué était dégradé par le RIBOTAC, les gouttelettes disparaissaient, les protéines Pumilio se dispersaient et les erreurs chromosomiques augmentaient. Ces expériences montrent que des régions spécifiques de NORAD sont essentielles pour former des gouttelettes protéine–ARN protectrices qui sauvegardent le génome.
Ce que cela signifie pour la biologie cellulaire future
En résumé, ce travail introduit une étiquette ARN polyvalente « plug‑in » qui permet à n’importe quel ARN choisi d’être à la fois visualisé et effacé avec précision à l’intérieur de la cellule, y compris dans des compartiments délicats de type liquide. En mariant imagerie lumineuse et destruction ciblée, et en ajoutant des interrupteurs lumineux marche/arrêt, le système Clivia‑HT permet de tester si la simple présence d’un ARN dans une structure influe réellement sur le comportement cellulaire. Cet ensemble d’outils aidera les chercheurs à aller au‑delà d’images statiques de la localisation de l’ARN pour mener des expériences causales révélant comment des ARN spécifiques façonnent les réponses au stress, la formation de gouttelettes et la stabilité du génome.
Citation: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Mots-clés: Imagerie de l’ARN, condensats séparés par phase, dégradation de l’ARN, chimie contrôlée par la lumière, ARN non codant long