Clear Sky Science · pl
Ortogonalny aptamer RNA do ukierunkowanej regulacji RNA w fazowo-rozgraniczonych podkomórkowych przedziałach
Obserwacja i kontrola RNA wewnątrz maleńkich kropli komórkowych
W każdej komórce nici RNA są nieustannie wytwarzane, przemieszczane i niszczone. Wiele z tych RNA gromadzi się w maleńkich, ciekopodobnych kroplach unoszących się w wnętrzu komórki. Krople te porządkują biochemię życia, ale trudno je badać w czasie rzeczywistym. W artykule opisano nowy zestaw molekularny, który pozwala naukowcom zarówno oświetlić wybrane RNA, jak i celowo je usuwać wewnątrz tych kropli, ujawniając, co te RNA robią w żywych komórkach.
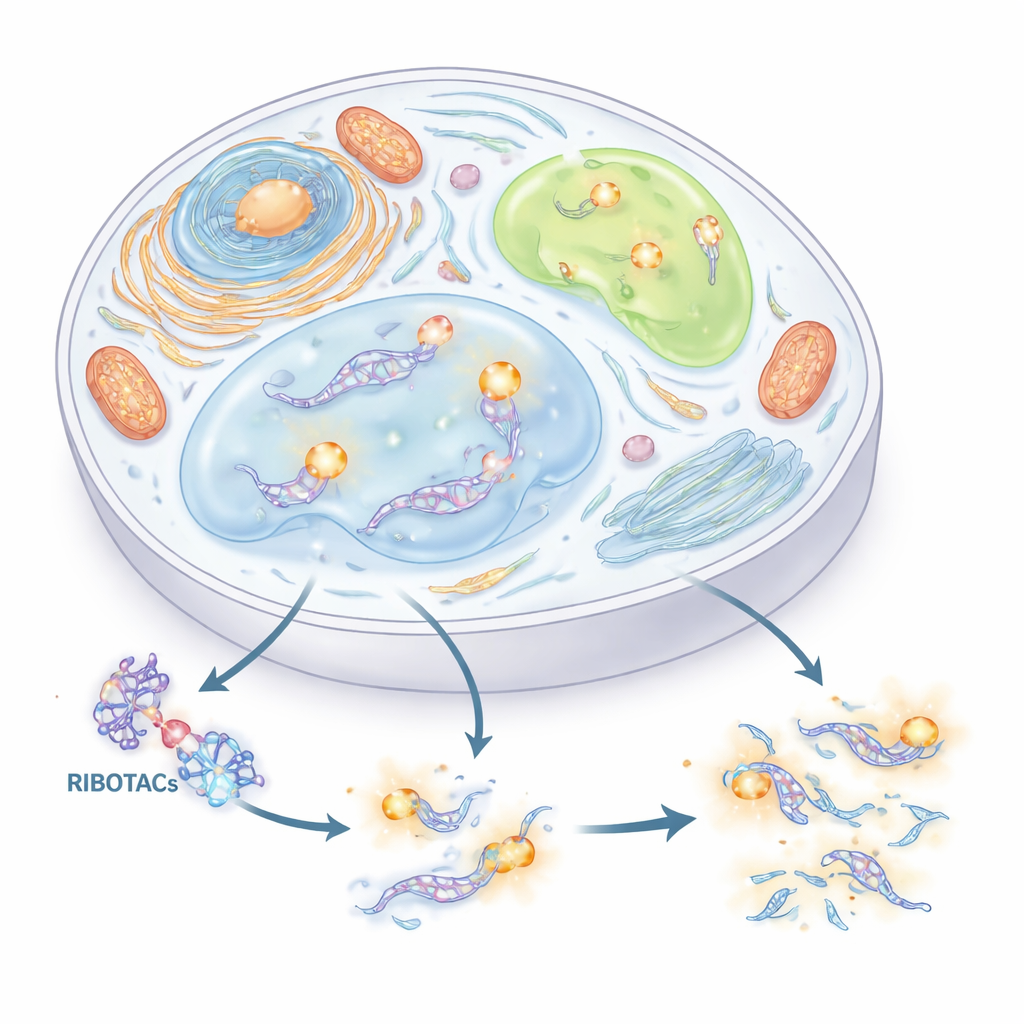
Nowy uchwyt do lokalizowania i przecinania RNA
Autorzy postawili sobie za cel skonstruowanie precyzyjnego systemu 2 w 1 do śledzenia i kontroli RNA. Połączyli dwie koncepcje. Pierwsza to krótki „znacznik” RNA (aptamer), który może złożyć się w kształt chwytający dopasowaną małą cząsteczkę. Druga to klasa zaprojektowanych cząsteczek zwanych RIBOTAC, które przyłączają się do wybranego RNA, a następnie rekrutują naturalne enzymy tnące RNA, by je zniszczyć. Poprzez staranne przesiewanie tysięcy małych cząsteczek i setek form RNA, zespół zidentyfikował kompaktowy znacznik RNA pochodzący z wirusowej sekwencji nazywanej HIV-TAR i zoptymalizował go do aptameru nazwanego HT. Następnie zbudowali RIBOTAC rozpoznające HT i przyciągające komórkowy enzym RNase L, przekształcając każde RNA z noszonym HT w selektywny cel do zniszczenia.
Dodanie jaskrawego koloru, by śledzić RNA w żywych komórkach
Aby uczynić oznakowane RNA widocznymi, badacze zespolili HT z oddzielnym fluoryzującym aptamerem o nazwie Clivia, który świeci na pomarańczowo-czerwono po związaniu nieszkodliwej barwnikowej cząsteczki (NBSI). Powstały hybrydowy znacznik Clivia-HT daje każdemu oznakowanemu RNA dwie odrębne zdolności: część Clivia przyciąga świecący barwnik do obrazowania, podczas gdy część HT jest rozpoznawana przez RIBOTAC do kontrolowanego przecinania. Zespół wykazał, że te dwie funkcje działają niezależnie: barwnik rozświetla Clivię bez wpływu na degradację, a RIBOTAC wiąże HT i wywołuje cięcie bez przyciemniania sygnału fluorescencyjnego aż do momentu usunięcia samego RNA. Powtarzając Clivia-HT kilkukrotnie na jednym RNA, zwiększyli jasność na tyle, by śledzić oznakowane cząsteczki w żywych komórkach.
Zgłębianie ukrytych ról RNA w kroplach stresowych
Wyposażeni w ten podwójny znacznik, autorzy zbadali RNA wewnątrz fazowo-rozgraniczonych podkomórkowych przedziałów — struktur przypominających krople, które powstają bez błon. Najpierw wstawili Clivia-HT do małego jądrowego RNA U1, który oznacza tzw. U bodies, rodzaj bogatych w RNA ziarnistości. Gdy komórki były zestresowane, te U bodies rozświetlały się; dodanie RIBOTAC celującego w HT stopniowo gasiło sygnał i zmniejszało liczbę U bodies, ale tylko gdy obecny był enzym RNase L. Następnie oznakowali mRNA ATF4 wewnątrz granul stresowych, kropelek pojawiających się podczas trudności komórkowych. Chociaż RNA ATF4 wyraźnie gromadziło się w tych grudkach i mogło być degradowane na żądanie, jego usunięcie nie zmieniało sposobu tworzenia ani rozpuszczania się grudek. Wskazuje to, że mimo obecności, RNA ATF4 nie jest kluczowym motorem dynamiki granul stresowych.
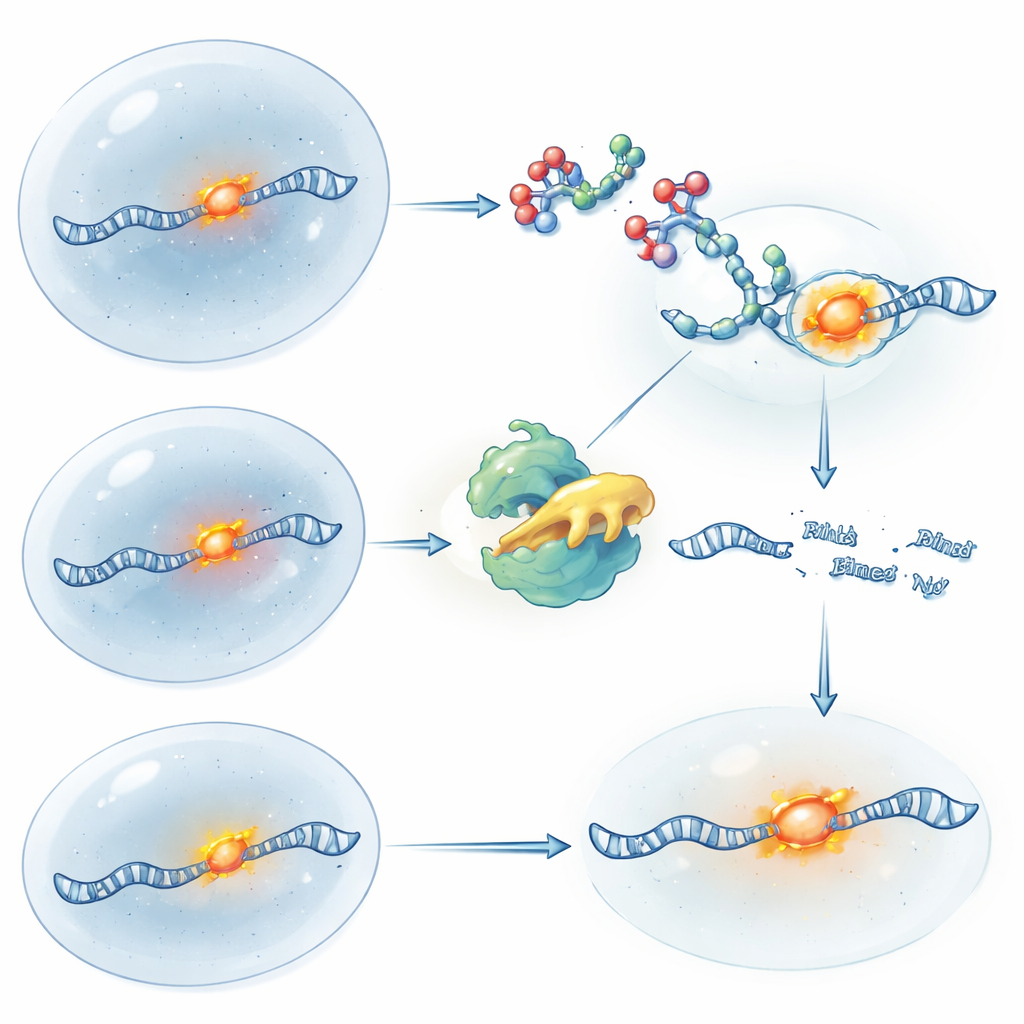
Włączanie i wyłączanie kontroli RNA światłem
Aby zyskać jeszcze dokładniejszą kontrolę nad czasem, zespół opracował wrażliwe na światło wersje swoich RIBOTAC. W jednym projekcie cząsteczka zaczyna aktywna i jest „wyłączana”, gdy krótki impuls ultrafioletu przecina wbudowane zabezpieczenie, zatrzymując dalsze cięcie i pozwalając na odbudowę świeżego RNA. W innym rozwiązaniu RIBOTAC jest zablokowany i nieaktywny dopóki światło nie usunie grupy blokującej, nagle uwalniając jego zdolność do przecinania RNA. Stosując te narzędzia wobec RNA ATF4, badacze mogli naśladować logikę wyłączenia genu i jego przywrócenia czysto za pomocą chemii i światła, jednocześnie śledząc lokalizację RNA przez fluorescencję. Podejście to pozwala naukowcom pytać nie tylko gdzie RNA się znajduje, lecz także co dzieje się z komórką, gdy to RNA jest usunięte lub przywrócone w precyzyjnych momentach.
Ujawnianie, jak długie RNA chroni genom
Autorzy zwrócili się następnie do długiego RNA o nazwie NORAD, znanego z udziału w zachowaniu integralności chromosomów. NORAD gromadzi się z białkami Pumilio w odrębnych kroplach zwanych NP bodies w cytoplazmie. Oznaczając NORAD i minimalny fragment NORAD (circPRE8) za pomocą Clivia-HT, mogli wizualizować te zespoły i selektywnie usuwać RNA. Gdy NORAD lub circPRE8 były obecne, białka Pumilio tworzyły jasne punkty, a komórki miały mniej błędów segregacji chromosomów. Po degradacji oznakowanego RNA przez RIBOTAC krople zniknęły, białka Pumilio się rozproszyły, a błędy chromosomowe wzrosły. Eksperymenty te pokazują, że konkretne regiony NORAD są niezbędne do tworzenia ochronnych kropli białkowo‑RNA, które chronią genom.
Co to oznacza dla przyszłej biologii komórki
Podsumowując, praca wprowadza wszechstronny „wtyczkowy” znacznik RNA, który pozwala wybranemu RNA być jednocześnie widocznym i precyzyjnie usuwanym w komórce, nawet w delikatnych, ciekopodobnych przedziałach. Łącząc jasne obrazowanie z ukierunkowanym niszczeniem oraz dodając przełączniki on–off sterowane światłem, system Clivia-HT umożliwia sprawdzenie, czy sama obecność RNA w strukturze rzeczywiście ma znaczenie dla zachowania komórki. Ten zestaw narzędzi pomoże badaczom pójść dalej niż statyczne obrazy lokalizacji RNA i przeprowadzać eksperymenty przyczynowe, które ujawnią, jak konkretne RNA kształtują odpowiedzi na stres, tworzenie kropli i stabilność genomu.
Cytowanie: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Słowa kluczowe: Obrazowanie RNA, kondensaty rozdzielone fazowo, degradacja RNA, chemia sterowana światłem, długie RNA niekodujące