Clear Sky Science · es
Un aptámero de ARN ortogonal para la regulación dirigida de ARN en compartimentos subcelulares separados por fase
Observar y Controlar el ARN Dentro de Pequeñas Gotas Celulares
Dentro de cada célula, las cadenas de ARN se sintetizan, se transportan y se eliminan constantemente. Muchos de estos ARN se agrupan en pequeñas gotas con comportamiento líquido que flotan en el interior celular. Estas gotas ayudan a organizar la química de la vida, pero son difíciles de estudiar en tiempo real. Este artículo describe un nuevo conjunto de herramientas moleculares que permite a los científicos tanto iluminar ARN específicos como borrarlos deliberadamente dentro de esas gotas, revelando qué hacen realmente esos ARN en células vivas.
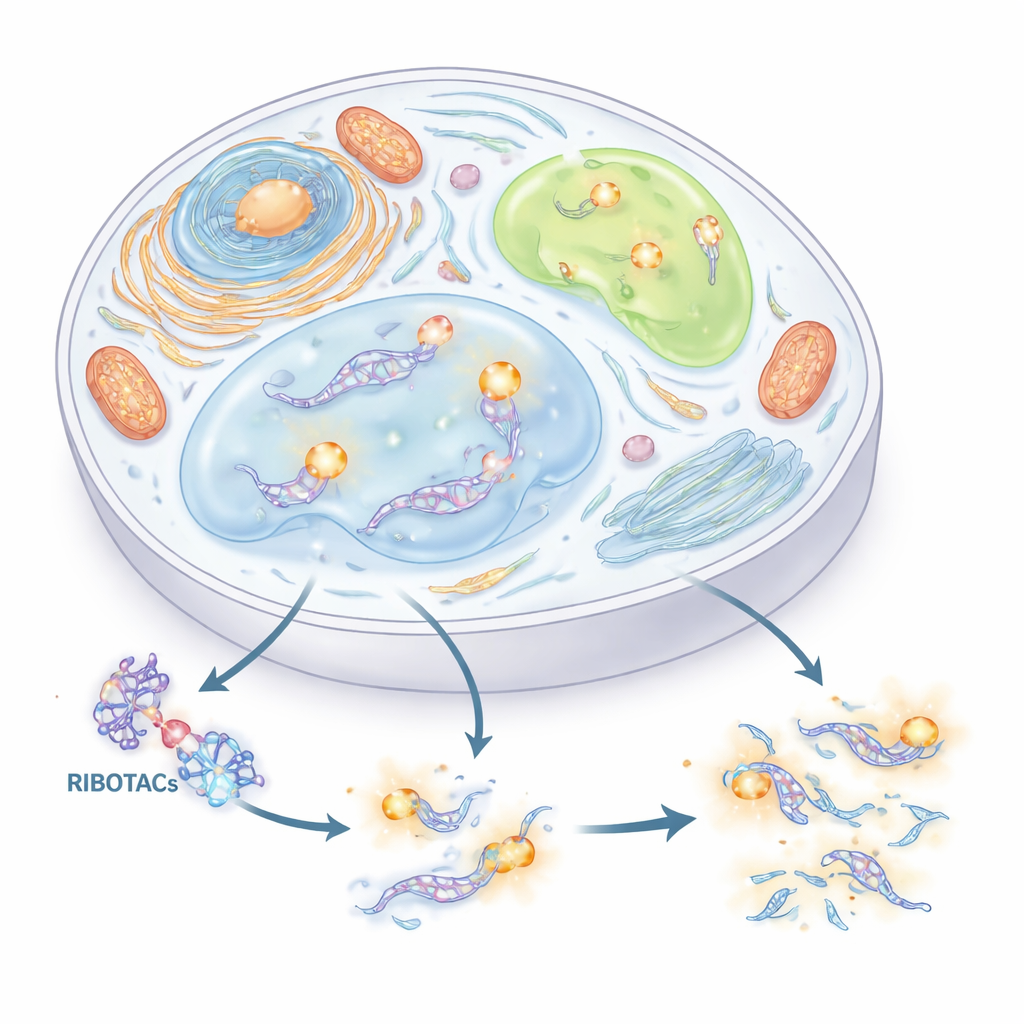
Un Nuevo Asidero para Encontrar y Cortar ARN
Los autores se propusieron construir un sistema preciso y doble para rastrear y controlar ARN. Combinaron dos ideas. La primera es una “etiqueta” corta de ARN (un aptámero) que puede plegarse y atrapar una pequeña molécula complementaria. La segunda es una clase de moléculas diseñadas llamadas RIBOTACs, que se unen a un ARN elegido y reclutan una enzima natural que corta ARN para destruirlo. Mediante un cribado cuidadoso de miles de pequeñas moléculas y cientos de estructuras de ARN, el equipo identificó una etiqueta compacta de ARN, derivada de una secuencia viral llamada HIV-TAR, y la optimizó hasta obtener un aptámero que llamaron HT. A continuación confeccionaron RIBOTACs que reconocen HT y reclutan la enzima celular RNase L, convirtiendo cualquier ARN que lleve HT en un blanco susceptible de destrucción selectiva.
Añadir un Color Brillante para Seguir el ARN en Células Vivas
Para hacer visibles estos ARN etiquetados, los investigadores fusionaron HT con un aptámero fluorescente separado llamado Clivia, que brilla en tonos naranja-rojo cuando se une a un tinte inocuo (NBSI). La etiqueta híbrida resultante, Clivia-HT, confiere a cada ARN marcado dos capacidades distintas: el lado Clivia atrae el tinte luminoso para la imagen, mientras que el lado HT es reconocido por el RIBOTAC para el corte controlado. El equipo mostró que estas dos funciones operan de forma independiente: el tinte ilumina Clivia sin afectar la degradación, y el RIBOTAC se une a HT y desencadena el corte sin apagar la señal fluorescente hasta que el propio ARN se elimina. Repetir Clivia-HT varias veces en un mismo ARN aumentó el brillo lo suficiente como para seguir moléculas etiquetadas en células vivas.
Sondeando Roles Ocultos del ARN en Gotas de Estrés
Equipados con esta etiqueta dual, los autores exploraron ARN dentro de compartimentos subcelulares separados por fase —estructuras tipo gota que se forman sin membranas. Primero insertaron Clivia-HT en el ARN nuclear pequeño U1, que marca los cuerpos U, un tipo de gránulo rico en ARN. Cuando las células se estresaron, estos cuerpos U se iluminaron; al añadir el RIBOTAC dirigido a HT la señal se borró gradualmente y disminuyó el número de cuerpos U, pero solo cuando la enzima cortadora RNase L estaba presente. A continuación, etiquetaron el ARNm ATF4 dentro de gránulos de estrés, gotas que aparecen durante situaciones de inconveniencia celular. Aunque el ARN ATF4 se acumuló claramente en estos gránulos y pudo degradarse a demanda, su eliminación no cambió cómo se formaban o disolvían los gránulos. Esto indica que, a pesar de su presencia allí, el ARN ATF4 no es un motor clave de la dinámica de los gránulos de estrés.
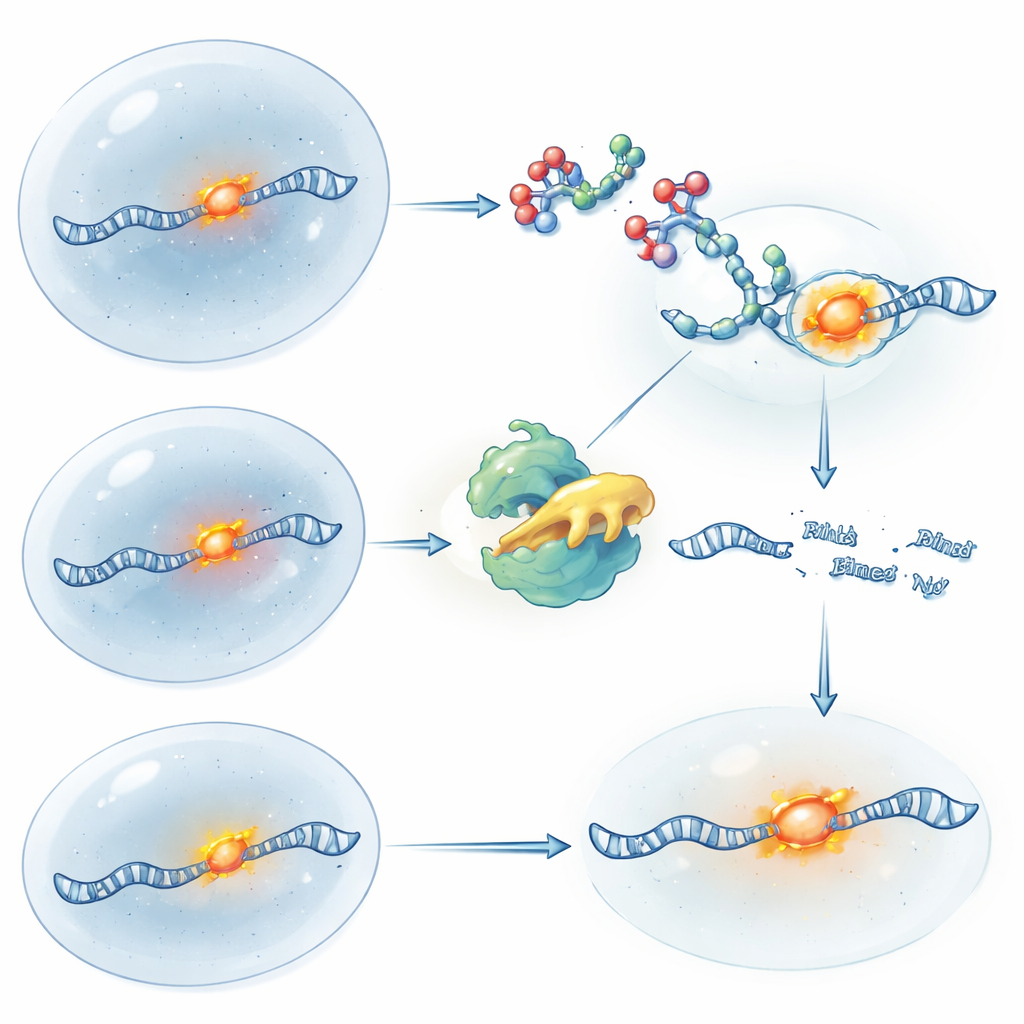
Encender y Apagar el Control del ARN con Luz
Para obtener un control temporal aún más fino, el equipo creó versiones fotosensibles de sus RIBOTACs. En un diseño, la molécula comienza activa y se “apaga” cuando un breve pulso de luz ultravioleta rompe un enlace de seguridad incorporado, deteniendo más cortes y permitiendo que ARN nuevo se regenere. En el otro diseño, el RIBOTAC está “encerrado” e inactivo hasta que la luz elimina el grupo bloqueador, liberando de repente su capacidad de cortar ARN. Usando estas herramientas sobre el ARN ATF4, los investigadores pudieron imitar la lógica de una eliminación génica y su restauración puramente con química y luz, todo mientras la ubicación del ARN se seguía por fluorescencia. Este enfoque permite a los científicos preguntar no solo dónde está un ARN, sino qué le ocurre a la célula cuando ese ARN se elimina o restaura en momentos precisos.
Revelando Cómo un ARN Largo Protege el Genoma
Los autores se centraron después en un ARN largo llamado NORAD, conocido por ayudar a preservar la integridad de los cromosomas. NORAD se agrupa con proteínas Pumilio en gotas distintas llamadas cuerpos NP en el citoplasma. Al etiquetar NORAD y un fragmento mínimo de NORAD (circPRE8) con Clivia-HT, pudieron visualizar estos ensamblajes y borrar selectivamente el ARN. Cuando NORAD o circPRE8 estaban presentes, las proteínas Pumilio formaban puntos brillantes y las células mostraban menos errores en la segregación cromosómica. Cuando el ARN etiquetado fue degradado por RIBOTAC, las gotas desaparecieron, las proteínas Pumilio se dispersaron y aumentaron los errores cromosómicos. Estos experimentos demuestran que regiones específicas de NORAD son esenciales para formar gotas protectoras de proteína–ARN que salvaguardan el genoma.
Qué Significa Esto para la Biología Celular Futura
En resumen, este trabajo presenta una etiqueta de ARN versátil “enchufable” que permite que cualquier ARN elegido pueda verse y borrarse con precisión dentro de la célula, incluso dentro de delicados compartimentos con comportamiento líquido. Al unir imágenes brillantes con destrucción dirigida, y añadir conmutadores fotoquímicos de encendido/apagado, el sistema Clivia-HT posibilita probar si la mera presencia de un ARN en una estructura realmente importa para el comportamiento celular. Este conjunto de herramientas ayudará a los investigadores a avanzar más allá de imágenes estáticas de la localización del ARN hacia experimentos causales que revelen cómo RNAs específicos moldean las respuestas al estrés, la formación de gotas y la estabilidad del genoma.
Cita: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Palabras clave: Imagen de ARN, condensados separados por fase, degradación de ARN, química controlada por luz, ARN largo no codificante