Clear Sky Science · de
Ein orthogonaler RNA-Aptamer zur gezielten RNA-Regulation in phasenseparierten subzellulären Kompartimenten
RNA in winzigen Zelltröpfchen beobachten und steuern
In jeder Zelle werden ständig RNA-Stränge hergestellt, transportiert und abgebaut. Viele dieser RNAs sammeln sich in winzigen, flüssigkeitsähnlichen Tröpfchen, die im Zellinneren schweben. Diese Tröpfchen helfen, die zellulären Reaktionen zu organisieren, sind aber in Echtzeit schwer zu untersuchen. Diese Arbeit beschreibt ein neues molekulares Werkzeug, mit dem Forschende bestimmte RNAs in diesen Tröpfchen sowohl sichtbar machen als auch gezielt entfernen können, sodass sich ihre tatsächlichen Funktionen in lebenden Zellen aufdecken lassen.
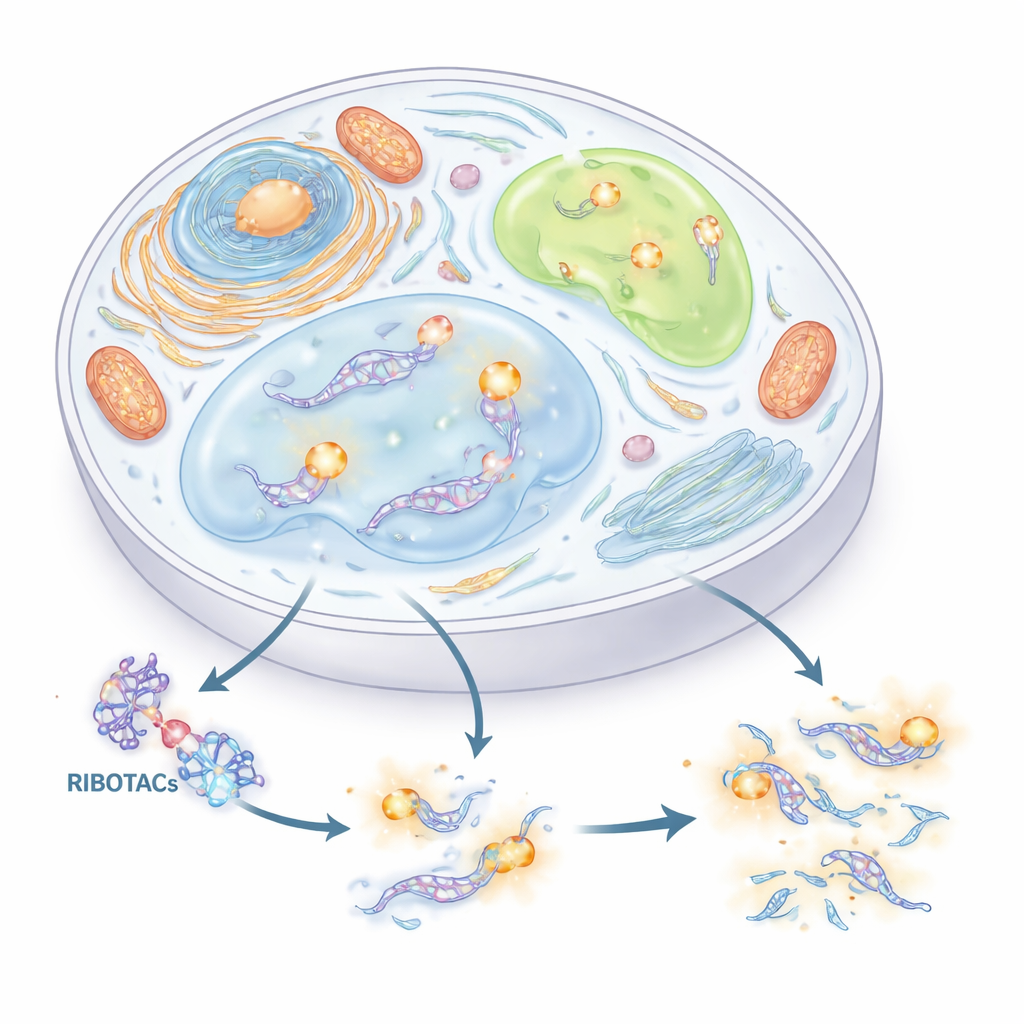
Ein neuer Griff zum Finden und Schneiden von RNA
Die Autor:innen wollten ein präzises Zwei-in-eins-System entwickeln, um RNA zu verfolgen und zu kontrollieren. Sie kombinierten zwei Konzepte. Das erste ist ein kurzer RNA-„Tag“ (ein Aptamer), der sich falten und ein passendes kleines Molekül binden kann. Das zweite ist eine Klasse von Designer-Molekülen, genannt RIBOTACs, die an eine ausgewählte RNA binden und dann ein natürliches RNA-schneidendes Enzym rekrutieren, um sie zu zerstören. Durch sorgfältiges Screening von Tausenden kleiner Moleküle und Hunderten von RNA-Faltungen identifizierte das Team einen kompakten RNA-Tag, abgeleitet von einer viralen Sequenz namens HIV-TAR, und optimierte ihn zu einem Aptamer, das sie HT nennen. Anschließend bauten sie RIBOTACs, die HT erkennen und das zelluläre RNase-L-Enzym heranziehen, wodurch jede RNA, die HT trägt, zu einem selektiv zerstörbaren Ziel wird.
Eine helle Farbe, um RNA in lebenden Zellen zu verfolgen
Um diese markierten RNAs sichtbar zu machen, fusionierten die Forschenden HT mit einem separaten fluoreszierenden Aptamer namens Clivia, das orange-rot leuchtet, wenn es ein unschädliches Färbemittel (NBSI) bindet. Der resultierende Hybridtag Clivia-HT verleiht jeder markierten RNA zwei unterschiedliche Fähigkeiten: Die Clivia-Seite zieht das leuchtende Farbstoffmolekül für die Bildgebung an, während die HT-Seite vom RIBOTAC für die gezielte Zerstörung erkannt wird. Das Team zeigte, dass diese beiden Funktionen unabhängig arbeiten: der Farbstoff bringt Clivia zum Leuchten, ohne den Abbau zu beeinflussen, und das RIBOTAC bindet HT und löst das Schneiden aus, ohne das Fluoreszenzsignal zu dämpfen, bis die RNA selbst entfernt ist. Durch mehrfache Wiederholung von Clivia-HT auf einer RNA erhöhten sie die Helligkeit genug, um markierte Moleküle in lebenden Zellen zu verfolgen.
Verborgene RNA-Rollen in Stress-Tröpfchen untersuchen
Mit diesem Doppel-Tag erforschten die Autor:innen RNAs innerhalb phasenseparierter subzellulärer Kompartimente—tröpfchenartige Strukturen, die ohne Membranen entstehen. Zuerst setzten sie Clivia-HT in die U1 small nuclear RNA ein, die U-Bodies markiert, eine Art RNA-reicher Granula. Unter Zellstress leuchteten diese U-Bodies auf; das Hinzufügen des HT-gerichteten RIBOTACs löschte dann allmählich das Signal und reduzierte die Anzahl der U-Bodies, jedoch nur, wenn das schneidende Enzym RNase L vorhanden war. Als Nächstes markierten sie die ATF4-Boten-RNA in Stressgranula, Tröpfchen, die bei zellulären Belastungen auftreten. Obwohl sich ATF4-RNA deutlich in diesen Granula ansammelte und bei Bedarf abgebaut werden konnte, veränderte ihr Entfernen weder die Bildung noch die Auflösung der Granula. Das deutet darauf hin, dass ATF4-RNA trotz ihrer Anwesenheit dort kein Schlüsseltreiber der Dynamik von Stressgranula ist.
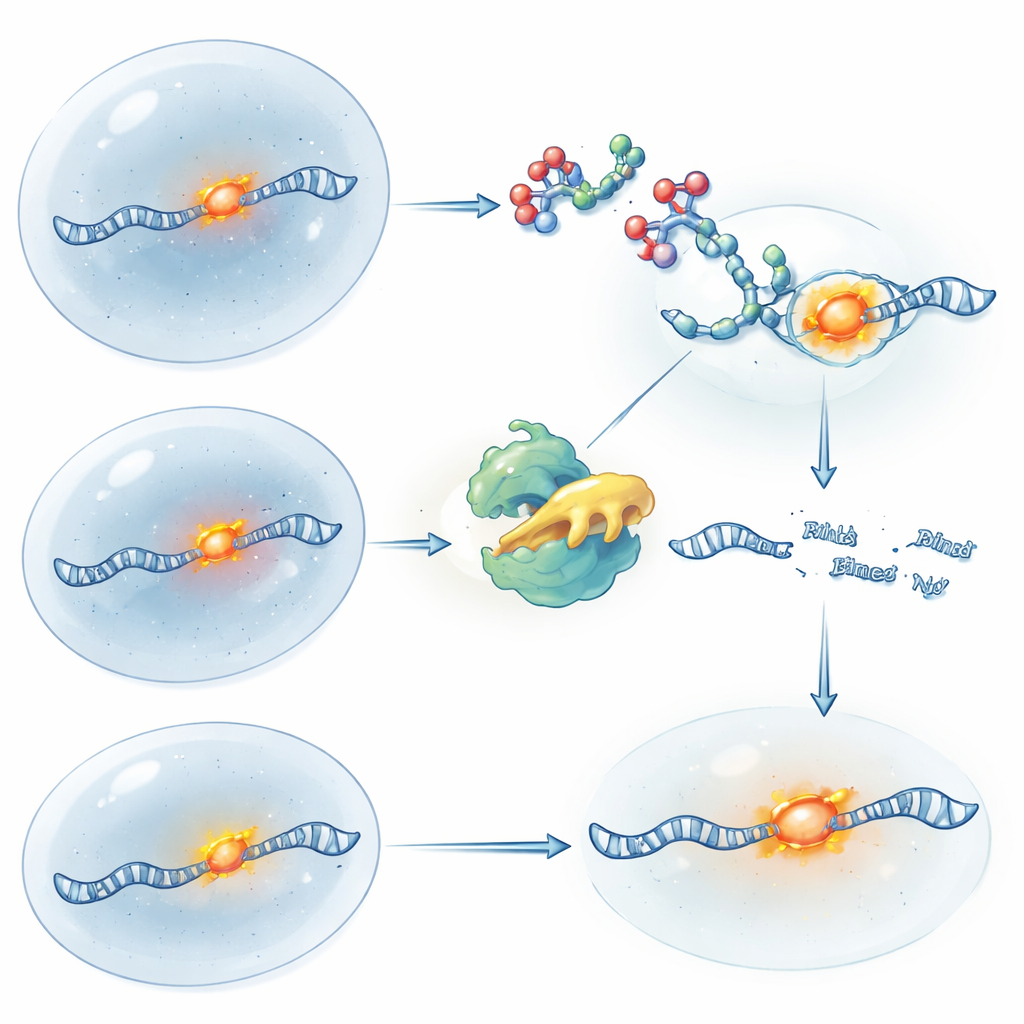
RNA-Steuerung mit Licht ein- und ausschalten
Um die zeitliche Kontrolle weiter zu verfeinern, entwickelten die Forschenden lichtempfindliche Versionen ihrer RIBOTACs. In einem Design ist das Molekül zunächst aktiv und wird durch einen kurzen UV-Lichtimpuls „abgeschaltet“, der eine eingebaute Sicherheitsverbindung spaltet, wodurch weiteres Schneiden gestoppt wird und frische RNA wieder aufgebaut werden kann. Im anderen Design ist das RIBOTAC eingekapselt und inaktiv, bis Licht die blockierende Gruppe entfernt und seine RNA-schneidende Wirkung plötzlich freisetzt. Mit diesen Werkzeugen auf ATF4-RNA konnten die Forschenden das Logikprinzip von Gen-Knockout und Gen-Wiederherstellung rein mit Chemie und Licht nachbilden, während die Position der RNA weiterhin durch Fluoreszenz verfolgt wurde. Dieser Ansatz erlaubt es, nicht nur zu fragen, wo eine RNA ist, sondern was mit der Zelle geschieht, wenn diese RNA zu exakt definierten Zeitpunkten entfernt oder wiederhergestellt wird.
Aufdecken, wie eine lange RNA das Genom schützt
Die Autor:innen richteten ihr Augenmerk anschließend auf eine lange RNA namens NORAD, die dafür bekannt ist, die Integrität von Chromosomen zu bewahren. NORAD sammelt sich zusammen mit Pumilio-Proteinen in charakteristischen Tröpfchen, den sogenannten NP-Bodies, im Zytoplasma. Durch das Markieren von NORAD und eines minimalen NORAD-Fragmentes (circPRE8) mit Clivia-HT konnten sie diese Assemblies visualisieren und die RNA selektiv löschen. Wenn NORAD oder circPRE8 vorhanden war, bildeten Pumilio-Proteine helle Punktstrukturen und Zellen zeigten weniger Fehler bei der Chromosomenaufteilung. Wurde die markierte RNA durch RIBOTAC abgebaut, verschwanden die Tröpfchen, die Pumilio-Proteine dispergierten und die Chromosomenfehler nahmen zu. Diese Experimente zeigen, dass spezifische NORAD-Regionen essenziell für die Bildung protektiver Protein–RNA-Tröpfchen sind, die das Genom schützen.
Was das für die künftige Zellbiologie bedeutet
Zusammengefasst stellt diese Arbeit einen vielseitigen „Plug-in“-RNA-Tag vor, der jede gewählte RNA innerhalb der Zelle, sogar in empfindlichen flüssigkeitsähnlichen Kompartimenten, sowohl sichtbar machen als auch präzise löschen kann. Durch die Verbindung heller Bildgebung mit gezielter Zerstörung und der Ergänzung durch lichtbasierte An- und Ausschalter ermöglicht das Clivia-HT-System, zu testen, ob die bloße Anwesenheit einer RNA in einer Struktur tatsächlich das Zellverhalten beeinflusst. Dieses Toolkit wird Forschenden helfen, über statische Abbildungen von RNA-Lokalisation hinauszugehen und kausale Experimente durchzuführen, die zeigen, wie spezifische RNAs Stressantworten, Tröpfchenbildung und Genomstabilität gestalten.
Zitation: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Schlüsselwörter: RNA-Bildgebung, phasenseparierte Kondensate, RNA-Abbau, lichtgesteuerte Chemie, lange nicht-kodierende RNA