Clear Sky Science · nl
Een orthogonaal RNA-aptameer voor gerichte RNA-regulatie in fasegescheiden subcellulaire compartimenten
RNA bekijken en beheersen in piepkleine celdruppels
Binnen elke cel worden RNA-strengen voortdurend aangemaakt, verplaatst en afgebroken. Veel van deze RNA’s verzamelen zich in kleine, vloeibare druppels die vrij in het celinterieur zweven. Deze druppels helpen de chemie van het leven te organiseren, maar ze zijn moeilijk in realtime te bestuderen. Dit artikel beschrijft een nieuwe moleculaire gereedschapskist waarmee wetenschappers specifieke RNA’s zowel kunnen laten oplichten als doelbewust kunnen wissen binnen deze druppels, waardoor zichtbaar wordt wat die RNA’s daadwerkelijk doen in levende cellen.
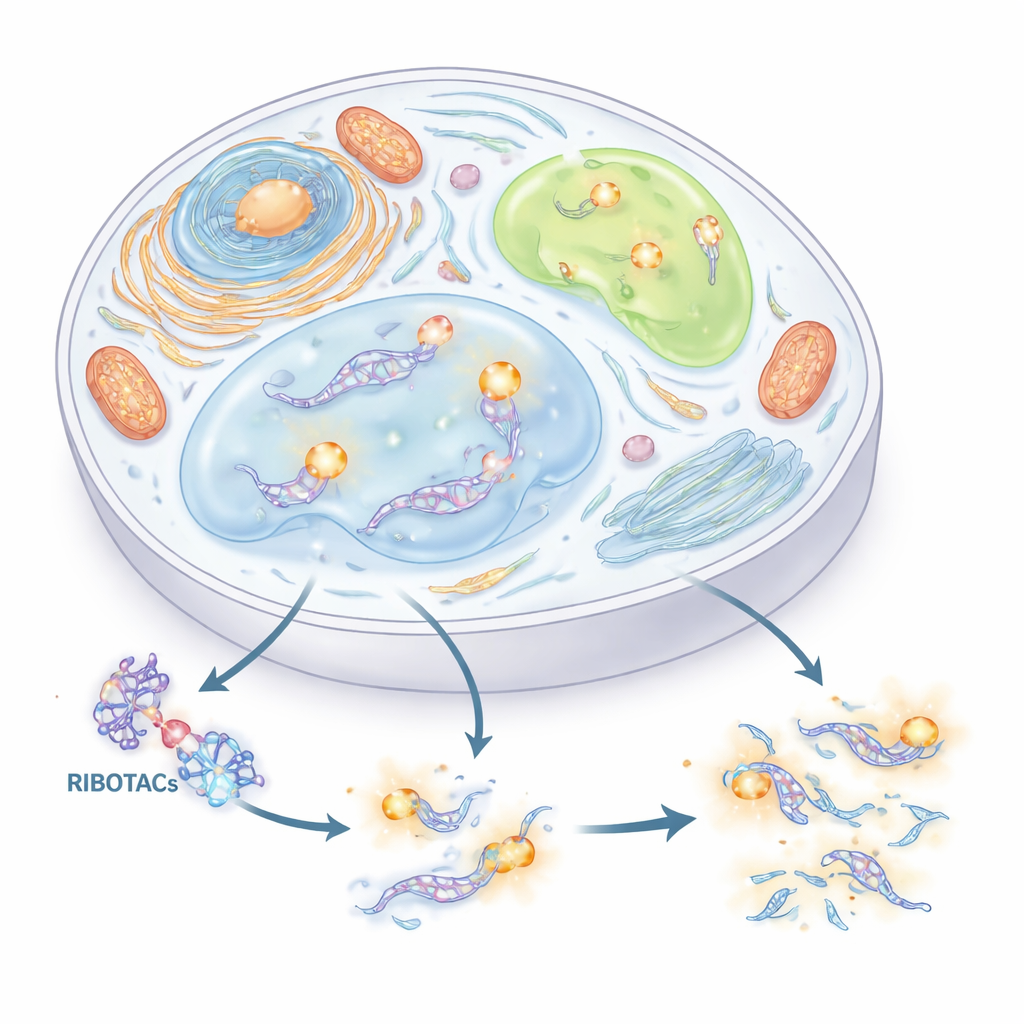
Een nieuwe greep om RNA te vinden en te knippen
De auteurs wilden een precies, twee-in-één systeem bouwen om RNA te volgen en te beheersen. Ze combineerden twee ideeën. Het eerste is een kort RNA-“label” (een aptameer) dat kan vouwen in een vorm en een overeenkomstig klein molecuul kan binden. Het tweede is een klasse van ontwerp-moleculen genaamd RIBOTACs, die zich hechten aan een gekozen RNA en vervolgens een natuurlijk RNA-knipend enzym rekruteren om het te vernietigen. Door zorgvuldig duizenden kleine moleculen en honderden RNA-vormen te screenen, identificeerde het team een compact RNA-label, afgeleid van een viraalsequentie genaamd HIV-TAR, en optimaliseerde het tot een aptameer dat ze HT noemen. Ze bouwden vervolgens RIBOTACs die HT herkennen en het celenzym RNase L naar zich toe trekken, waardoor elk RNA dat HT draagt een selectief afbreekbaar doelwit wordt.
Een felle kleur toevoegen om RNA in levende cellen te volgen
Om deze gelabelde RNA’s zichtbaar te maken, fuseerden de onderzoekers HT met een apart fluorescent aptameer genaamd Clivia, dat oranje-rood oplicht wanneer het een onschadelijke kleurstof (NBSI) bindt. Het resulterende hybride label, Clivia-HT, geeft elk gelabeld RNA twee verschillende eigenschappen: de Clivia-zijde trekt de gloeiende kleurstof aan voor beeldvorming, terwijl de HT-zijde door de RIBOTAC wordt herkend voor gecontroleerd knippen. Het team toonde aan dat deze twee functies onafhankelijk werken: de kleurstof laat Clivia oplichten zonder afbraak te beïnvloeden, en de RIBOTAC bindt HT en veroorzaakt knippen zonder het fluorescentiesignaal te dempen totdat het RNA zelf is verwijderd. Door Clivia-HT meerdere keren achter elkaar op één RNA te plaatsen, verhoogden ze de helderheid genoeg om gelabelde moleculen in levende cellen te volgen.
Verborgen RNA-functies onderzoeken in stressdruppels
Gewapend met dit dubbele label onderzochten de auteurs RNA’s binnen fasegescheiden subcellulaire compartimenten — druppelachtige structuren die zonder membranen ontstaan. Ze voegden eerst Clivia-HT in U1 klein nucleus-RNA, dat U-lichaampjes markeert, een type RNA-rijke korrel. Wanneer cellen gestrest waren, lichtten deze U-lichaampjes op; het toevoegen van de HT-gerichte RIBOTAC wist vervolgens geleidelijk het signaal uit en verminderde het aantal U-lichaampjes, maar alleen wanneer het knipenzym RNase L aanwezig was. Vervolgens labelden ze ATF4 boodschapper-RNA in stressgranules, druppels die verschijnen tijdens cellulaire stress. Hoewel ATF4-RNA duidelijk in deze granules ophoopte en op verzoek afgebroken kon worden, veranderde het verwijderen ervan niet hoe de granules vormden of oplosten. Dit wijst erop dat ATF4-RNA, ondanks zijn aanwezigheid daar, geen sleutelrol speelt in de dynamiek van stressgranules.
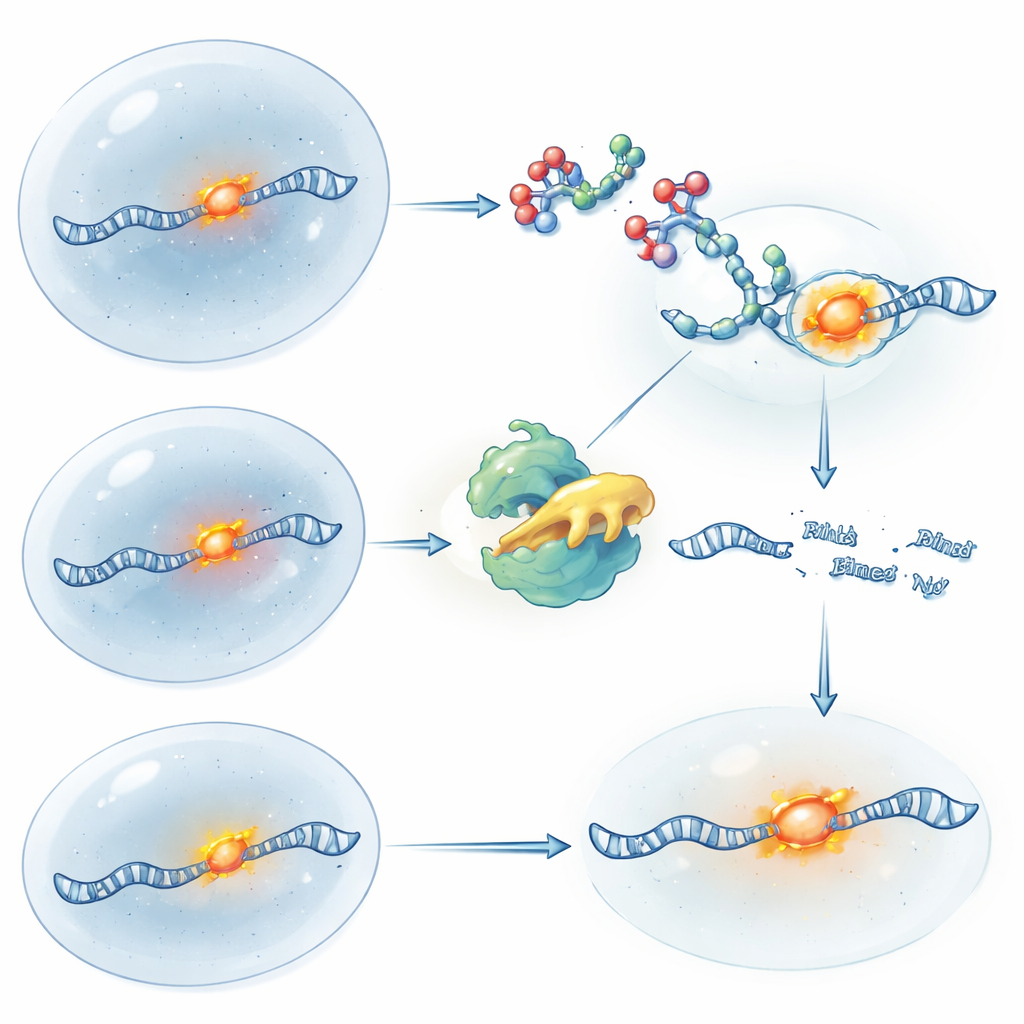
RNA-regulatie aan- en uitzetten met licht
Om nog fijnmaziger timingcontrole te verkrijgen, maakten de onderzoekers lichtgevoelige versies van hun RIBOTACs. In één ontwerp is het molecuul aanvankelijk actief en wordt het “uitgeschakeld” wanneer een korte puls ultraviolet licht een ingebouwde veiligheidsschakel knipt, waardoor verder knippen stopt en nieuw RNA zich kan herstellen. In het andere ontwerp is de RIBOTAC gecaged en inactief totdat licht de blokkerende groep verwijdert, waarna zijn RNA-knipkracht plotseling vrij komt. Met deze hulpmiddelen op ATF4-RNA konden de onderzoekers de logica van genverwijdering en genherstel nabootsen puur met chemie en licht, terwijl de locatie van het RNA via fluorescentie werd gevolgd. Deze benadering stelt wetenschappers in staat niet alleen te vragen waar een RNA zich bevindt, maar ook wat er met de cel gebeurt wanneer dat RNA op nauwkeurige momenten wordt verwijderd of hersteld.
Onthullen hoe een lang RNA het genoom beschermt
De auteurs richtten zich vervolgens op een lang RNA genaamd NORAD, waarvan bekend is dat het helpt de integriteit van chromosomen te behouden. NORAD verzamelt zich met Pumilio-eiwitten in afzonderlijke druppels die NP-lichaampjes worden genoemd in het cytoplasma. Door NORAD en een minimaal NORAD-fragment (circPRE8) te labelen met Clivia-HT, konden ze deze assemblages visualiseren en selectief het RNA wissen. Wanneer NORAD of circPRE8 aanwezig was, vormden Pumilio-eiwitten felle puncta en hadden cellen minder fouten bij chromosoomscheiding. Toen het gelabelde RNA door RIBOTAC werd afgebroken, verdwenen de druppels, verspreidden de Pumilio-eiwitten zich en namen de chromosoomfouten toe. Deze experimenten tonen aan dat specifieke NORAD-regio’s essentieel zijn voor het vormen van beschermende eiwit–RNA-druppels die het genoom beveiligen.
Wat dit betekent voor toekomstige celbiologie
Samengevat introduceert dit werk een veelzijdig “plug-in” RNA-label waarmee elk gekozen RNA zowel zichtbaar als nauwkeurig te verwijderen is binnen de cel, zelfs binnen kwetsbare vloeibare compartimenten. Door heldere beeldvorming te combineren met gerichte vernietiging, en lichtgestuurde aan/uit-schakelaars toe te voegen, maakt het Clivia-HT-systeem het mogelijk te testen of de loutere aanwezigheid van een RNA in een structuur werkelijk van belang is voor celgedrag. Deze gereedschapskist zal onderzoekers helpen voorbij statische beelden van RNA-locatie te komen naar causaal onderzoek dat onthult hoe specifieke RNA’s stressreacties, druppelvorming en genoomstabiliteit beïnvloeden.
Bronvermelding: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Trefwoorden: RNA-beeldvorming, fasegescheiden condensaten, RNA-afbraak, lichtgestuurde chemie, lange niet-coderende RNA