Clear Sky Science · sv
En ortogonal RNA-aptamer för riktad RNA-reglering i faseskiljda subcellulära kompartiment
Observera och kontrollera RNA inuti små cell-droppar
Inne i varje cell bildas, transporteras och bryts RNA-strängar ständigt ned. Många av dessa RNA samlas i små, vätskeliknande droppar som svävar i cellens inre. Dessa droppar hjälper till att organisera cellens kemi, men de är svåra att studera i realtid. Denna artikel beskriver ett nytt molekylärt verktyg som låter forskare både belysa specifika RNA och avsiktligt radera dem inuti dessa droppar, vilket visar vad dessa RNA faktiskt gör i levande celler.
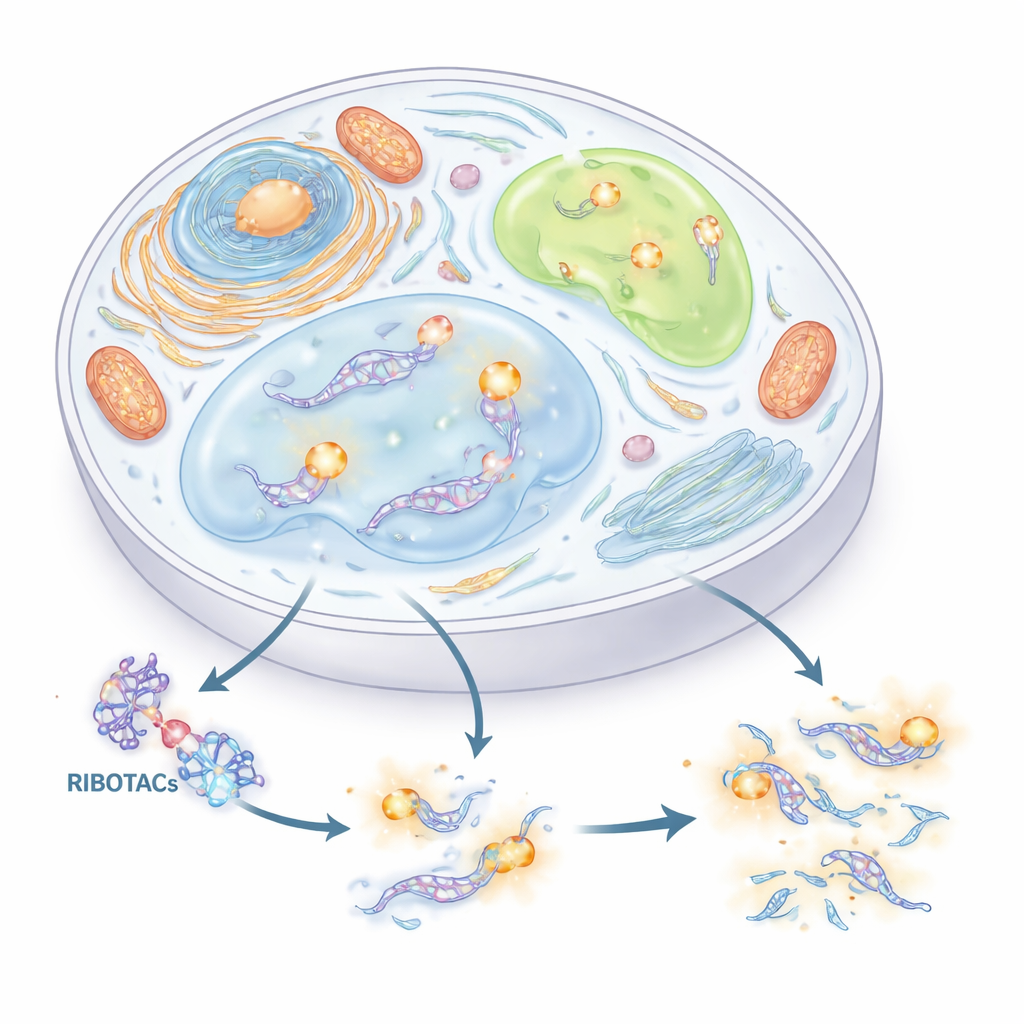
Ett nytt grepp för att hitta och klippa RNA
Författarna ville bygga ett precist, två-i-ett-system för att spåra och kontrollera RNA. De kombinerade två idéer. Den första är en kort RNA-”tagg” (en aptamer) som kan veckas till en form och fånga en matchande liten molekyl. Den andra är en klass av designade molekyler som kallas RIBOTACs, vilka fäster vid ett valt RNA och sedan rekryterar ett naturligt RNA-skärytem för att destruera det. Genom att noggrant skärma igenom tusentals små molekyler och hundratals RNA-strukturer identifierade teamet en kompakt RNA-tagg, härledd från en viral sekvens kallad HIV-TAR, och optimerade den till en aptamer de kallar HT. De byggde därefter RIBOTACs som känner igen HT och rekryterar cellens RNase L-enzym, och gör därigenom vilket RNA som bär HT till ett selektivt förgörbart mål.
Lägga till en klar färg för att följa RNA i levande celler
För att göra dessa taggade RNA synliga fäste forskarna HT till en separat fluorescerande aptamer kallad Clivia, som lyser orange-rött när den binder ett ofarligt färgämne (NBSI). Den resulterande hybridtaggen, Clivia-HT, ger varje märkt RNA två skilda förmågor: Clivia-delen attraherar det lysande färgämnet för avbildning, medan HT-delen känns igen av RIBOTAC för kontrollerad klippning. Teamet visade att dessa två funktioner fungerar oberoende: färgämnet lyser upp Clivia utan att påverka nedbrytningen, och RIBOTAC binder HT och triggar klippning utan att dämpa den fluorescerande signalen förrän RNA:t självt försvinner. Genom att upprepa Clivia-HT flera gånger på ett RNA ökade de ljusstyrkan tillräckligt för att följa märkta molekyler i levande celler.
Undersöka dolda RNA-roller i stressdroppar
Beväpnade med denna dubbla tagg utforskade författarna RNA inuti faseskiljda subcellulära kompartiment — dropp-liknande strukturer som bildas utan membran. Först satte de in Clivia-HT i U1 små nukleära RNA, som markerar U-kroppar, en typ av RNA-rik granula. När celler utsattes för stress lyste dessa U-kroppar upp; tillsats av HT-riktad RIBOTAC raderade sedan gradvis signalen och minskade antalet U-kroppar, men endast när klippenzymet RNase L var närvarande. Därefter märkte de ATF4 budbärar-RNA inuti stresskorn, droppar som uppträder vid cellulär press. Även om ATF4-RNA tydligt ackumulerade i dessa korn och kunde degraderas vid behov, förändrade borttagandet inte hur kornen bildades eller löstes upp. Detta tyder på att ATF4-RNA, trots sin närvaro där, inte är en huvuddrivkraft för stresskornens dynamik.
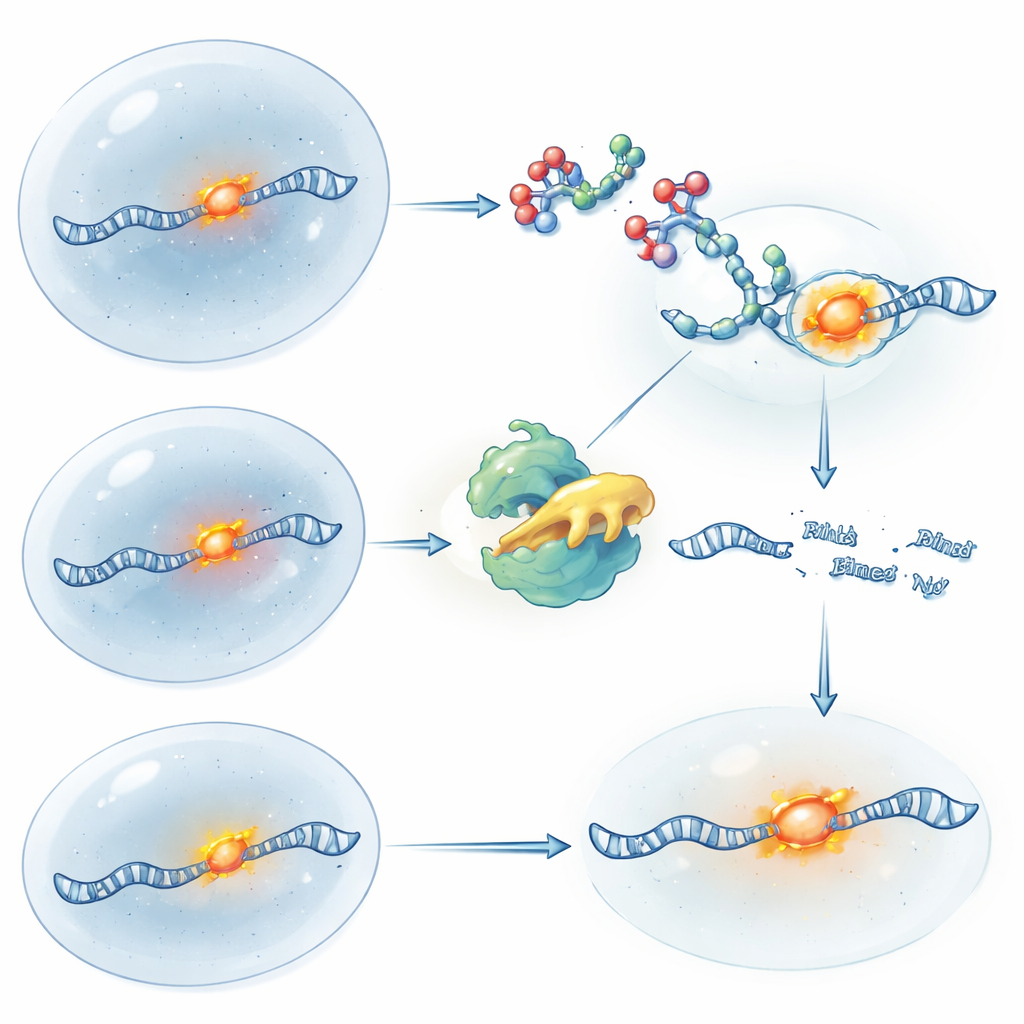
Slå av och på RNA-kontroll med ljus
För att få ännu finare tidskontroll gjorde teamet ljuskänsliga versioner av sina RIBOTACs. I en design börjar molekylen aktiv och ”stängs av” när en kort puls av ultraviolett ljus klyver en inbyggd säkerhetslänk, vilket stoppar fortsatt klippning och tillåter nytt RNA att byggas upp igen. I den andra designen är RIBOTAC innesluten och inaktiv tills ljus avlägsnar blockeringsgruppen och plötsligt släpper lös dess RNA-klippande kraft. Genom att använda dessa verktyg på ATF4-RNA kunde forskarna efterlikna logiken hos genutslagning och genåterställning enbart med kemi och ljus, samtidigt som RNA:ts lokalisering följdes via fluorescens. Detta tillvägagångssätt låter forskare fråga inte bara var ett RNA är, utan vad som händer med cellen när det RNA:t tas bort eller återställs vid precisa tidpunkter.
Avslöja hur ett långt RNA skyddar genomet
Författarna vände sig sedan till ett långt RNA kallat NORAD, känt för att hjälpa bevara kromosomernas integritet. NORAD samlas med Pumilio-proteiner i distinkta droppar kallade NP-kroppar i cytoplasman. Genom att tagga NORAD och en minimal NORAD-fragment (circPRE8) med Clivia-HT kunde de visualisera dessa sammankomster och selektivt radera RNA:t. När NORAD eller circPRE8 var närvarande bildade Pumilio-proteiner ljusa punkter och cellerna hade färre fel vid kromosomsegregering. När det taggade RNA:t degraderades av RIBOTAC försvann dropparna, Pumilio-proteinerna spreds ut och kromosomfelen ökade. Dessa experiment visar att specifika NORAD-regioner är avgörande för att bilda skyddande protein–RNA-droppar som värnar genomet.
Vad detta innebär för framtida cellbiologi
Sammanfattningsvis introducerar detta arbete en mångsidig ”plug-in” RNA-tagg som gör det möjligt att se och precist utplåna valfritt RNA inne i cellen, även inom känsliga vätskeliknande kompartiment. Genom att förena ljusstark avbildning med riktad destruktion, och addera ljusbaserade av-/på-brytare, gör Clivia-HT-systemet det möjligt att testa om ett RNAs blotta närvaro i en struktur faktiskt spelar roll för cellens beteende. Detta verktygslåda kommer att hjälpa forskare att gå bortom statiska bilder av RNA-lokalisering mot kausala experiment som avslöjar hur specifika RNA formar stressrespons, droppbildning och genomstabilitet.
Citering: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Nyckelord: RNA-avbildning, faseskiljda kondensat, RNA-nedbrytning, ljusstyrd kemi, långa icke-kodande RNA