Clear Sky Science · ar
أبتامير RNA متعامد لتنظيم RNA مستهدف داخل حجرات خلوية مفصولة بالطور
مراقبة والتحكم في RNA داخل قطرات خلوية صغيرة
داخل كل خلية، تُصنَع سلاسل RNA باستمرار وتُنقل وتُهدر. تتجمع العديد من هذه الجزيئات داخل قطرات صغيرة شبيهة بالسائل تطفو في داخل الخلية. تساعد هذه القطرات في تنظيم الكيمياء الحيوية للحياة، لكنها صعبة الدراسة في الزمن الحقيقي. يصف هذا البحث مجموعة أدوات جزيئية جديدة تُمكّن العلماء من إضاءة RNA محدد وعن عمد محوه داخل هذه القطرات، كاشفةً عمّا تفعله تلك الجزيئات في الخلايا الحية.
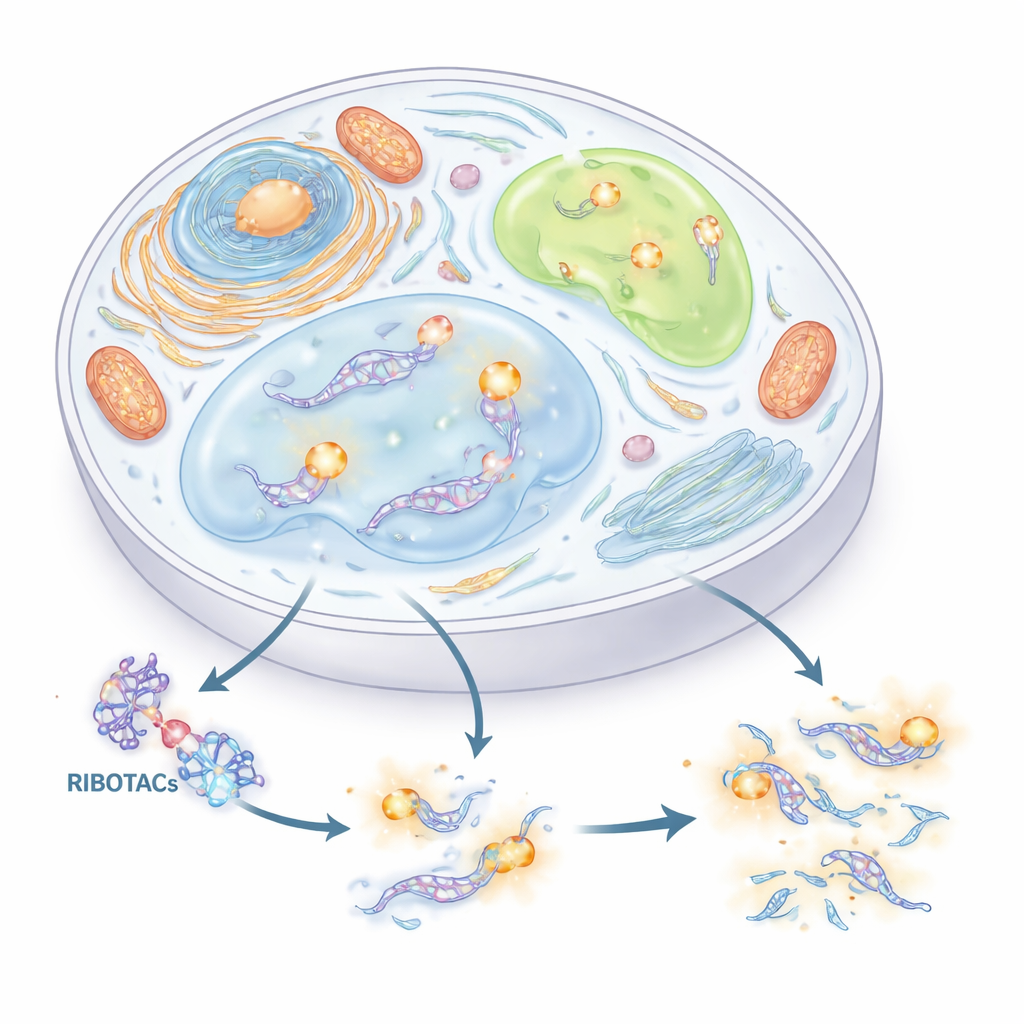
مقبض جديد لاكتشاف وقطع RNA
سعى المؤلفون إلى بناء نظام دقيق يجمع بين تعقب RNA والتحكم فيه. جمعوا فكرتين: الأولى وسم RNA قصير (أبتامير) يمكنه الطيَ إلى شكل يمسك بجزيء صغير مطابق. والثانية فئة من الجزيئات المصمَّمة تسمى RIBOTACs، التي تلتصق بـRNA مختار ثم تجند إنزيمًا طبيعيًا لقطع RNA لتدميره. من خلال فحص آلاف الجزيئات الصغيرة ومئات أشكال RNA، حدَّد الفريق وسم RNA مدمجًا مشتقًا من تسلسل فيروسي يُدعى HIV-TAR، وحسَّنه إلى أبتامير أسموه HT. ثم بنوا RIBOTACs تتعرف على HT وتجذب إنزيم RNase L الخلوي، محوِّلةً أي RNA يحمل HT إلى هدف يمكن تدميره انتقائيًا.
إضافة لون ساطع لتتبع RNA في خلايا حية
لجعل هذه الـRNA الموسومة مرئية، وصل الباحثون HT بأبتامير فلوري مستقل يُدعى Clivia، يضيء بلون أحمر برتقالي عند ربطه بصبغة غير ضارة (NBSI). الوسم الهجين الناتج، Clivia-HT، يمنح كل RNA موسوم سمتين متميزتين: جانب Clivia يجذب الصبغة المتوهجة للتصوير، بينما يُعترف بجانب HT بواسطة RIBOTAC للقطع المتحكم فيه. أظهر الفريق أن هاتين الوظيفتين تعملان بشكل مستقل: الصبغة تُضيء Clivia دون التأثير على التحلل، وRIBOTAC يربط HT ويشغّل القطع دون إضعاف الإشارة الفلورية حتى يُزال الـRNA نفسه. بتكرار Clivia-HT عدة مرات على RNA واحد، عززوا السطوع بما يكفي لتتبع الجزيئات الموسومة في خلايا حية.
استقصاء أدوار RNA الخفية داخل قطرات الإجهاد
مزودين بهذا الوسم المزدوج، استكشف المؤلفون RNAs داخل حجرات خلوية مفصولة بالطور — هياكل شبيهة بالقطرات تتكوّن دون غشاء. أدخلوا أولًا Clivia-HT في RNA النووي الصغير U1، الذي يوسم أجسام U، وهي نوع من الحبيبات الغنية بالـRNA. عند تعرض الخلايا للإجهاد، أضاءت هذه الأجسام؛ ثم أدى إضافة RIBOTAC المستهدف لـHT تدريجيًا إلى محو الإشارة وتقليص عدد أجسام U، لكن فقط بوجود إنزيم القطع RNase L. بعد ذلك، وسموا mRNA لــATF4 داخل حبيبات الإجهاد، وهي قطرات تظهر أثناء الشدائد الخلوية. رغم أن RNA ATF4 تراكم بوضوح في هذه الحبيبات ويمكن تدميره عند الطلب، فإن إزالته لم تغيّر طريقة تكوّن الحبيبات أو ذوبانها. يشير ذلك إلى أن ATF4، رغم وجوده هناك، ليس محركًا أساسيًا لديناميكيات حبيبات الإجهاد.
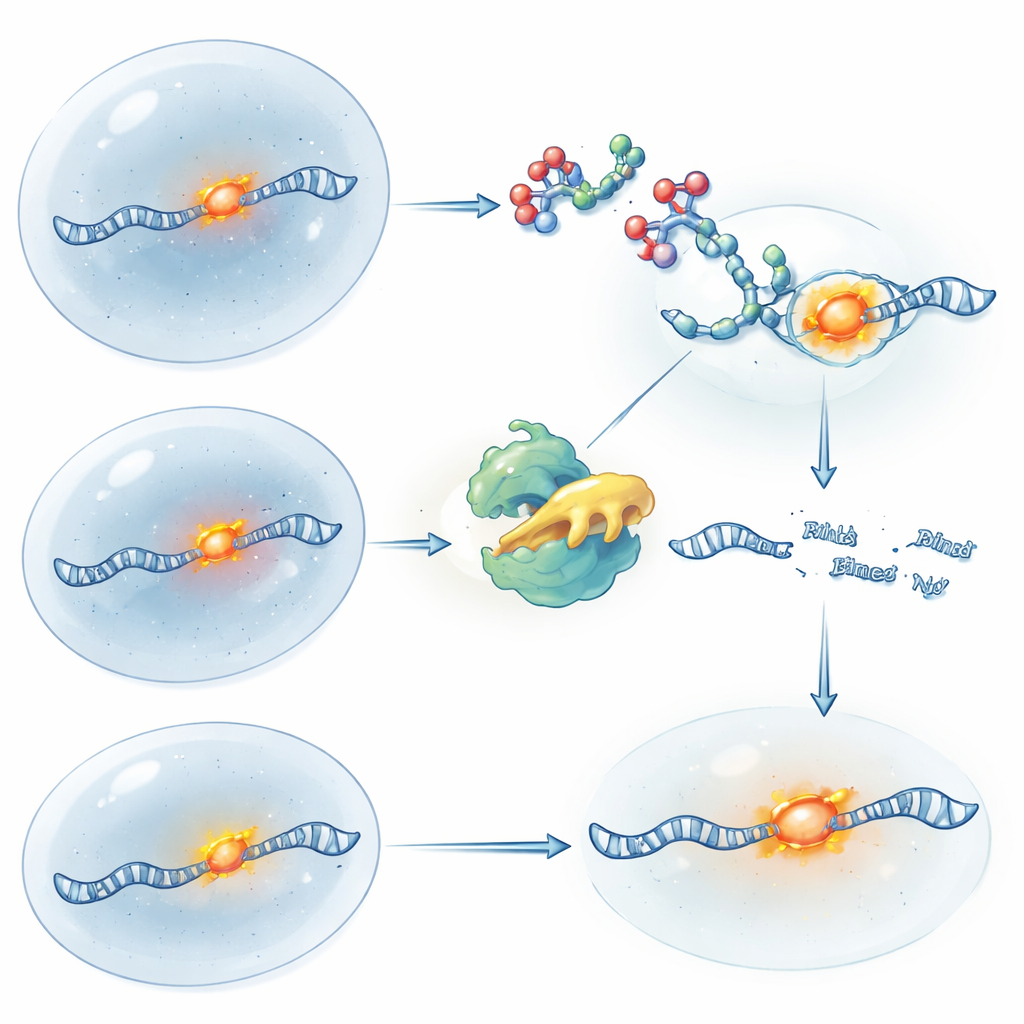
تشغيل وإيقاف التحكم في RNA بالضوء
للحصول على تحكم أدق في التوقيت، صنع الفريق نسخًا حساسة للضوء من RIBOTACs. في تصميم واحد، يبدأ الجزيء نشطًا ثم «يُطفأ» عندما يقص نبضة قصيرة من ضوء فوق بنفسجي حلقة أمان مدمجة، موقفةً القطع ومنتِّحةً الفرصة لبناء RNA جديد. في التصميم الآخر، يكون RIBOTAC محجوزًا وغير نشط حتى يزيل الضوء مجموعة الحجب، مفجِّرًا فجأة قوته القاطعة للـRNA. باستخدام هذه الأدوات على RNA ATF4، تمكّن الباحثون من تقليد منطق حذف جين واستعادته كيميائيًا وبالضوء، مع تتبُّع موقع RNA بصريًا. تتيح هذه المقاربة للعلماء أن يسألوا ليس فقط أين يوجد RNA، بل ماذا يحدث للخلايا عندما يُزال ذلك RNA أو يُستعاد في لحظات محددة بدقة.
كشف كيف يحمي RNA طويل الجينوم
توجه المؤلفون بعد ذلك إلى RNA طويل يُدعى NORAD، المعروف بمساعدته على حفظ سلامة الكروموسومات. يتجمع NORAD مع بروتينات Pumilio في قطرات مميزة تسمى NP bodies في السيتوبلازم. بوَسْم NORAD وشظية صغيرة منه (circPRE8) بـClivia-HT، تمكنوا من تصور هذه التجمُّعات ومحو الـRNA بشكل انتقائي. عندما كان NORAD أو circPRE8 موجودًا، شكَّلت بروتينات Pumilio نقاطًا مضيئة وكانت الخلايا أقل عرضة لأخطاء فصل الكروموسومات. عند تدمير الـRNA الموسوم بواسطة RIBOTAC، اختفت القطرات، تشتتت بروتينات Pumilio، وزادت أخطاء الكروموسوم. تظهر هذه التجارب أن مناطق محددة في NORAD ضرورية لتكوين قطرات بروتينية–RNA واقية تحمي الجينوم.
ما الذي يعنيه هذا لعلم الأحياء الخلوية المستقبلي
خلاصة القول، يقدم هذا العمل وسم RNA «قابل للتركيب» متعدد الاستخدامات يسمح لأي RNA مختار أن يُرى ويُمحى بدقة داخل الخلية، حتى داخل الحجرات الرقيقة الشبيهة بالسائل. من خلال الجمع بين التصوير اللامع والتدمير المستهدف، وإضافة مفاتيح تشغيل–إيقاف بالضوء، يجعل نظام Clivia-HT من الممكن اختبار ما إذا كان وجود RNA في بنية ما له أثر فعلي على سلوك الخلية. ستساعد هذه الأدوات الباحثين على الانتقال من صور ثابتة لمواقع RNA إلى تجارب سببية تكشف كيف تشكّل RNAs محددة استجابات الإجهاد وتكوّن القطرات واستقرار الجينوم.
الاستشهاد: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
الكلمات المفتاحية: تصوير RNA, تكاثفات مفصولة بالطور, تحلل RNA, كيمياء يمكن التحكم بها بالضوء, RNA طويل غير مرمَّز