Clear Sky Science · it
Un aptamero RNA ortogonale per la regolazione mirata dell’RNA in compartimenti subcellulari separati per fase
Osservare e controllare l’RNA all’interno di piccole goccioline cellulari
All’interno di ogni cellula, filamenti di RNA vengono continuamente sintetizzati, trasportati e degradati. Molti di questi RNA si radunano in piccole goccioline di tipo liquido che fluttuano nel citoplasma. Queste goccioline contribuiscono a organizzare la chimica della vita, ma sono difficili da studiare in tempo reale. Questo lavoro descrive un nuovo kit molecolare che permette agli scienziati sia di illuminare RNA specifici sia di cancellarli deliberatamente all’interno di queste goccioline, rivelando cosa fanno realmente quegli RNA nelle cellule vive.
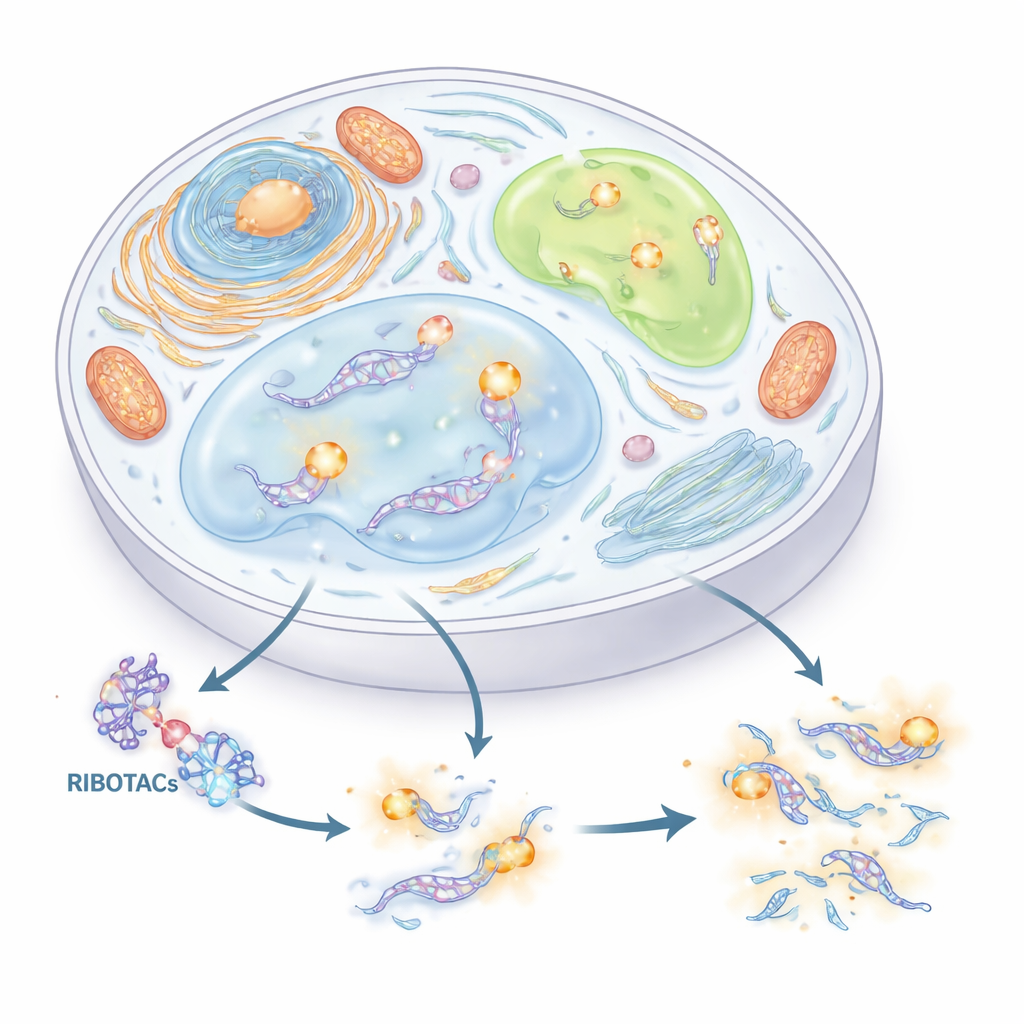
Una nuova maniglia per trovare e tagliare l’RNA
Gli autori hanno voluto costruire un sistema preciso e duplice per tracciare e controllare l’RNA. Hanno combinato due idee. La prima è un breve “tag” di RNA (un aptamero) che si piega in una forma in grado di legare una piccola molecola complementare. La seconda è una classe di molecole di sintesi chiamate RIBOTAC, che si agganciano a un RNA scelto e poi reclutano un enzima cellulare naturale che taglia l’RNA per distruggerlo. Attraverso uno screening accurato di migliaia di piccole molecole e centinaia di strutture di RNA, il gruppo ha identificato un tag RNA compatto, derivato da una sequenza virale chiamata HIV-TAR, e lo ha ottimizzato in un aptamero che chiamano HT. Hanno quindi costruito RIBOTAC in grado di riconoscere HT e richiamare l’enzima cellulare RNase L, trasformando qualsiasi RNA che porti HT in un bersaglio distruttibile in modo selettivo.
Aggiungere un colore brillante per seguire l’RNA nelle cellule vive
Per rendere visibili questi RNA targati, i ricercatori hanno fuso HT con un aptamero fluorescente separato chiamato Clivia, che emette un rosso-arancio quando lega un colorante innocuo (NBSI). Il tag ibrido risultante, Clivia-HT, conferisce a ogni RNA etichettato due abilità distinte: il lato Clivia attrae il colorante fluorescente per l’imaging, mentre il lato HT è riconosciuto dal RIBOTAC per il taglio controllato. Il team ha dimostrato che queste due funzioni operano in modo indipendente: il colorante illumina Clivia senza influenzare la degradazione, e il RIBOTAC si lega a HT e provoca il taglio senza attenuare il segnale fluorescente finché l’RNA non viene rimosso. Ripetendo Clivia-HT più volte su un singolo RNA, hanno aumentato la luminescenza a sufficienza per seguire le molecole etichettate nelle cellule vive.
Indagare ruoli nascosti dell’RNA nelle goccioline di stress
Con questo doppio tag, gli autori hanno esplorato gli RNA all’interno di compartimenti subcellulari separati per fase — strutture simili a goccioline che si formano senza membrane. Hanno prima inserito Clivia-HT nell’RNA piccolo nucleare U1, che marca gli U body, un tipo di granulo ricco di RNA. Quando le cellule sono state sottoposte a stress, questi U body si sono illuminati; aggiungendo il RIBOTAC mirato a HT, il segnale è stato gradualmente cancellato e il numero di U body è diminuito, ma solo in presenza dell’enzima tagliente RNase L. Poi hanno etichettato l’mRNA di ATF4 all’interno dei granuli di stress, goccioline che appaiono durante difficoltà cellulari. Sebbene l’RNA di ATF4 si accumulasse chiaramente in questi granuli e potesse essere degradato su richiesta, la sua rimozione non ha modificato come i granuli si formavano o si dissolv evano. Ciò indica che, nonostante la sua presenza, l’RNA di ATF4 non è un fattore determinante per la dinamica dei granuli di stress.
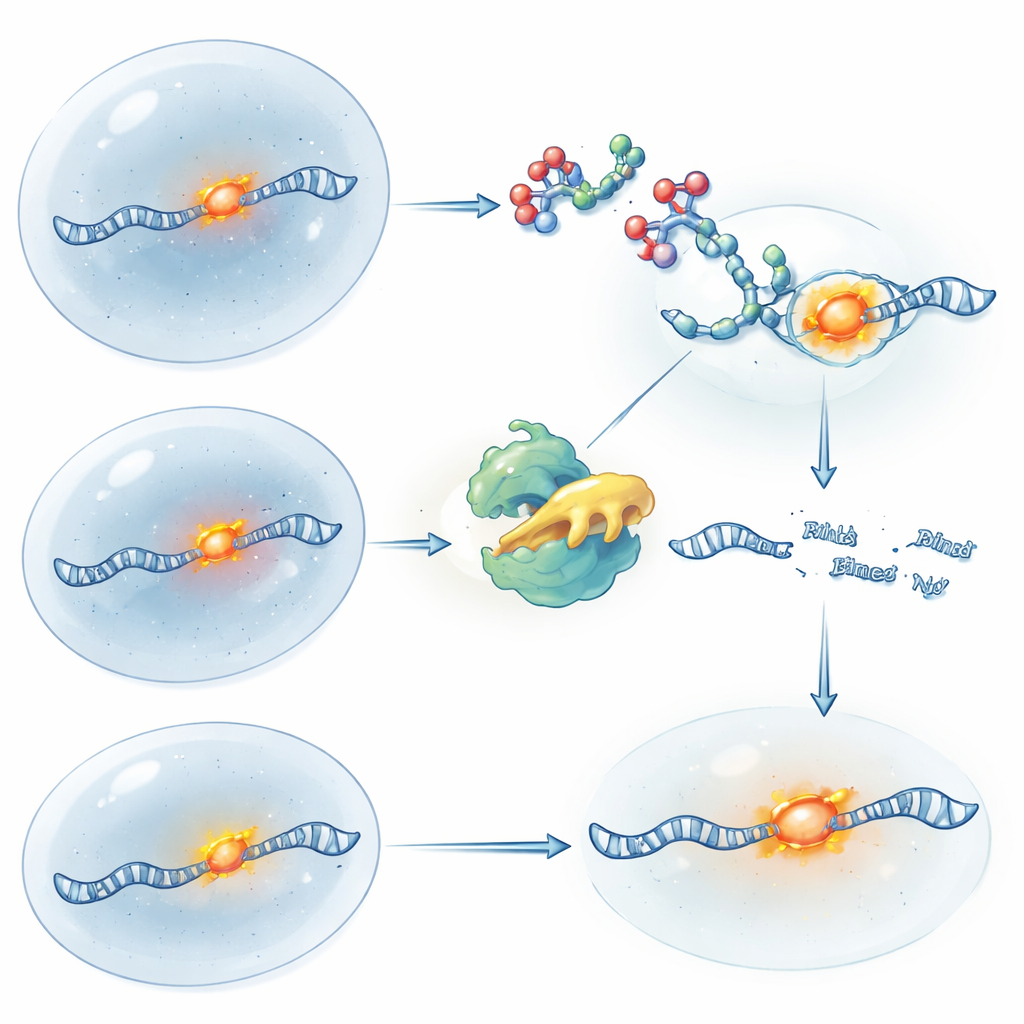
Accendere e spegnere il controllo dell’RNA con la luce
Per ottenere un controllo temporale ancora più fine, il team ha realizzato versioni sensibili alla luce dei loro RIBOTAC. In un progetto, la molecola è attiva all’inizio e viene “spenta” quando un breve impulso di luce ultravioletta cliva un collegamento di sicurezza incorporato, interrompendo ulteriori tagli e permettendo al nuovo RNA di ricostituirsi. Nell’altro progetto, il RIBOTAC è incapsulato e inattivo finché la luce non rimuove il gruppo bloccante, liberando improvvisamente la sua capacità di tagliare l’RNA. Usando questi strumenti su ATF4, i ricercatori hanno potuto imitare la logica di un knockout genico e della sua restaurazione solo con chimica e luce, mentre la posizione dell’RNA veniva monitorata tramite fluorescenza. Questo approccio consente agli scienziati di chiedersi non solo dove si trova un RNA, ma cosa succede alla cellula quando quell’RNA viene rimosso o ripristinato in momenti precisi.
Rivelare come un RNA lungo protegge il genoma
Gli autori si sono poi concentrati su un RNA lungo chiamato NORAD, noto per contribuire a preservare l’integrità dei cromosomi. NORAD si raccoglie con le proteine Pumilio in distinti condensati chiamati NP bodies nel citoplasma. Etichettando NORAD e un frammento minimale di NORAD (circPRE8) con Clivia-HT, hanno potuto visualizzare questi assemblaggi e cancellare selettivamente l’RNA. Quando NORAD o circPRE8 erano presenti, le proteine Pumilio formavano punteggiature luminose e le cellule mostravano meno errori nella segregazione cromosomica. Quando l’RNA etichettato è stato degradato dal RIBOTAC, i condensati sono scomparsi, le proteine Pumilio si sono disperse e gli errori cromosomici sono aumentati. Questi esperimenti mostrano che regioni specifiche di NORAD sono essenziali per formare goccioline protettive proteina–RNA che salvaguardano il genoma.
Cosa significa per la biologia cellulare futura
In sintesi, questo lavoro introduce un tag RNA versatile “plug-in” che permette a qualsiasi RNA scelto di essere sia visto sia cancellato con precisione all’interno della cellula, anche all’interno di delicati compartimenti di tipo liquido. Unendo imaging brillante e distruzione mirata, e aggiungendo interruttori acceso–spento basati sulla luce, il sistema Clivia-HT rende possibile verificare se la semplice presenza di un RNA in una struttura ha davvero importanza per il comportamento cellulare. Questo kit aiuterà i ricercatori a superare le immagini statiche della localizzazione dell’RNA verso esperimenti causali che rivelano come RNA specifici influenzino le risposte allo stress, la formazione di goccioline e la stabilità del genoma.
Citazione: Wang, J., Ma, K., Cao, X. et al. An orthogonal RNA aptamer for targeted RNA regulation in phase-separated subcellular compartments. Nat Commun 17, 4140 (2026). https://doi.org/10.1038/s41467-026-70638-2
Parole chiave: Imaging dell'RNA, condensati separati per fase, degradazione dell'RNA, chimica controllata dalla luce, RNA non codificante lungo