Clear Sky Science · tr
Fluoresan mikroskopi görüntülerinin çok görevli, çapraz dağılım restorasyonu için bir temel model
Gizli Hücre Dünyasının Daha Net Görünümleri
Modern biyoloji, hücrelerin içindeki yoğun yaşamı izlemek için mikroskoplara dayanıyor, ancak yakaladığımız görüntüler sıklıkla grenli, bulanık ya da ince ayrıntılardan yoksun oluyor. Bu makale, farklı deneyler arasında tek bir sistem içinde floresan mikroskopi görüntülerini temizleyip keskinleştirmek için tasarlanmış yeni bir yapay zeka (YZ) modeli olan FluoResFM’i sunuyor. Bilim insanları için bu, daha az deneme-yanılma ile daha net görüntüler; hastalar ve toplum içinse daha yüksek kaliteli verilere dayanan daha hızlı ve güvenilir biyolojik keşifler ve tıbbi içgörüler anlamına geliyor.
Neden Mikroskopi Görüntülerini Doğru Almak Bu Kadar Zor?
Floresan mikroskoplar, proteinleri, zarları ve organelleri parlatıp görünür kılarak gösterir; ancak bir ödün vardır: canlı hücreleri korumak için düşük ışık kullanmak genellikle gürültülü, soluk ve bulanık görüntüler üretir. Araştırmacılar bu görüntüleri onarmak için derin öğrenmeye yöneldi; sinir ağlarına gürültüyü gidermeyi, bulanıklığı tersine çevirmeyi veya çözünürlüğü artırmayı düşük ve yüksek kaliteli görüntü çiftleri üzerinden öğrettiler. Ancak mevcut araçların çoğu dar uzmanlar. Bir model yalnızca belirli bir yapıyı parazit azaltmak için etkin biçimde işleyebilir, bir diğeri yalnızca belirli bir mikroskop türü için keskinleştirme yapabilir. Böyle bir model yeni bir yapı veya görüntüleme düzenine uygulandığında kötü sonuç verebilir, sahte ayrıntılar uydurabilir veya gerçekleri çarpıtabilir—bu, bilim insanlarının hassas ölçümler için bu görüntülere güvendiği durumlarda ciddi bir sorundur.
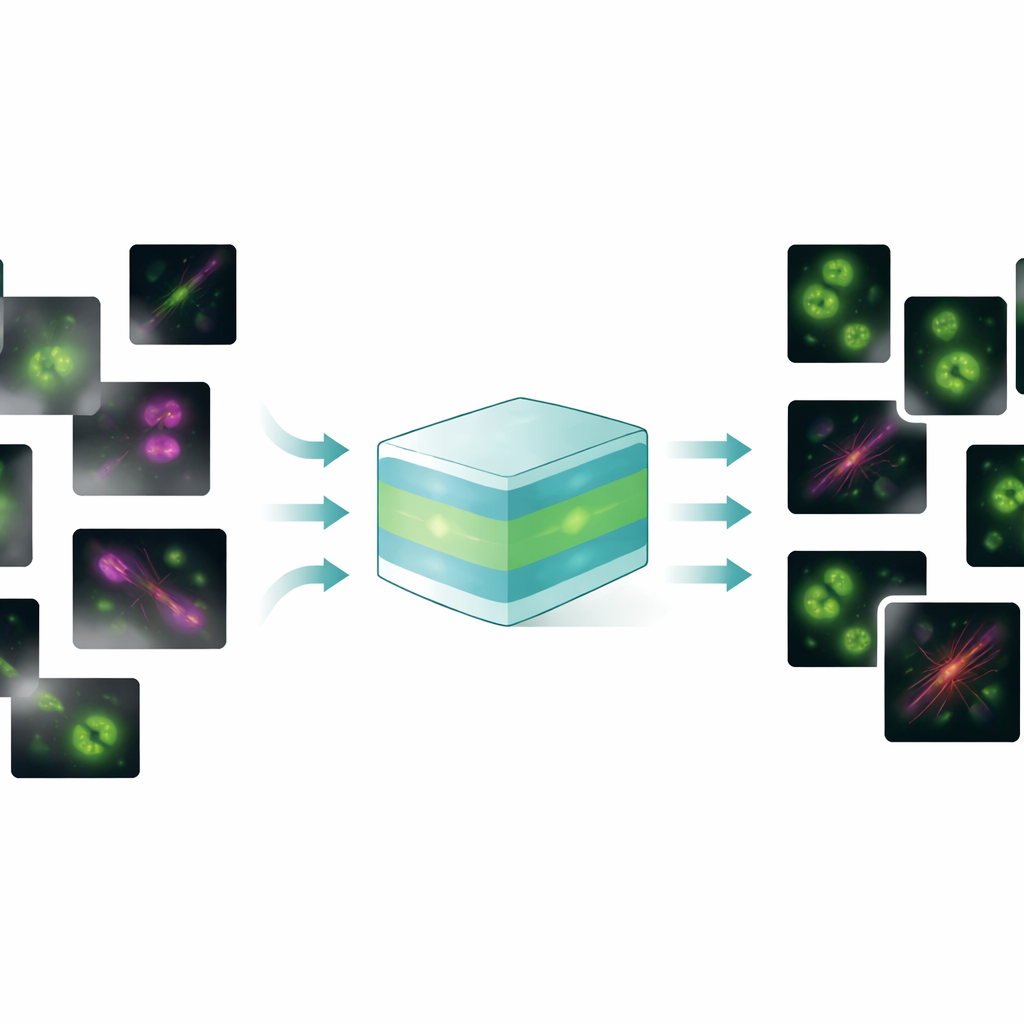
Bir Model, Birçok Görüntü Sorununu Ele Alır
FluoResFM genelci (generalist) olmayı hedefliyor: tek ve birleşik bir çerçevede gürültü giderme, bulanıklık düzeltme (dekonvolüsyon) ve süper-çözünürlük gibi birden fazla restorasyon görevini birçok hücre yapısı ve mikroskop türü arasında ele alabilen bir temel model. Yazarlar, klatrin kaplı çukurlardan ve mikrotübüllerden çekirdeklere, lizozomlara ve endoplazmik retikuluma kadar 20’den fazla biyolojik yapıyı kapsayan ve çeşitli görüntüleme koşullarından toplanmış 4,3 milyondan fazla görüntü parçası üzerinde eğittiler. FluoResFM’in çekirdeğinde, biyomedikal görüntü işleme için yaygın bir tasarım olan U‑Net tarzı bir mimari bulunuyor; ancak modele ek bilgi yön veriyor: hangi görevin yapıldığı, hangi yapının bulunduğu ve görüntülerin nasıl elde edildiğini kodlayan kısa metin açıklamaları. Bu metin istemleri, önceden eğitilmiş bir biyomedikal dil–görsel modeli kullanılarak sayısal özelliklere dönüştürülüyor ve ardından dikkat katmanları aracılığıyla ağın içindeki görüntü özellikleriyle birleştiriliyor. Etkide model sadece “bu resmi temizle” değil, “bu tür bir mikroskoptan alınmış bir mikrotübül görüntüsünü şu hedef kalitede gürültüden arındır” gibi daha yönlendirilmiş talimatlar alıyor; bu da doğru düzeltme türünü seçmesine yardımcı oluyor.
Metin Yönlendirmesi Görüntü Kalitesini Nasıl İyileştiriyor
Yazarlar, FluoResFM’i önde gelen bir önceki temel modelle ve metin yönlendirmesi olmayan bir sürümüyle karşılaştırdıklarında, metin farkındalığına sahip modelin bariz şekilde önde olduğunu gösterdiler. Yüzlerce dahili veri seti ve 51 daha önce görülmemiş harici veri seti boyunca, FluoResFM çeşitli keskinlik, benzerlik ve hata ölçütlerine göre yüksek kaliteli referanslara daha yakın görüntüler üretti. Özellikle çekirdek zarfındaki halka şeklindeki gözenekler veya dolaşık mikrotübül ağları gibi birbirine yakın özellikleri çözmede iyiydi ve komşu yapıları birbirine karıştırma eğiliminden kaçındı. Metinsel istemler aynı zamanda güçlü bir yönlendirme mekanizması sundu. Görev açıklamasını kavramsal olarak “gürültü giderme”den “süper-çözünürlüğe” değiştirmek, aynı ağı özdeş giriş görüntüleri üzerinde çok farklı işlemler yapmaya yönlendirdi. Benzer şekilde, yanlış yapı türü belirtmek modelin yanıltıcı desenler oluşturmasına neden oldu; örneğin retiküler bir ağı nokta benzeri lekelere çevirmek gibi—bu, hem modelin esnekliğini hem de doğru önbilginin önemini vurguluyor.
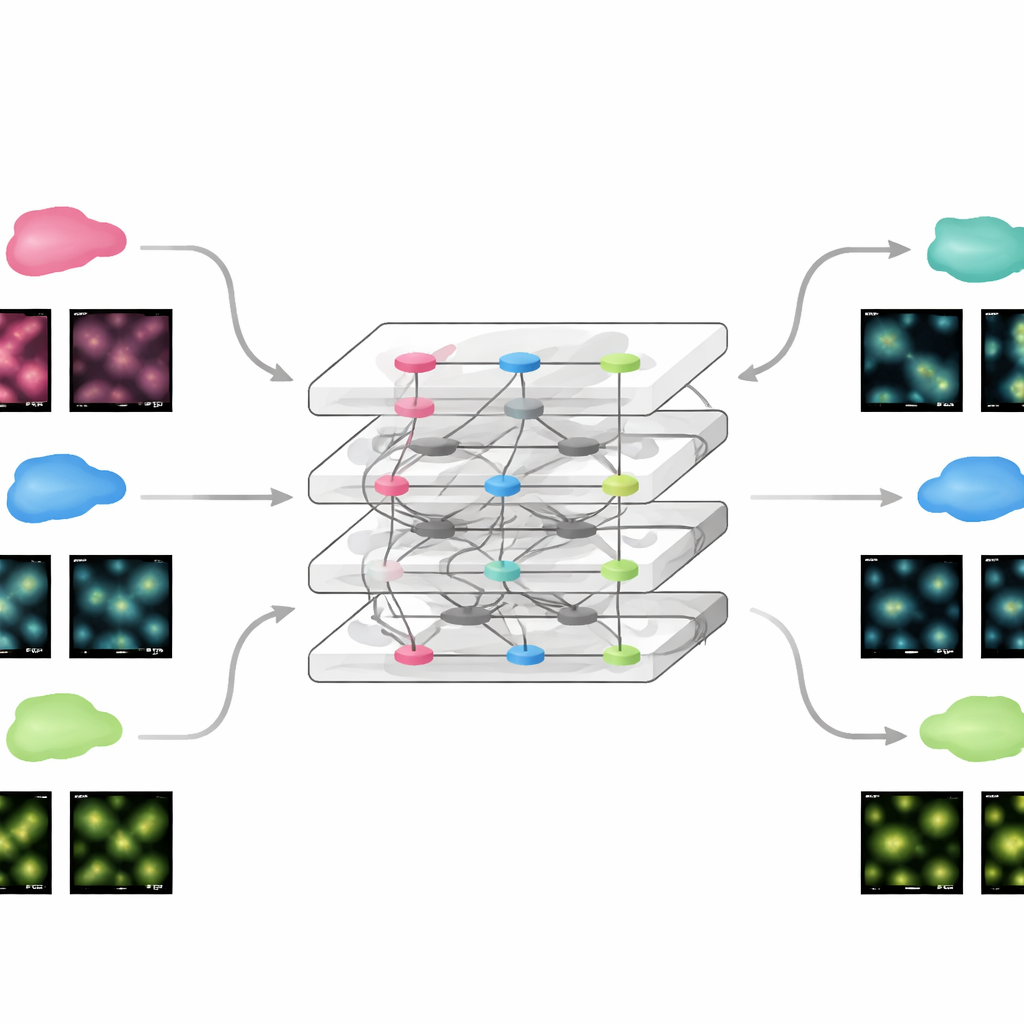
Yeni Deneylere Hızlı Uyarlanma
FluoResFM geniş bir deneyim tabanından başladığı için, yeni verilere oldukça az ek bilgiyle ince ayar yapılabiliyor. Ekip, ağın yalnızca küçük bir bölümünü yeni bir veri kümesinden tek bir örnek görüntü ile güncelleyerek modelin, sıfırdan yüzlerce görüntü üzerinde eğitilmiş geleneksel derin ağlara kıyaslanabilir performansa ulaştığını gösterdi. Bu, statik görüntüler için olduğu gibi hareketli hücresel yapıların zaman atlamalı filmleri için de geçerliydi; ince ayarlı model hem netlik hem de zaman içindeki ölçümlerin tutarlılığını iyileştirdi. Aynı strateji, FluoResFM’in orijinal eğitim görevlerinin ötesine, üç boyutlu hacim restorasyonu, 3B’den 2B’ye yüzey projeksiyonları, farklı eksenler boyunca çözünürlüğü daha dengeli hale getirme ve daha yüksek büyütme faktörleriyle başa çıkma gibi yeni görevlere genişletilmesini sağladı. Tüm bu durumlarda model daha net yapılar ve referans verilerle daha iyi nicel uyum üretti.
Diğer Araçların Hücreleri Daha Net Görmesini Sağlamak
FluoResFM sadece güzel görüntüler oluşturmanın bir yolu değil; görüntü kalitesine dayanan ardışık analiz araçlarını da güçlendiriyor. Yazarlar, restore edilmiş görüntüleri çekirdekleri, zarları ve organelleri çevrelemek için kullanılan popüler otomatik segmentasyon programlarına beslediklerinde, bu araçlar daha fazla nesne tespit etti, daha az kaçırdı ve uzman tarafından türetilmiş yer gerçeğiyle daha iyi uyuşan şekiller üretti. Bu iyileşme, birçok hücre türü ve yapıyı içeren onlarca veri setinde görüldü. Günlük kullanımı kolaylaştırmak için ekip, FluoResFM’i yaygın kullanılan etkileşimli bir görüntüleyici olan napari için bir eklenti olarak paketledi; böylece biyologlar kod yazmak zorunda kalmadan kendi iş akışları içinde görüntüleri restore edebilir ve modeli ince ayarlayabilirler.
Geleceğin Mikroskopisi İçin Ne Anlama Geliyor
Basitçe ifade etmek gerekirse, bu çalışma tek bir metinle yönlendirilen YZ modelinin çok çeşitli floresan mikroskopi görüntülerini temizleyip keskinleştirebildiğini, yeni deneylere hızla uyum sağlayabildiğini ve diğer analiz araçlarının performansını artırabildiğini gösteriyor. Ne görüntülendiği, nasıl yakalandığı ve hangi iyileştirmenin istendiği bilgilerini bir araya getirerek, FluoResFM izole olarak eğitilmiş görev-özgü ağlardan daha güvenilir görüntüler üretiyor. Daha fazla veri ve görev eklendikçe, böyle temel modeller mikroskopların standart yardımcıları haline gelebilir ve kusurlu ham görüntüleri, yaşayan hücrelerin gizli mimarisi ve dinamiklerine dair güvenilir pencerelere dönüştürebilir.
Atıf: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Anahtar kelimeler: fluoresan mikroskopi, görüntü restorasyonu, derin öğrenme, temel modeller, hücre görüntüleme